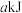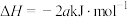下列依据热化学方程式得出的结论正确的是
| 选项 | 热化学方程式 | 结论 |
| A | 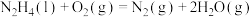 ΔH=-534 kJ·mol-1 ΔH=-534 kJ·mol-1 | N2H4的燃烧热为534 kJ·mol-1 |
| B |  ΔH=-57.3 kJ·mol-1 ΔH=-57.3 kJ·mol-1 | 含40 g NaOH的稀溶液与浓硫酸完全中和,放出的热量等于57.3kJ |
| C | C(s)+ O2(g)=CO(g) ΔH= - 110.5 kJ·mol-1 O2(g)=CO(g) ΔH= - 110.5 kJ·mol-1CO(g)+  O2(g)=CO2(g) ΔH=-283 kJ·mol-1 O2(g)=CO2(g) ΔH=-283 kJ·mol-1 | 2mol C(s) 完全燃烧放出787kJ热量 |
| D | C(石墨,s)= C(金刚石,s) ΔH= +1.5 kJ·mol-1 | 金刚石比石墨稳定 |
| A.A | B.B | C.C | D.D |
更新时间:2022-08-19 20:49:00
|
相似题推荐
【推荐1】下列说法或表示法正确的是
| A.由“C(s,石墨)→C(s,金刚石)△H=+119kJ·mol-1”可知金刚石比石墨稳定 |
| B.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,则氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O (1) △H=-285.8kJ·mol-1 |
| C.在101kPa时,1mol碳燃烧所放出的热量为碳的燃烧热 |
| D.等量的磷蒸气和磷固体分别完全燃烧,前者放出的热量多 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】如图所示,有关化学反应和能量变化的说法正确的是
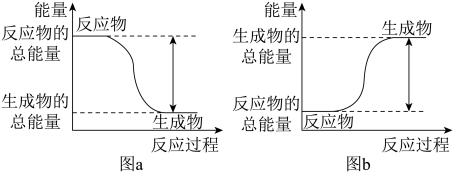

A.图a可以表示 和 和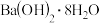 反应的能量变化 反应的能量变化 |
| B.图a中生成物比反应物稳定 |
| C.图b可以表示甲烷燃烧反应的能量变化 |
| D.图b表示的反应一定需要加热才能发生 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】下列依据热化学方程式得出的结论正确的是
| A.已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定 |
| B.H2(g)+F2(g)=2HF(g) ΔH=-270kJ•mol-1,则相同条件下,2molHF气体的能量小于1mol氢气和1mol氟气的能量之和 |
C.500°C、30MPa下,N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ•mol-1;将1.5molH2和过量的N2在此条件下充分反应,放出热量46.2kJ 2NH3(g) ΔH=-92.4kJ•mol-1;将1.5molH2和过量的N2在此条件下充分反应,放出热量46.2kJ |
| D.2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ•mol-1,则氢气的燃烧热为241.8kJ•mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】已知25℃时:
①HF(aq)+OH-(aq)=F-(aq)+H2O(l) ΔH1=-67.7 kJ·mol-1
②H+(aq)+OH-(aq)=H2O(l) ΔH2=-57.3 kJ·mol-1
③Ba2+(aq)+SO42—(aq)=BaSO4(s) ΔH3<0
下列说法正确的是( )
①HF(aq)+OH-(aq)=F-(aq)+H2O(l) ΔH1=-67.7 kJ·mol-1
②H+(aq)+OH-(aq)=H2O(l) ΔH2=-57.3 kJ·mol-1
③Ba2+(aq)+SO42—(aq)=BaSO4(s) ΔH3<0
下列说法正确的是( )
| A.HF的电离方程式及热效应:HF(aq)=H+(aq)+F-(aq) ΔH>0 |
| B.在氢氧化钠溶液与盐酸的反应中,盐酸量一定,氢氧化钠溶液量越多,中和热越大 |
| C.ΔH2=-57.3 kJ·mol-1是强酸和强碱在稀溶液中反应生成可溶盐的中和热 |
| D.稀硫酸与稀氢氧化钡溶液反应的热化学方程式为H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l)ΔH=-114.6 kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】已知:
 ;
;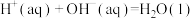
 则
则 的
的 等于
等于

 ;
;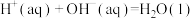
 则
则 的
的 等于
等于A.+1528.6  | B.+1473  |
C.−1528.6  | D.−1473  |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】已知H+(aq)+OH-(aq) ═ H2O(l) ΔH=-57.3 kJ/mol,下列说法正确的是
| A.当用稀CH3COOH(aq)和稀NaOH(aq)生成1 mol H2O(l)时,反应热为ΔH1,ΔH1>ΔH |
| B.用含1 mol HCl的稀HCl(aq)和40 g NaOH固体反应生成1 mol H2O(l)时,反应热为ΔH1,ΔH1>ΔH |
| C.含1 mol H2SO4的稀溶液和含1 mol Ba(OH)2的稀溶液完全反应,放出57.3 kJ的热量 |
| D.中和反应中,反应物的总能量低于生成物的总能量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列有关说法正确的是
| A.已知2C(s)+2O2(g)=2CO2(g) ΔH1,2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1<ΔH2 |
| B.已知2H2(g)+O2(g)=2H2O(g) ΔH=-571.6kJ·mol-1,则H2的燃烧热为285.8kJ·mol-1 |
C.已知HI(g) 1/2H2(g)+1/2I2(s) ΔH=-26.5kJ·mol-1,由此可知,在密闭容器中充入1mol HI气体,充分分解后可以放出26.5kJ的热量 1/2H2(g)+1/2I2(s) ΔH=-26.5kJ·mol-1,由此可知,在密闭容器中充入1mol HI气体,充分分解后可以放出26.5kJ的热量 |
| D.HCl和NaOH反应中和热ΔH=-57.3kJ·mol-1,H2SO4(aq)+Ca(OH)2(aq)=CaSO4(s)+2H2O(l) ΔH=-114.6kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列有关热化学方程式的叙述正确的是
A.已知 ,则金刚石比石墨稳定 ,则金刚石比石墨稳定 |
| B.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
C.甲烷的燃烧热为 ,则甲烷燃烧的热化学方程式可表示为 ,则甲烷燃烧的热化学方程式可表示为 |
D.已知 ,则含 ,则含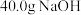 的稀溶液与稀醋酸完全中和,放出小于 的稀溶液与稀醋酸完全中和,放出小于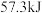 的热量 的热量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】二氧化碳甲烷化的研究对缓解能源危机意义重大。以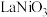 催化二氧化碳甲烷化的反应机理如图所示(
催化二氧化碳甲烷化的反应机理如图所示(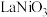 与
与 作用生成
作用生成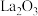 和
和 )。下列说法不正确的是
)。下列说法不正确的是
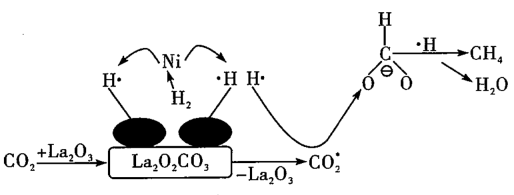
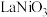 催化二氧化碳甲烷化的反应机理如图所示(
催化二氧化碳甲烷化的反应机理如图所示(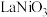 与
与 作用生成
作用生成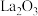 和
和 )。下列说法不正确的是
)。下列说法不正确的是
A.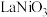 被 被 还原 还原 |
B.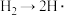 放出能量 放出能量 |
C.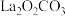 为中间产物 为中间产物 |
D.该反应的总方程式可表示为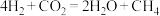 |
您最近一年使用:0次
【推荐2】某反应由两步反应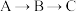 构成,它的反应能量曲线如图
构成,它的反应能量曲线如图 、
、 、
、 、
、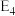 表示活化能
表示活化能 。下列有关叙述正确的是
。下列有关叙述正确的是


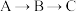 构成,它的反应能量曲线如图
构成,它的反应能量曲线如图 、
、 、
、 、
、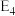 表示活化能
表示活化能 。下列有关叙述正确的是
。下列有关叙述正确的是


A.相同条件下 反应的速率小于 反应的速率小于 的速率 的速率 |
| B.两步反应均为吸热反应 |
| C.A、B、C中物质B最稳定 |
D.整个反应的 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】已知25℃时:
①HF(aq)+OH-(aq)=F-(aq)+H2O(l) ΔH1=-67.7 kJ·mol-1
②H+(aq)+OH-(aq)=H2O(l) ΔH2=-57.3 kJ·mol-1
③Ba2+(aq)+SO42—(aq)=BaSO4(s) ΔH3<0
下列说法正确的是( )
①HF(aq)+OH-(aq)=F-(aq)+H2O(l) ΔH1=-67.7 kJ·mol-1
②H+(aq)+OH-(aq)=H2O(l) ΔH2=-57.3 kJ·mol-1
③Ba2+(aq)+SO42—(aq)=BaSO4(s) ΔH3<0
下列说法正确的是( )
| A.HF的电离方程式及热效应:HF(aq)=H+(aq)+F-(aq) ΔH>0 |
| B.在氢氧化钠溶液与盐酸的反应中,盐酸量一定,氢氧化钠溶液量越多,中和热越大 |
| C.ΔH2=-57.3 kJ·mol-1是强酸和强碱在稀溶液中反应生成可溶盐的中和热 |
| D.稀硫酸与稀氢氧化钡溶液反应的热化学方程式为H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l)ΔH=-114.6 kJ·mol-1 |
您最近一年使用:0次

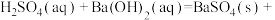
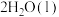
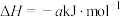
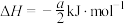


 的摩尔燃烧焓
的摩尔燃烧焓 )是
)是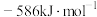
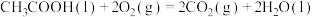
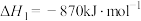

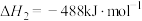
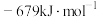
 下,将0.5
下,将0.5
 和1.5
和1.5 置于密闭容器中充分反应生成
置于密闭容器中充分反应生成 ,放出的热量为
,放出的热量为