某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。

请回答下列问题:
(1)甲池为_______ (填“原电池”“电解池”或“电镀池”),A电极的电极反应式为_______ 。
(2)丙池中F电极为_______ (填“正极”“负极”“阴极”或“阳极”),该池的总反应化学方程式方程式为_______ 。
(3)当乙池中C极质量减轻5.4 g时,甲池中B电极理论上消耗O2的体积为_______ mL(标准状况)。
(4)一段时间后,断开电键K,下列物质能使乙池恢复到反应前浓度的是_______(填选项字母)。
(5)某兴趣小组同学如图装置进行实验,观察到两极均有气体产生,Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍澄清。查阅资料知,高铁酸根离子(FeO )在溶液中呈紫红色。
)在溶液中呈紫红色。
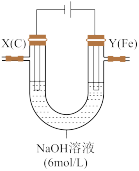
①电解过程中,X极溶液的pH_______ (填“增大”“减小”或“不变”)。
②电解过程中,Y极发生的电极反应为4OH--4e-=2H2O+O2↑和_______ 。

请回答下列问题:
(1)甲池为
(2)丙池中F电极为
(3)当乙池中C极质量减轻5.4 g时,甲池中B电极理论上消耗O2的体积为
(4)一段时间后,断开电键K,下列物质能使乙池恢复到反应前浓度的是_______(填选项字母)。
| A.Cu | B.CuO | C.Cu(OH)2 | D.Cu2(OH)2CO3 |
 )在溶液中呈紫红色。
)在溶液中呈紫红色。
①电解过程中,X极溶液的pH
②电解过程中,Y极发生的电极反应为4OH--4e-=2H2O+O2↑和
更新时间:2022-08-18 18:43:39
|
相似题推荐
【推荐1】如图所示,某化学兴趣小组设计了一个燃料电池,并探究氯碱工业原理和粗铜精炼原理,其中乙装置中X为阳离子交换膜。根据要求回答相关问题:

(1)通入氧气的电极为_____ (填“正极”或“负极”),通氢气一极的电极反应式为_________________ ;
(2)铁电极为_______ (填“阳极”或“阴极”),乙装置中电解反应的化学方程式为_________________ 。
(3)若在标准状况下,有1.12 L氧气参加反应,丙装置中阴极增重的质量为______ g;
(4)某粗铜中含有铁、金、银和铂等杂质,通过电解精制后,为从电解液中制得硫酸铜晶体(CuSO4·5H2O),设计了如下工艺流程:
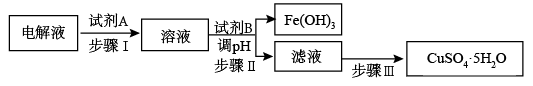
已知:几种金属阳离子开始沉淀和沉淀完全的pH:
①步骤I中加入试剂A的目的是_____________________________ ,试剂A应选择______ (填序号);
a.氯气 b.过氧化氢 C.酸性高锰酸钾溶液
选择该试剂的原因_____________________________________________________ ;
②步骤II中试剂B为_________ ,调节pH的范围是___________ ;
③步骤III的操作是加热浓缩、_______ 、___________ 。

(1)通入氧气的电极为
(2)铁电极为
(3)若在标准状况下,有1.12 L氧气参加反应,丙装置中阴极增重的质量为
(4)某粗铜中含有铁、金、银和铂等杂质,通过电解精制后,为从电解液中制得硫酸铜晶体(CuSO4·5H2O),设计了如下工艺流程:

已知:几种金属阳离子开始沉淀和沉淀完全的pH:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
a.氯气 b.过氧化氢 C.酸性高锰酸钾溶液
选择该试剂的原因
②步骤II中试剂B为
③步骤III的操作是加热浓缩、
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】高纯硫酸锰在电池材料领域有重要用途。以软锰矿(主要成分为MnO2,含有少量铁和铝的氧化物)、硫铁矿(主要成分为FeS2)、钛白废酸(主要成分为H2SO4)为原料制备MnSO4·H2O的工艺流程如图:
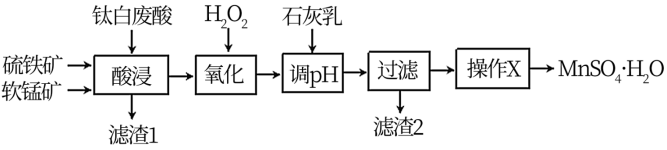
(1)“酸浸”时,为提高锰的浸出率,可采取的措施是___ ,“酸浸”过程中钛白废酸不宜过量太多,原因是___ 。
(2)在“酸浸”过程中,FeS2和MnO2颗粒组成两个原电池,如图所示,其中,MnO2原电池反应迅速,而FeS2原电池由于生成的硫覆盖在FeS2颗粒表面,溶解速率受阻变慢。
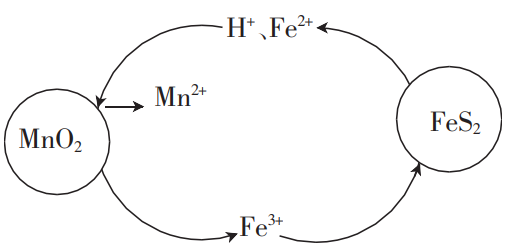
①MnO2原电池中,MnO2为原电池的___ (填“正极”或“负极”),每消耗1molMnO2,生成___ molFe3+。
②FeS2原电池负极上的电极反应式为___ 。
(3)已知部分金属阳离子开始沉淀和沉淀完全的pH如表:
①要除去Fe3+和Al3+,需要调节溶液的pH的范围为___ 。
②加入CaCO3也可以将滤液中的Fe3+转化为Fe(OH)3而除去,该反应的化学方程式为___ 。
③若石灰乳用量过大,则MnSO4·H2O的产量会___ (填“增加”、“减少”或“无影响”)。
(4)“操作X”为蒸发浓缩、___ 、过滤、洗涤、烘干。
(5)某工厂用10t软锰矿(含87%MnO2)制备MnSO4·H2O,最终得到MnSO4·H2O13.52t,则MnSO4·H2O的产率为___ 。

(1)“酸浸”时,为提高锰的浸出率,可采取的措施是
(2)在“酸浸”过程中,FeS2和MnO2颗粒组成两个原电池,如图所示,其中,MnO2原电池反应迅速,而FeS2原电池由于生成的硫覆盖在FeS2颗粒表面,溶解速率受阻变慢。

①MnO2原电池中,MnO2为原电池的
②FeS2原电池负极上的电极反应式为
(3)已知部分金属阳离子开始沉淀和沉淀完全的pH如表:
| 开始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.9 | 3.2 |
| Al3+ | 3.4 | 4.7 |
| Mn2+ | 8.1 | 10.1 |
| Fe2+ | 7 | 9.5 |
②加入CaCO3也可以将滤液中的Fe3+转化为Fe(OH)3而除去,该反应的化学方程式为
③若石灰乳用量过大,则MnSO4·H2O的产量会
(4)“操作X”为蒸发浓缩、
(5)某工厂用10t软锰矿(含87%MnO2)制备MnSO4·H2O,最终得到MnSO4·H2O13.52t,则MnSO4·H2O的产率为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】Ⅰ.研原电池是化学对人类的一项重大贡献。
(1)如图是甲烷燃料电池原理示意图,回答下列问题:
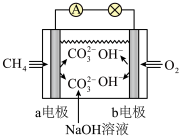
①电池的负极是_______ (填“a”或“b”)电极,该极的电极反应式为_______
②电池工作一段时间后电解质溶液的pH_______ (填 “增大”、“减小”或“不变”)。
(2)熔融盐燃料电池具有很高的发电效率,因而受到重视。可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650℃下工作的燃料电池。请完成有关的电池反应式:
负极反应式:2CO+2 —4e—=4CO2;
—4e—=4CO2;
正极反应式:_______ ,总电池反应式:_______
Ⅱ.“神舟九号”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。
(3)飞船在光照区运行时,太阳能电池帆板将太阳能转化为电能,除供给飞船使用外,多余部分用镉镍蓄电池储存起来。其工作原理为Cd+2NiO(OH)+2H2O Cd(OH)2 +2Ni(OH)2;当飞船运行到阴影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性
Cd(OH)2 +2Ni(OH)2;当飞船运行到阴影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性 _______ (填“增大”“减小”或“不变”)。
(4)紧急状况下,应急电池会自动启动,工作原理为Zn+Ag2O+H2O 2Ag+ Zn(OH)2,负极的电极反应式为
2Ag+ Zn(OH)2,负极的电极反应式为_______ 。
(1)如图是甲烷燃料电池原理示意图,回答下列问题:

①电池的负极是
②电池工作一段时间后电解质溶液的pH
(2)熔融盐燃料电池具有很高的发电效率,因而受到重视。可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650℃下工作的燃料电池。请完成有关的电池反应式:
负极反应式:2CO+2
 —4e—=4CO2;
—4e—=4CO2;正极反应式:
Ⅱ.“神舟九号”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。
(3)飞船在光照区运行时,太阳能电池帆板将太阳能转化为电能,除供给飞船使用外,多余部分用镉镍蓄电池储存起来。其工作原理为Cd+2NiO(OH)+2H2O
 Cd(OH)2 +2Ni(OH)2;当飞船运行到阴影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性
Cd(OH)2 +2Ni(OH)2;当飞船运行到阴影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性 (4)紧急状况下,应急电池会自动启动,工作原理为Zn+Ag2O+H2O
 2Ag+ Zn(OH)2,负极的电极反应式为
2Ag+ Zn(OH)2,负极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】Ⅰ.一定条件下,容积2L的密闭容器中,将2 L气体和3
L气体和3 M气体混合,发生如下反应:
M气体混合,发生如下反应: ,10s末,生成2.4
,10s末,生成2.4 R,测得Q的浓度为0.4
R,测得Q的浓度为0.4 。
。
(1)前10s内用M表示的化学反应速率为_______ 。
(2)化学方程式中x值为_______ 。
(3)10s末L的转化率是_______ 。
(4)下列说法可以说明该反应已达平衡的是_______ 。(填序号)
①体系内压强不再改变
②容器内气体的密度不再改变
③混合气体的平均相对分子质量不再改变
④单位时间内消耗3 M的同时生成3
M的同时生成3 R
R
⑤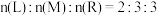
Ⅱ.乙醇燃料电池因其无污染,且原料来源广可再生被人们青睐。现有如下图所示装置,所有电极均为 ,请按要求回答下列问题:
,请按要求回答下列问题:
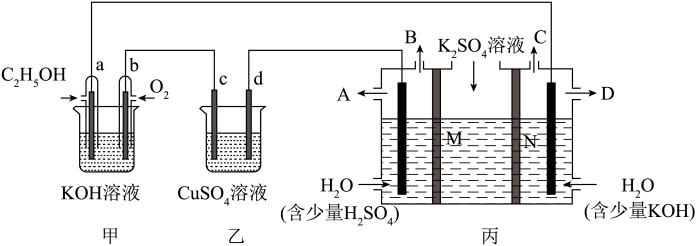
(5)写出甲装置a极的电极反应式_______ 。
(6)若乙池中 溶液足量,当b极消耗标准状况下
溶液足量,当b极消耗标准状况下 11.2
11.2 时,d电极增重
时,d电极增重_______ g。
(7)现用丙装置电解硫酸钾溶液制取氢气、氧气、硫酸和氢氧化钾,其中M、N为离子交换膜,只允许某些离子通过,则N为_______ 离子交换膜(填“阴”或“阳”),产生B气体的电极反应式为_______ 。
 L气体和3
L气体和3 M气体混合,发生如下反应:
M气体混合,发生如下反应: ,10s末,生成2.4
,10s末,生成2.4 R,测得Q的浓度为0.4
R,测得Q的浓度为0.4 。
。(1)前10s内用M表示的化学反应速率为
(2)化学方程式中x值为
(3)10s末L的转化率是
(4)下列说法可以说明该反应已达平衡的是
①体系内压强不再改变
②容器内气体的密度不再改变
③混合气体的平均相对分子质量不再改变
④单位时间内消耗3
 M的同时生成3
M的同时生成3 R
R⑤
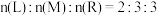
Ⅱ.乙醇燃料电池因其无污染,且原料来源广可再生被人们青睐。现有如下图所示装置,所有电极均为
 ,请按要求回答下列问题:
,请按要求回答下列问题:
(5)写出甲装置a极的电极反应式
(6)若乙池中
 溶液足量,当b极消耗标准状况下
溶液足量,当b极消耗标准状况下 11.2
11.2 时,d电极增重
时,d电极增重(7)现用丙装置电解硫酸钾溶液制取氢气、氧气、硫酸和氢氧化钾,其中M、N为离子交换膜,只允许某些离子通过,则N为
您最近一年使用:0次
【推荐2】高铁电池作为新型可充电电池,具有放电曲线平坦,高能高容量,原料丰富,绿色无污染等优点。
I.如图为简易的高铁电池的工作装置。已知:放电后,两极都产生红褐色悬浮物。

请回答下列问题:
(1)该电池放电时的总反应为___________ 。
(2)该电池充电时阳极反应的电极反应方程式为___________ 。
(3)放电时,此盐桥中阴离子的运动方向是__________ (填“从左向右”或“从右向左”)。
II.现用蓄电池Fe+NiO2+2H2O Fe(OH)2+Ni(OH)2为电源,制取少量高铁酸钾。反应装置如图所示:
Fe(OH)2+Ni(OH)2为电源,制取少量高铁酸钾。反应装置如图所示:
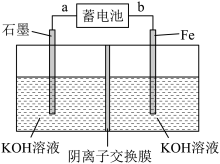
(1)电解时,石墨电极连接的a极上放电的物质为__________ (填“Fe”或“NiO2”)。
(2)写出电解池中铁电极发生的电极反应式__________ 。
(3)当消耗掉0.1molNiO2时,生成高铁酸钾__________ g。
I.如图为简易的高铁电池的工作装置。已知:放电后,两极都产生红褐色悬浮物。

请回答下列问题:
(1)该电池放电时的总反应为
(2)该电池充电时阳极反应的电极反应方程式为
(3)放电时,此盐桥中阴离子的运动方向是
II.现用蓄电池Fe+NiO2+2H2O
 Fe(OH)2+Ni(OH)2为电源,制取少量高铁酸钾。反应装置如图所示:
Fe(OH)2+Ni(OH)2为电源,制取少量高铁酸钾。反应装置如图所示:
(1)电解时,石墨电极连接的a极上放电的物质为
(2)写出电解池中铁电极发生的电极反应式
(3)当消耗掉0.1molNiO2时,生成高铁酸钾
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】按照要求回答下列问题。
(1)工业上,在强碱性条件下用电解法除去废水中的 ,装置如图所示,依次发生的反应有:
,装置如图所示,依次发生的反应有:
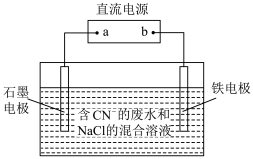
i.
ii.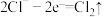
iii.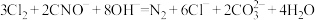
①a为电源_______ 极。
②通电过程中溶液pH不断_______ (填“增大”“减小”或“不变”)。
③除去1mol ,外电路中至少需要转移
,外电路中至少需要转移_______ mol电子。
④为了使电解池连续工作,需要不断补充_______ 。
(2)用NaOH溶液吸收烟气中的 ,将所得的
,将所得的 溶液进行电解,可循环再生NaOH,同时得到
溶液进行电解,可循环再生NaOH,同时得到 ,其原理如图所示(电极材料为石墨)。
,其原理如图所示(电极材料为石墨)。
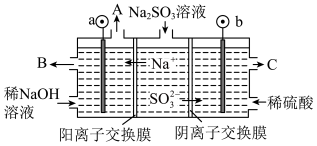
① C口流出的物质是_______ 。
② 放电的电极反应式为
放电的电极反应式为_______ 。
③电解过程中阴极区碱性明显增强,用平衡移动原理解释原因:_______ 。
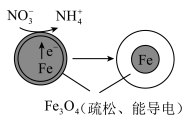
(3)用零价铁(Fe)去除水体中的硝酸盐( )已成为环境修复研究的热点之一、Fe还原水体中的
)已成为环境修复研究的热点之一、Fe还原水体中的 的反应原理如图所示。正极的电极反应式是
的反应原理如图所示。正极的电极反应式是_______ 。
(1)工业上,在强碱性条件下用电解法除去废水中的
 ,装置如图所示,依次发生的反应有:
,装置如图所示,依次发生的反应有:
i.

ii.
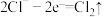
iii.
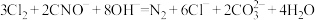
①a为电源
②通电过程中溶液pH不断
③除去1mol
 ,外电路中至少需要转移
,外电路中至少需要转移④为了使电解池连续工作,需要不断补充
(2)用NaOH溶液吸收烟气中的
 ,将所得的
,将所得的 溶液进行电解,可循环再生NaOH,同时得到
溶液进行电解,可循环再生NaOH,同时得到 ,其原理如图所示(电极材料为石墨)。
,其原理如图所示(电极材料为石墨)。
① C口流出的物质是
②
 放电的电极反应式为
放电的电极反应式为③电解过程中阴极区碱性明显增强,用平衡移动原理解释原因:
(3)用零价铁(Fe)去除水体中的硝酸盐(
 )已成为环境修复研究的热点之一、Fe还原水体中的
)已成为环境修复研究的热点之一、Fe还原水体中的 的反应原理如图所示。正极的电极反应式是
的反应原理如图所示。正极的电极反应式是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
已知: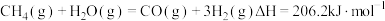
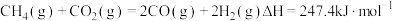
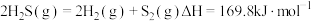
(1) 热分解制氢时常向反应器中通入一定比例空气,使部分
热分解制氢时常向反应器中通入一定比例空气,使部分 燃烧,其目的是
燃烧,其目的是___________ 。燃烧生成的 与
与 进一步反应,生成物在常温下均非气体,其中一种物质的摩尔质量为
进一步反应,生成物在常温下均非气体,其中一种物质的摩尔质量为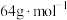 ,写出该反应的化学方程式:
,写出该反应的化学方程式:___________ 。
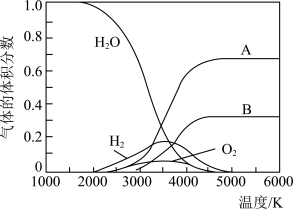
(2) 的热分解也可得到
的热分解也可得到 ,高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A、B表示的物质依次是
,高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A、B表示的物质依次是___________ 。
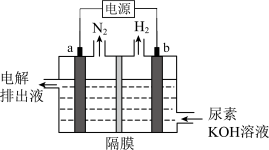
(3)电解尿素 的碱性溶液制氢的装置示意图见图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为
的碱性溶液制氢的装置示意图见图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为___________ 。
(4)镁铝合金(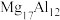 )是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为
)是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为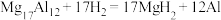 。得到的混合物
。得到的混合物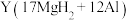 在一定条件下释放出氢气。
在一定条件下释放出氢气。
①熔炼制备镁铝合金(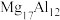 )时通入氩气的目的是
)时通入氩气的目的是___________ 。
②在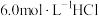 溶液中,混合物Y能完全释放出
溶液中,混合物Y能完全释放出 。
。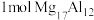 完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出
完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出 的物质的量为
的物质的量为___________ 。
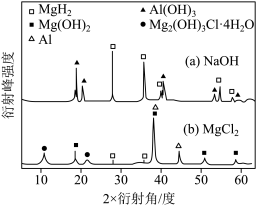
③在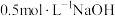 和
和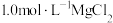 溶液中,混合物Y均只能部分放出氢气,反应后残留固体物质X-态物质是否存在,不同晶态物质出现衍射峰的衍射角射线衍射谱图如图所示(X-射线衍射可用于判断某晶不同)。在上述
溶液中,混合物Y均只能部分放出氢气,反应后残留固体物质X-态物质是否存在,不同晶态物质出现衍射峰的衍射角射线衍射谱图如图所示(X-射线衍射可用于判断某晶不同)。在上述 溶液中,混合物Y中产生氢气的主要物质是
溶液中,混合物Y中产生氢气的主要物质是_________ 。(填化学式)。
已知:
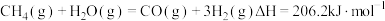
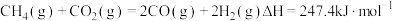
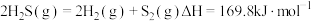
(1)
 热分解制氢时常向反应器中通入一定比例空气,使部分
热分解制氢时常向反应器中通入一定比例空气,使部分 燃烧,其目的是
燃烧,其目的是 与
与 进一步反应,生成物在常温下均非气体,其中一种物质的摩尔质量为
进一步反应,生成物在常温下均非气体,其中一种物质的摩尔质量为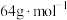 ,写出该反应的化学方程式:
,写出该反应的化学方程式:(2)
 的热分解也可得到
的热分解也可得到 ,高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A、B表示的物质依次是
,高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A、B表示的物质依次是
(3)电解尿素
 的碱性溶液制氢的装置示意图见图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为
的碱性溶液制氢的装置示意图见图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为
(4)镁铝合金(
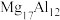 )是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为
)是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为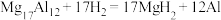 。得到的混合物
。得到的混合物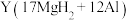 在一定条件下释放出氢气。
在一定条件下释放出氢气。①熔炼制备镁铝合金(
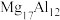 )时通入氩气的目的是
)时通入氩气的目的是②在
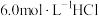 溶液中,混合物Y能完全释放出
溶液中,混合物Y能完全释放出 。
。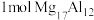 完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出
完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出 的物质的量为
的物质的量为③在
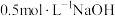 和
和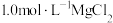 溶液中,混合物Y均只能部分放出氢气,反应后残留固体物质X-态物质是否存在,不同晶态物质出现衍射峰的衍射角射线衍射谱图如图所示(X-射线衍射可用于判断某晶不同)。在上述
溶液中,混合物Y均只能部分放出氢气,反应后残留固体物质X-态物质是否存在,不同晶态物质出现衍射峰的衍射角射线衍射谱图如图所示(X-射线衍射可用于判断某晶不同)。在上述 溶液中,混合物Y中产生氢气的主要物质是
溶液中,混合物Y中产生氢气的主要物质是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】氯化亚铜(CuCl)常用作有机合成工业中的催化剂,是一种白色粉末;微溶于水、不溶于乙醇及稀硫酸。工业用如下流程,从酸性废液(主要含Cu2+、Fe3+、H+、Cl-)中制备氯化亚铜。
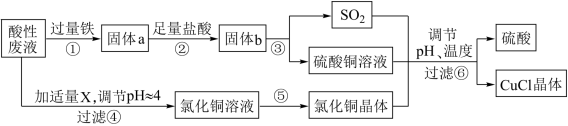
请回答下列问题:
(1)写出步骤①中发生的两个主要反应的离子方程式:_________________________ 。
(2)步骤②的操作名称是:_____________ 。
(3)步骤④中所加物质X为:__________ 。
(4)步骤⑤的操作是:___________________________________________________ 。
(5)步骤⑥应调节溶液pH呈酸性,且用乙醇洗涤CuCl晶体,目的是:______________ 。
(6)在CuCl的生成过程中,可以循环利用的物质是______________ ,理论上_____ (填“是”或“否”)需要补充(不考虑调节等消耗);理由是__________________________________ 。
(7)工业上还可以采用以碳棒为电极电解CuCl2溶液得到CuCl。写出电解CuCl2溶液中的阴极上发生的电极反应___________________________________________ 。

请回答下列问题:
(1)写出步骤①中发生的两个主要反应的离子方程式:
(2)步骤②的操作名称是:
(3)步骤④中所加物质X为:
(4)步骤⑤的操作是:
(5)步骤⑥应调节溶液pH呈酸性,且用乙醇洗涤CuCl晶体,目的是:
(6)在CuCl的生成过程中,可以循环利用的物质是
(7)工业上还可以采用以碳棒为电极电解CuCl2溶液得到CuCl。写出电解CuCl2溶液中的阴极上发生的电极反应
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】氨氮废水中的氮元素多以 和NH3等形式存在,是造成河流及湖泊富营养化的主要因素之一。
和NH3等形式存在,是造成河流及湖泊富营养化的主要因素之一。
(1)高浓度氨氮废水一种预处理的方式是加NaOH溶液,调节pH至9后,升温至30℃通空气将氨赶出并回收。用离子方程式表示NaOH溶液的作用:___________ ;升温至30℃的作用是 ___________ 。
次氯酸钠法处理废水中的氨氮原理如下:
i.NH3(aq)+HClO(aq)=NH2Cl(aq)+H2O(l)
ii.2NH2Cl(aq)+HClO(aq)=N2(g)+H2O(l)+3HCl(aq)
(2)以上反应中HClO的来源是___________ (用离子方程式表示)。
(3)溶液pH对次氯酸钠去除氨氮有较大的影响(如图所示)。在pH较低时,溶液中有能使带火星木条复燃的气体生成,氨氮去除效率较低,其原因是___________ (用化学方程式表示);在pH较高时,氨氮去除率下降的原因是 ___________ 。
(4)•OH的电子式为___________ ,其中氧元素的化合价为 ___________ 。
(5)H2O2生成•OH时断裂的化学键为 ___________。
(6)阴极生成H2O2的电极反应为:___________ 。
生物膜式厌氧氨氧化是一种较先进的氨氮废水处理工艺,通过在填料上附着不同菌种的生物膜来实现低能耗脱氨氮,其过程如图所示。___________ 。
(8)关于生物膜式厌氧氨氧化反应相关说法正确的是 ___________。
 和NH3等形式存在,是造成河流及湖泊富营养化的主要因素之一。
和NH3等形式存在,是造成河流及湖泊富营养化的主要因素之一。(1)高浓度氨氮废水一种预处理的方式是加NaOH溶液,调节pH至9后,升温至30℃通空气将氨赶出并回收。用离子方程式表示NaOH溶液的作用:
次氯酸钠法处理废水中的氨氮原理如下:
i.NH3(aq)+HClO(aq)=NH2Cl(aq)+H2O(l)
ii.2NH2Cl(aq)+HClO(aq)=N2(g)+H2O(l)+3HCl(aq)
(2)以上反应中HClO的来源是
(3)溶液pH对次氯酸钠去除氨氮有较大的影响(如图所示)。在pH较低时,溶液中有能使带火星木条复燃的气体生成,氨氮去除效率较低,其原因是

(4)•OH的电子式为
(5)H2O2生成•OH时断裂的化学键为 ___________。
| A.离子键 | B.氢键 | C.极性共价键 | D.非极性共价键 |
(6)阴极生成H2O2的电极反应为:
生物膜式厌氧氨氧化是一种较先进的氨氮废水处理工艺,通过在填料上附着不同菌种的生物膜来实现低能耗脱氨氮,其过程如图所示。
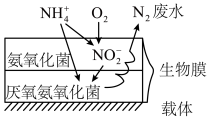
(8)关于生物膜式厌氧氨氧化反应相关说法正确的是 ___________。
| A.每生成22.4LN2消耗相同条件下33.6LO2 |
| B.随着氨氮去除,废水pH逐渐降低 |
| C.将上下两层菌种交换,对氨氮脱除无影响 |
D.该工艺总反应 H可能大于0 H可能大于0 |
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液c;M、N是两块电极板,通过导线与直流电源相连。

请回答以下问题:
(1)若M、N都是惰性电极,c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试液,则:
①电解池中M极上的电极反应式是_____ 。检验该电极反应产物的方法是______ 。
②在N极附近观察到的现象是______ 。
(2)若要进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,电解液c选用CuSO4溶液,则:(说明:杂质发生的电极反应不必写出)
①M电极的材料是_____ ,电极反应式是__________ 。
②下列说法正确的是________ 。
A.电能全部转化为化学能
B.在电解精炼中,电解液中有Al3+、Zn2+产生
C.溶液中Cu2+向阳极移动
D.阳极泥中可回收Ag、Pt、Au等金属
(3)用惰性电极电解CuSO4溶液。若阴极析出Cu的质量为16g,则阳极上产生的气体在标准状况下的体积为___________ L 。

请回答以下问题:
(1)若M、N都是惰性电极,c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试液,则:
①电解池中M极上的电极反应式是
②在N极附近观察到的现象是
(2)若要进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,电解液c选用CuSO4溶液,则:(说明:杂质发生的电极反应不必写出)
①M电极的材料是
②下列说法正确的是
A.电能全部转化为化学能
B.在电解精炼中,电解液中有Al3+、Zn2+产生
C.溶液中Cu2+向阳极移动
D.阳极泥中可回收Ag、Pt、Au等金属
(3)用惰性电极电解CuSO4溶液。若阴极析出Cu的质量为16g,则阳极上产生的气体在标准状况下的体积为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】二甲醚(CH3OCH3)是一种新兴化工原料,具有甲基化反应性能。
l.二甲醚的生产:
二甲醚的生产原理之一是利用甲醇脱水成二甲醚,化学方程式如下:
反应i 2CH3OH(g) CH3OCH3(g)+H2O(g) △H1
CH3OCH3(g)+H2O(g) △H1
(1)已知:甲醇、二甲醚的气态标准燃烧热分别为-761.5kJ·mol-1、-1455.2kJ·mol-1,且H2O(g)=H2O(1) △H=-44.0kJ·mol-1。
反应i的△H1=___________ kJ·mol-1。
(2)反应i中甲醇转化率、二甲醚选择性的百分率与不同催化剂的关系如图1所示,生产时,选择的最佳催化剂是___________ 。

(3)选定催化剂后,测得平衡时的甲醇转化率与温度的关系如图2所示。经研究产物的典型色谱图发现该过程主要存在的副反应为:
反应ii 2CH3OH(g) C2H4(g)+2H2O(g) △H2=-29.1kJ·mol-1
C2H4(g)+2H2O(g) △H2=-29.1kJ·mol-1
①工业上生产二甲醚的温度通常在270-300℃,高于330℃之后,甲醇转化率下降,根据化学平衡移动原理分析原因是______________________ ;根据化学反应速率变化分析原因是______________________ 。
②某温度下,以CH3OH(g)为原料,平衡时各物质的分压数据如下表:

则反应i中,CH3OH(g)的平衡转化率α=___________ ,反应i的平衡常数Kp=__________ (用平衡分压代替平衡浓度计算;结果保留两位有效数字)
Ⅱ.二甲醚的应用:
(4)图3为绿色电源“直接二甲醚燃料电池”的工作原理示意图:
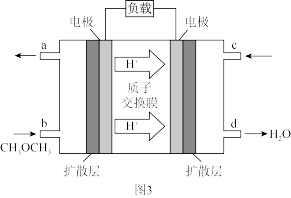
①该电池的负极反应式为:______________________ ;
②若串联该燃料电池电解硫酸钠溶液,消耗4.6g二甲醚后总共可在电解池两极收集到13.44L(标况)气体,该套装置的能量利用率为___________ 。(保留3位有效数字)
l.二甲醚的生产:
二甲醚的生产原理之一是利用甲醇脱水成二甲醚,化学方程式如下:
反应i 2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H1
CH3OCH3(g)+H2O(g) △H1(1)已知:甲醇、二甲醚的气态标准燃烧热分别为-761.5kJ·mol-1、-1455.2kJ·mol-1,且H2O(g)=H2O(1) △H=-44.0kJ·mol-1。
反应i的△H1=
(2)反应i中甲醇转化率、二甲醚选择性的百分率与不同催化剂的关系如图1所示,生产时,选择的最佳催化剂是

(3)选定催化剂后,测得平衡时的甲醇转化率与温度的关系如图2所示。经研究产物的典型色谱图发现该过程主要存在的副反应为:
反应ii 2CH3OH(g)
 C2H4(g)+2H2O(g) △H2=-29.1kJ·mol-1
C2H4(g)+2H2O(g) △H2=-29.1kJ·mol-1①工业上生产二甲醚的温度通常在270-300℃,高于330℃之后,甲醇转化率下降,根据化学平衡移动原理分析原因是
②某温度下,以CH3OH(g)为原料,平衡时各物质的分压数据如下表:

则反应i中,CH3OH(g)的平衡转化率α=
Ⅱ.二甲醚的应用:
(4)图3为绿色电源“直接二甲醚燃料电池”的工作原理示意图:

①该电池的负极反应式为:
②若串联该燃料电池电解硫酸钠溶液,消耗4.6g二甲醚后总共可在电解池两极收集到13.44L(标况)气体,该套装置的能量利用率为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】目前,“低碳经济”备受关注, 的产生及有效开发利用成为科学家研究的重要课题.
的产生及有效开发利用成为科学家研究的重要课题.
(1)向浓 溶液中通入
溶液中通入 和
和 ,可以制得纳米级碳酸钙(粒子直径在
,可以制得纳米级碳酸钙(粒子直径在 之间)①向浓
之间)①向浓 溶液中通入
溶液中通入 和
和 气体制纳米级碳酸钙时,应先通入
气体制纳米级碳酸钙时,应先通入 ,后通 入
,后通 入 。制备纳米级碳酸钙的离子方程式为
。制备纳米级碳酸钙的离子方程式为______ ②判断产品中是否含有纳米级碳酸钙的实验方法为______ .
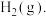 定条件下,
定条件下,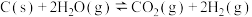 和
和 反应,能生成
反应,能生成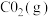 和
和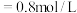 将
将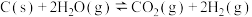 和
和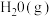 分别 加入甲、乙两个密闭容器中,发生反应:
分别 加入甲、乙两个密闭容器中,发生反应: ,其相关数 据如下表所示:
,其相关数 据如下表所示:
① 时,该反应的平衡常数
时,该反应的平衡常数
______
②乙容器中,当反应进行到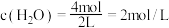 时,
时, 的物质的量浓度
的物质的量浓度______  填选项字母
填选项字母 .
.
A.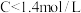
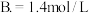
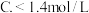
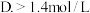
③丙容器的容积为1L, 时,起始充入a mol
时,起始充入a mol  和b mol
和b mol  ,反应达到平衡时,测得
,反应达到平衡时,测得 的转化率大于
的转化率大于 的转化率,则
的转化率,则 的值需满足的条件为
的值需满足的条件为______ ;
④丁容器的容积为1L, 时,按下列配比充入
时,按下列配比充入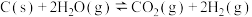 、
、 、
、 和
和 ,达到平衡时各气体的体积分数与甲容器完全相同的是
,达到平衡时各气体的体积分数与甲容器完全相同的是______  填选项字母
填选项字母 .
.
A. 、
、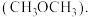 、
、 、
、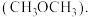
B. 、
、 、O mol、O mol
、O mol、O mol
C.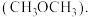 、
、 、
、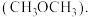 、
、
D. 、
、 、
、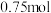 、
、
 在一定条件下可转化为甲醚
在一定条件下可转化为甲醚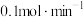 用甲醚燃料电池做电源,用惰性电极电 解饱和
用甲醚燃料电池做电源,用惰性电极电 解饱和 溶液可制取
溶液可制取 和KOH,实验装置如图所示
和KOH,实验装置如图所示
①甲醚燃料电池的负极反应式为______
② 口导出的物质为
口导出的物质为______  填化学式
填化学式 .
.
③若燃料电池通入 的速率为
的速率为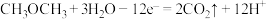 ,2min时,理论上C口收集 到标准状况下气体的体积为
,2min时,理论上C口收集 到标准状况下气体的体积为______ .
 的产生及有效开发利用成为科学家研究的重要课题.
的产生及有效开发利用成为科学家研究的重要课题.(1)向浓
 溶液中通入
溶液中通入 和
和 ,可以制得纳米级碳酸钙(粒子直径在
,可以制得纳米级碳酸钙(粒子直径在 之间)①向浓
之间)①向浓 溶液中通入
溶液中通入 和
和 气体制纳米级碳酸钙时,应先通入
气体制纳米级碳酸钙时,应先通入 ,后通 入
,后通 入 。制备纳米级碳酸钙的离子方程式为
。制备纳米级碳酸钙的离子方程式为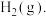 定条件下,
定条件下,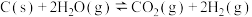 和
和 反应,能生成
反应,能生成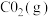 和
和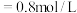 将
将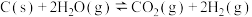 和
和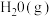 分别 加入甲、乙两个密闭容器中,发生反应:
分别 加入甲、乙两个密闭容器中,发生反应: ,其相关数 据如下表所示:
,其相关数 据如下表所示:| 容器 | 容积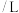 | 温度 | 起始量 | 平衡量 | 达到平衡所需时间 | |
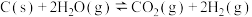 |  |  | ||||
| 甲 | 2 |  | 2 | 4 |  | 8 |
| 乙 | 1 |  | 1 | 2 |  | 3 |
 时,该反应的平衡常数
时,该反应的平衡常数
②乙容器中,当反应进行到
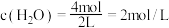 时,
时, 的物质的量浓度
的物质的量浓度 填选项字母
填选项字母 .
.A.
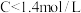
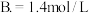
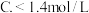
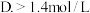
③丙容器的容积为1L,
 时,起始充入a mol
时,起始充入a mol  和b mol
和b mol  ,反应达到平衡时,测得
,反应达到平衡时,测得 的转化率大于
的转化率大于 的转化率,则
的转化率,则 的值需满足的条件为
的值需满足的条件为④丁容器的容积为1L,
 时,按下列配比充入
时,按下列配比充入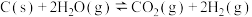 、
、 、
、 和
和 ,达到平衡时各气体的体积分数与甲容器完全相同的是
,达到平衡时各气体的体积分数与甲容器完全相同的是 填选项字母
填选项字母 .
.A.
 、
、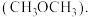 、
、 、
、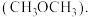
B.
 、
、 、O mol、O mol
、O mol、O molC.
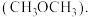 、
、 、
、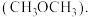 、
、
D.
 、
、 、
、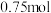 、
、
 在一定条件下可转化为甲醚
在一定条件下可转化为甲醚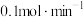 用甲醚燃料电池做电源,用惰性电极电 解饱和
用甲醚燃料电池做电源,用惰性电极电 解饱和 溶液可制取
溶液可制取 和KOH,实验装置如图所示
和KOH,实验装置如图所示
①甲醚燃料电池的负极反应式为
②
 口导出的物质为
口导出的物质为 填化学式
填化学式 .
.③若燃料电池通入
 的速率为
的速率为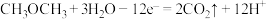 ,2min时,理论上C口收集 到标准状况下气体的体积为
,2min时,理论上C口收集 到标准状况下气体的体积为
您最近一年使用:0次



