下列离子方程式中,不 正确的是
A.向NaHCO3溶液中加入过量的NaOH溶液: +OH-= +OH-= +H2O +H2O |
| B.稀硫酸中加入铁粉:2Fe+6H+=2Fe3++3H2↑ |
| C.FeBr2溶液中通入过量的Cl2:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
D.向Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++ =3Fe3++NO↑+2H2O =3Fe3++NO↑+2H2O |
更新时间:2022-09-14 17:34:49
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】能正确表示下列化学反应的离子方程式的是
| A.锌与稀硫酸反应:Zn+2H+=Zn2++H2↑ |
| B.澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O |
| C.氨水与醋酸溶液反应:H++OH-=H2O |
D.碳酸钙溶于足量稀盐酸中: +2H+=H2O+CO2↑ +2H+=H2O+CO2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列反应的离子方程式书写不正确的是
A.碳酸钠溶液与足量盐酸反应:CO +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
| B.钠与水反应:2Na+2H2O=2Na++2OH-+H2↑ |
C.氯化钡溶液与稀硫酸反应:Ba2++SO =BaSO4↓ =BaSO4↓ |
| D.铜与氯化铁溶液反应:Cu+Fe3+=Cu2++Fe2+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列各反应对应的离子方程式正确的是
A.向Ca(OH)2溶液中加入过量的NaHCO3溶液:Ca2++2OH-+2HCO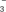 ===CaCO3↓+CO ===CaCO3↓+CO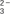 +2H2O +2H2O |
B.向含0.1 mol NaOH和0.1 mol Na2CO3的溶液中加入1 L 0.2 mol·L-1稀盐酸:OH-+CO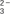 +3H+===CO2↑+2H2O +3H+===CO2↑+2H2O |
C.硫酸氢钠与氢氧化钡两种溶液反应后pH恰好为7:H++SO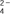 +Ba2++OH-===BaSO4↓+H2O +Ba2++OH-===BaSO4↓+H2O |
D.向100 mL 0.12 mol·L-1的Ba(OH)2溶液中通入0.02 mol CO2:Ba2++3OH-+2CO2===HCO +BaCO3↓+H2O +BaCO3↓+H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列离子方程式书写错误的是
A. 溶液中通入过量 溶液中通入过量 |
B.碳酸氢钠溶液中加入足量氢氧化钠溶液: |
C.用氯酸钠的酸性溶液与 作用制取 作用制取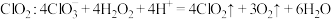 |
D.用稀硝酸洗涤做过银镜反应的试管: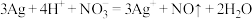 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列反应的离子方程式正确的是
| A.Fe与稀H2SO4反应:2Fe + 6H+ = 2Fe3+ + 3H2↑ |
| B.硫酸铜溶液与氢氧化钡溶液反应 :Ba2++ SO42― = BaSO4↓ |
| C.氧化铜溶于硫酸:O2―+2H+= H2O |
| D.NaCl溶液与AgNO3溶液反应:Ag++Cl―= AgCl↓ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室模拟工业处理含铬废水,操作及现象如图甲所示,反应过程中铬元素的化合价变化如图乙。已知:深蓝色溶液中生成了CrO5。

下列说法正确的是

下列说法正确的是
A.0~5 s过程中, 发生了氧化还原反应 发生了氧化还原反应 |
B.实验开始至30 s,溶液中发生的总反应离子方程式为 +3H2O2+H2O=2Cr3++3O2↑+8OH- +3H2O2+H2O=2Cr3++3O2↑+8OH- |
| C.30~80 s过程中,Cr元素被氧化,可能是溶解的氧气和剩余的H2O2所致 |
D.80 s时,溶液中含铬微粒主要为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】高铁酸钾(K2FeO4)是一种集氧化、杀菌、脱色、除臭的新型高效水处理剂,工业上可通过 Fe(NO3)3与NaClO在强碱性介质中反应生成紫红色高铁酸盐溶液,其对应的工业流程如图所示。有关说法正确的是
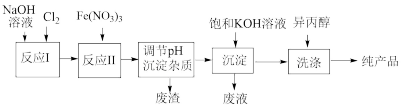

| A.K2FeO4能够作为净水剂的原因,在于其氧化产物能够水解生成氢氧化铁胶体 |
B.反应II的离子方程式为 3ClO−+5H2O+2Fe3+=2 +3Cl−+10H+ +3Cl−+10H+ |
| C.向Na2FeO4中加入饱和KOH 溶液,析出K2FeO4沉淀,说明K2FeO4的溶解度比Na2FeO4大 |
| D.洗涤粗品时选用异丙醇而不用水,可以减少K2FeO4的溶解损失 |
您最近一年使用:0次

 溶液加入
溶液加入 溶液中,离子方程式正确的是
溶液中,离子方程式正确的是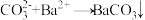
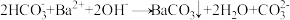
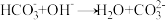
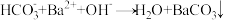
 通入
通入 溶液时,
溶液时,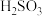 ,
,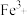 形成配合物后,通过配合物中“
形成配合物后,通过配合物中“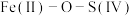 ”氧桥将
”氧桥将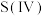 的电子传递给
的电子传递给 发生“配位体对金属的荷移”,其反应机理图示如下:
发生“配位体对金属的荷移”,其反应机理图示如下: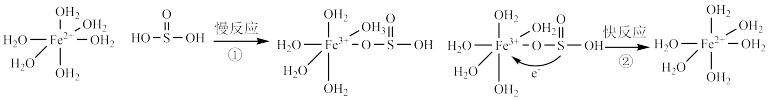

 的配位反应决定图中总反应的速率
的配位反应决定图中总反应的速率 中含有
中含有 键
键

