氮、硫的氧化物都会引起环境问题,越来越引起人们的重视。如图是氮、硫元素的各种价态与物质类别的对应关系:

(1)根据A对应的化合价和物质类别,A为_______ (写分子式),从氮元素的化合价能否发生变化的角度判断,图中既有氧化性又有还原性的含氮化合物有_______ 。
(2)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择_______ 。
(3)工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,试写出其化学方程式:_______ 。
(4)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。常用的方法是先用热空气吹出Br2,再用SO2水溶液吸收Br2.取吸收后的溶液,向其中加入氯化钡溶液有白色沉淀析出。写出SO2水溶液吸收Br2反应的化学方程式:_______ 。

(1)根据A对应的化合价和物质类别,A为
(2)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择
(3)工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,试写出其化学方程式:
(4)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。常用的方法是先用热空气吹出Br2,再用SO2水溶液吸收Br2.取吸收后的溶液,向其中加入氯化钡溶液有白色沉淀析出。写出SO2水溶液吸收Br2反应的化学方程式:
更新时间:2022-09-25 22:29:02
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】黄铁矿石的主要成分为FeS2和少量FeS(假设其它杂质中不含铁、硫元素,且高温下不发生化学变化),它是我国大多数硫酸厂制取硫酸的主要原料。某化学兴趣小组对该黄铁矿石进行如下实验探究。将m1g该黄铁矿石的样品放入如图装置(夹持和加热装置略)的石英管中,从a处不断地缓缓通入空气,高温灼烧黄铁矿样品至反应完全。其反应的化学方程式为4FeS2+11O2=2Fe2O3+8SO2,4FeS+7O2=2Fe2O3+4SO2

【实验一】测定硫元素的含量
反应结束后,将乙瓶中的溶液进行如下处理:
(1)鼓入空气的作用是_____________________ 。
(2)反应结束后,给乙瓶溶液中加入足量H2O2溶液的目的是___________ (用化学方 程式表示)。H2O2可以看成是一种很弱的酸,写出其主要的电离方程式为____________________ 。
(3)该黄铁砂石中硫元素的质量分数为____________________ (列出 表达式即可)。
【实验二】测定铁元素的含量
①用足量稀硫酸溶解石英管中的固体残渣②加还原剂使溶液中的Fe3+恰好完全转化为Fe2+后,过滤、洗涤 ③将过滤液稀释至250mL
④取25.00 mL稀释液,用0.100 mol·L-1的酸性KMnO4溶液滴定
(4)步骤②中,若用铁粉作还原剂,则所测得的铁元素的含量__________ (填“偏大”“ 偏小” 或“无影响”)。
(5)请写出步骤②中洗涤的方法____________________ 。
(6)某同学一共进行了四次滴定实验,实验结果记录如下:
根据所给数据,计算该稀释液中Fe2+的物质的量浓度c(Fe2+)=__________ 。

【实验一】测定硫元素的含量
反应结束后,将乙瓶中的溶液进行如下处理:
(1)鼓入空气的作用是
(2)反应结束后,给乙瓶溶液中加入足量H2O2溶液的目的是
(3)该黄铁砂石中硫元素的质量分数为
【实验二】测定铁元素的含量
①用足量稀硫酸溶解石英管中的固体残渣②加还原剂使溶液中的Fe3+恰好完全转化为Fe2+后,过滤、洗涤 ③将过滤液稀释至250mL
④取25.00 mL稀释液,用0.100 mol·L-1的酸性KMnO4溶液滴定
(4)步骤②中,若用铁粉作还原剂,则所测得的铁元素的含量
(5)请写出步骤②中洗涤的方法
(6)某同学一共进行了四次滴定实验,实验结果记录如下:
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 消耗KMnO4溶液体积/ml | 25.00 | 25.03 | 20.00 | 24.97 |
根据所给数据,计算该稀释液中Fe2+的物质的量浓度c(Fe2+)=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。实验室可通过以下反应制得:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O,回答下列问题:
(1)该反应中还原产物的化学式是______ ,被氧化的元素是______ (填元素符号)。
(2)用双线桥标出上述反应的电子转移情况______ 。
(3)若反应共产生了8.96L(标准状况)气体,则反应转移的电子的物质的量为______ mol,消耗还原剂的物质的量为______ mol。
(4)标准状况下44.8mL的ClO2恰好能与50mL0.1mol•L-1的Na2SO3溶液完全反应,得到的产物之一为Na2SO4,氯元素在产物中的化合价为______ ,此过程说明ClO2具有______ (填“氧化”或“还原”)性。
(5)在硫化钠溶液中通入ClO2可发生如下反应,请完成配平:______ 。
ClO2+ S2- H2O= Cl-+ SO H+
H+
(1)该反应中还原产物的化学式是
(2)用双线桥标出上述反应的电子转移情况
(3)若反应共产生了8.96L(标准状况)气体,则反应转移的电子的物质的量为
(4)标准状况下44.8mL的ClO2恰好能与50mL0.1mol•L-1的Na2SO3溶液完全反应,得到的产物之一为Na2SO4,氯元素在产物中的化合价为
(5)在硫化钠溶液中通入ClO2可发生如下反应,请完成配平:
ClO2+ S2- H2O= Cl-+ SO
 H+
H+
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下图是甲、乙两位同学探究铜与稀硝酸反应还原产物的实验装置图,请回答下列问题:
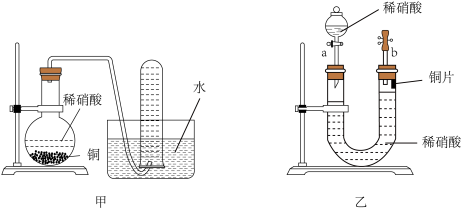
(1)写出铜和稀硝酸反应的离子方程式:___________ 。
(2)实验装置甲能否证明铜和稀硝酸反应的产物是NO气体___________ (填“能”或“不能”),请简述理由(用文字和化学方程式表示):___________
(3)若用实验装置乙进行实验,该装置的优点是___________ 。

(1)写出铜和稀硝酸反应的离子方程式:
(2)实验装置甲能否证明铜和稀硝酸反应的产物是NO气体
(3)若用实验装置乙进行实验,该装置的优点是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有下列八种物质:①Fe;②Ba(HCO3)2;③CaO;④CO2;⑤NaHSO4;⑥熔融KNO3⑦氢氧化铁胶体;⑧稀硝酸。
(1)其中能导电的是___ (填序号);属于非电解质的是___ (填序号)。
(2)⑤在熔融状态下的电离方程式为___ 。
(3)向盛有一定量②溶液的试管中逐滴加入一定量的⑤溶液至恰好沉淀完全,此时对应的离子方程式为___ ;之后继续向试管中加入⑤溶液,现象为___ ,对应的离子方程式为___ 。
(4)①与⑧发生反应的化学方程式为3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,HNO3在此反应中表现的性质是___ 。
(1)其中能导电的是
(2)⑤在熔融状态下的电离方程式为
(3)向盛有一定量②溶液的试管中逐滴加入一定量的⑤溶液至恰好沉淀完全,此时对应的离子方程式为
(4)①与⑧发生反应的化学方程式为3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,HNO3在此反应中表现的性质是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】海洋是一个巨大的化学资源宝库,从海水中可制取氯、溴、碘及其化工产品。
(1)氯的原子结构示意图是___ 。
(2)碘在元素周期表中的位置是___ 。
(3)向浓缩的海水中通入Cl2,可将Br﹣转化为Br2.该反应的离子方程式是___ 。
(4)用热空气将上述过程中产生的Br2吹出,并用浓Na2CO3溶液吸收,生成NaBr、NaBrO3等;再将混合溶液用稀硫酸酸化得到Br2,得到Br2的离子方程式是___ 。
(1)氯的原子结构示意图是
(2)碘在元素周期表中的位置是
(3)向浓缩的海水中通入Cl2,可将Br﹣转化为Br2.该反应的离子方程式是
(4)用热空气将上述过程中产生的Br2吹出,并用浓Na2CO3溶液吸收,生成NaBr、NaBrO3等;再将混合溶液用稀硫酸酸化得到Br2,得到Br2的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
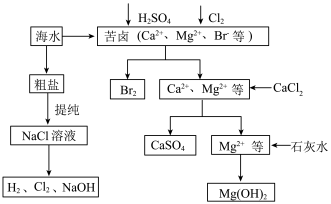
【推荐2】工业上对海水资源综合开发利用的部分工艺流程如下图所示。
(1)电解饱和食盐水常用离子膜电解槽和隔膜电解槽,离子膜和隔膜均允许通过的分子或离子是_______ 。电解槽中的阳极材料为_________________ 。
(2)本工艺流程中先后制得Br2、CaSO4和Mg(OH)2,能否按Br2、Mg(OH)2、CaSO4的顺序制备_______ ?原因是____________________________ 。
(3)膜在四氧化碳中的溶解度比在水中大得多,四氧化碳与水不互溶,故可用于萃取溴,但在上述工艺中却不用四氧化碳,原因是______________________________________ 。
(1)电解饱和食盐水常用离子膜电解槽和隔膜电解槽,离子膜和隔膜均允许通过的分子或离子是
(2)本工艺流程中先后制得Br2、CaSO4和Mg(OH)2,能否按Br2、Mg(OH)2、CaSO4的顺序制备
(3)膜在四氧化碳中的溶解度比在水中大得多,四氧化碳与水不互溶,故可用于萃取溴,但在上述工艺中却不用四氧化碳,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:

(1)除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序正确的是__________ 。
A.NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
B.BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸
C.NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤后加盐酸
D.Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
(2)制备钠单质的方法之一是将熔融NaCl进行电解,写出电解化学方程式:
___________________________________________________________ 。
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是______________ 。写出步骤Ⅱ中发生反应的化学方程式:___________________ 。
(4)某化学小组的同学为了了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59 ℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如下实验装置:

①图中仪器B的名称是________ ,冷却水的出口为____ (填“甲”或“乙”)。
②C中液体的颜色为__________________ 。
③D装置的作用是__________________ 。

(1)除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序正确的是
A.NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
B.BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸
C.NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤后加盐酸
D.Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
(2)制备钠单质的方法之一是将熔融NaCl进行电解,写出电解化学方程式:
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是
(4)某化学小组的同学为了了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59 ℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如下实验装置:

①图中仪器B的名称是
②C中液体的颜色为
③D装置的作用是
您最近一年使用:0次





