完成下列问题。
(1)如图NO2(g)和CO(g)反应生成CO2(g)和NO(g)过程中能量变化图。该反应是_______ (填“放热”或“吸热”)反应,该反应物的总焓_______ 生成物的焓(填“小于”或“大于”)。请写出NO2和CO反应的热化学方程式_______ ;
(2)有如下三个热化学方程式:
H2(g)+ O2(g)═H2O(g) △H1=akJ•mol﹣1
O2(g)═H2O(g) △H1=akJ•mol﹣1
H2(g)+ O2(g)═H2O(l) △H2=bkJ•mol﹣1
O2(g)═H2O(l) △H2=bkJ•mol﹣1
2H2O(l)═2H2(g)+O2(g) △H3=ckJ•mol﹣1
①请写出b、c的关系式_______ ;判断c_______ 0(填“>”或“<”)。
②试比较△H1_______ △H2(填“>”或“<”)。
③相同条件下,1molH2O(g)比1molH2O(l)更_______ (填“稳定”或“不稳定”)
(1)如图NO2(g)和CO(g)反应生成CO2(g)和NO(g)过程中能量变化图。该反应是

(2)有如下三个热化学方程式:
H2(g)+
 O2(g)═H2O(g) △H1=akJ•mol﹣1
O2(g)═H2O(g) △H1=akJ•mol﹣1H2(g)+
 O2(g)═H2O(l) △H2=bkJ•mol﹣1
O2(g)═H2O(l) △H2=bkJ•mol﹣12H2O(l)═2H2(g)+O2(g) △H3=ckJ•mol﹣1
①请写出b、c的关系式
②试比较△H1
③相同条件下,1molH2O(g)比1molH2O(l)更
更新时间:2022-09-23 21:13:19
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
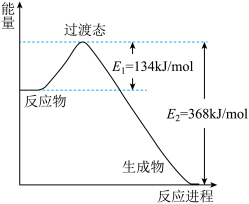
【推荐1】煤和石油通常都含有硫的化合物,燃烧生成的二氧化硫为大气主要污染物之一,二氧化硫的治理已成为当前研究的课题。硫与硫的氧化物在转化过程中的能量变化如图所示。

已知: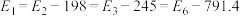
回答下列问题:
(1)图中的Ⅰ、Ⅱ、Ⅲ、Ⅳ中属于放热反应的是_______ 。
(2)写出表示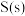 的燃烧热的热化学方程式:
的燃烧热的热化学方程式:_______ 。
(3)从图中可看出将 氧化成
氧化成 有两条途径:①
有两条途径:① 经过程Ⅲ、过程Ⅳ转化成
经过程Ⅲ、过程Ⅳ转化成 ;②
;② 经过程Ⅱ转化成
经过程Ⅱ转化成 。这两种途径相比,①改变的条件是
。这两种途径相比,①改变的条件是_______ ,改变该条件主要是降低了_______ 。已知过程Ⅳ的化学方程式为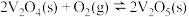 ,则过程Ⅲ的热化学方程式为
,则过程Ⅲ的热化学方程式为_______ 。
(4) 和
和 在一定条件下连续发生过程Ⅰ和过程Ⅱ的反应,充分反应后无固体剩余,测得放出的热量为
在一定条件下连续发生过程Ⅰ和过程Ⅱ的反应,充分反应后无固体剩余,测得放出的热量为 。则反应后的体系中各组分的物质的量分别为
。则反应后的体系中各组分的物质的量分别为_______ (保留两位有效数字)。

已知:
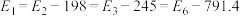
回答下列问题:
(1)图中的Ⅰ、Ⅱ、Ⅲ、Ⅳ中属于放热反应的是
(2)写出表示
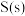 的燃烧热的热化学方程式:
的燃烧热的热化学方程式:(3)从图中可看出将
 氧化成
氧化成 有两条途径:①
有两条途径:① 经过程Ⅲ、过程Ⅳ转化成
经过程Ⅲ、过程Ⅳ转化成 ;②
;② 经过程Ⅱ转化成
经过程Ⅱ转化成 。这两种途径相比,①改变的条件是
。这两种途径相比,①改变的条件是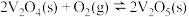 ,则过程Ⅲ的热化学方程式为
,则过程Ⅲ的热化学方程式为(4)
 和
和 在一定条件下连续发生过程Ⅰ和过程Ⅱ的反应,充分反应后无固体剩余,测得放出的热量为
在一定条件下连续发生过程Ⅰ和过程Ⅱ的反应,充分反应后无固体剩余,测得放出的热量为 。则反应后的体系中各组分的物质的量分别为
。则反应后的体系中各组分的物质的量分别为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氨气是重要的化工原料,工业合成氨反应原理为: ,其反应过程中能量变化如图所示。
,其反应过程中能量变化如图所示。
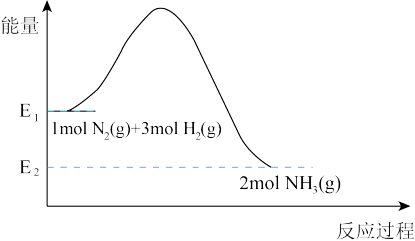
(1)工业合成氨的条件是___________ 。
(2)合成氨的反应是___________ 反应(填“吸热”或“放热”)。
(3)若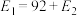 ,则每消耗
,则每消耗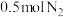 ,反应放出(或吸收)的热量
,反应放出(或吸收)的热量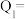
___________ kJ。
(4)将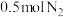 和
和 充入密闭容器中,在相同条件下发生该反应,达到平衡时,放出或吸收的热量为
充入密闭容器中,在相同条件下发生该反应,达到平衡时,放出或吸收的热量为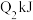 ,则
,则
___________  (填“>”“<”或“=”),理由是
(填“>”“<”或“=”),理由是___________ 。
 ,其反应过程中能量变化如图所示。
,其反应过程中能量变化如图所示。
(1)工业合成氨的条件是
(2)合成氨的反应是
(3)若
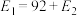 ,则每消耗
,则每消耗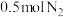 ,反应放出(或吸收)的热量
,反应放出(或吸收)的热量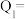
(4)将
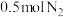 和
和 充入密闭容器中,在相同条件下发生该反应,达到平衡时,放出或吸收的热量为
充入密闭容器中,在相同条件下发生该反应,达到平衡时,放出或吸收的热量为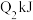 ,则
,则
 (填“>”“<”或“=”),理由是
(填“>”“<”或“=”),理由是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】白磷(P4)与氯气反应的能量变化如图所示。回答下列问题:
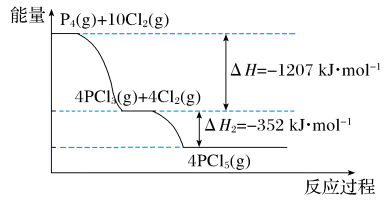
(1)白磷在氯气中燃烧的反应是放热反应,但是启动反应时需要点燃或加热,其原因是_______ 。
(2)PCl5(g)=PCl3(g)+Cl2(g) ΔH=_______ 。
(3)写出白磷蒸气在氯气中反应生成五氯化磷气体的热化学方程式:_______ 。
(4)在密闭容器中充入1 mol PCl3(g)和3 mol Cl2(g),发生反应:PCl3(g)+Cl2(g) ⇌PCl5(g),放出热量Q的范围为_______ 。
(5)白磷在氯气中燃烧,开始引燃之后,停止加热,反应持续进行至一种物质(或两种物质)完全反应,其原因是_______ 。

(1)白磷在氯气中燃烧的反应是放热反应,但是启动反应时需要点燃或加热,其原因是
(2)PCl5(g)=PCl3(g)+Cl2(g) ΔH=
(3)写出白磷蒸气在氯气中反应生成五氯化磷气体的热化学方程式:
(4)在密闭容器中充入1 mol PCl3(g)和3 mol Cl2(g),发生反应:PCl3(g)+Cl2(g) ⇌PCl5(g),放出热量Q的范围为
(5)白磷在氯气中燃烧,开始引燃之后,停止加热,反应持续进行至一种物质(或两种物质)完全反应,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氨气是一种重要的物质,可用于制取化肥和硝酸等。已知H﹣H键、N﹣H键、N≡N键的键能分别是436 kJ·mol-1、391 kJ·mol-1、946 kJ·mol-1。
(1)写出合成氨的热反应方程式:____ 。生成1 mol NH3需要吸收或放出___ kJ。
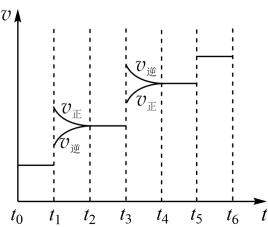
(2)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图所示。图中t1时引起平衡移动的条件可能是______ 。其中表示平衡混合物中NH3的含量最高的一段时间是______ 。
(1)写出合成氨的热反应方程式:
(2)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图所示。图中t1时引起平衡移动的条件可能是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请运用反应热的知识填写下列空白:
(1)已知: (s,白磷)=
(s,白磷)= (s,黑磷)
(s,黑磷) 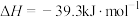 ;
;
 (s,白磷)=
(s,白磷)= (s,红磷)
(s,红磷) 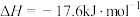 ;
;
由此推知,其中最稳定的磷单质是___________ 。
(2)①硅粉与HCl在300℃时反应生成1 mol SiHCl3气体和H2,放出225 kJ热量,该反应的热化学方程式为___________ 。
②在 25℃ 和 101kPa时,4 g硫粉在O2中完全燃烧生成SO2气体,放出37 kJ的热量,写出表示S燃烧热的热化学方程式:___________ 。
(3)已知上述反应中相关的化学键键能数据如下:
则该反应的 ΔH = ___________ 。
(4)将 氢化为
氢化为 有三种方法,对应的反应依次为:
有三种方法,对应的反应依次为:
①

②

③

反应③的 ΔH3 =___________ (用ΔH1,ΔH2表示)
(5)①2Cu2O(s) + O2(g) =4CuO(s) ΔH1=-277kJ·mol-1
②8CuO(s) + CH4(g)=4Cu2O(s) + CO2(g)+2H2O(g) ΔH2=-348kJ·mol-1
反应CH4(g) +2O2(g)=CO2(g)+2H2O(g) ΔH=___________ kJ·mol-1
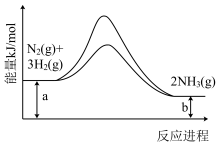
(6)合成氨反应常使用铁触媒提高反应速率。如图为有、无铁触媒时,反应的能量变化示意图。写出该反应的热化学方程式___________ 。
(1)已知:
 (s,白磷)=
(s,白磷)= (s,黑磷)
(s,黑磷) 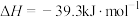 ;
; (s,白磷)=
(s,白磷)= (s,红磷)
(s,红磷) 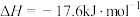 ;
;由此推知,其中最稳定的磷单质是
(2)①硅粉与HCl在300℃时反应生成1 mol SiHCl3气体和H2,放出225 kJ热量,该反应的热化学方程式为
②在 25℃ 和 101kPa时,4 g硫粉在O2中完全燃烧生成SO2气体,放出37 kJ的热量,写出表示S燃烧热的热化学方程式:
(3)已知上述反应中相关的化学键键能数据如下:
| 化学键 | C-H | C=O | H-H | C O(CO) O(CO) |
| 键能/kJ·mol−1 | 413 | 745 | 436 | 1075 |
(4)将
 氢化为
氢化为 有三种方法,对应的反应依次为:
有三种方法,对应的反应依次为:①


②


③


反应③的 ΔH3 =
(5)①2Cu2O(s) + O2(g) =4CuO(s) ΔH1=-277kJ·mol-1
②8CuO(s) + CH4(g)=4Cu2O(s) + CO2(g)+2H2O(g) ΔH2=-348kJ·mol-1
反应CH4(g) +2O2(g)=CO2(g)+2H2O(g) ΔH=
(6)合成氨反应常使用铁触媒提高反应速率。如图为有、无铁触媒时,反应的能量变化示意图。写出该反应的热化学方程式

您最近一年使用:0次



