回答下列问题:
(1)火药是中国古代“四大发明”之一。黑火药爆炸时发生如下反应:2KNO3+C+S=K2S+2NO2↑+CO2↑。其中被还原的元素是_______ ,被氧化的元素是 _______ ,氧化剂是 _______ ,还原剂是 _______ 。
(2)阅读下列材料,回答有关问题:一个体重50kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而是以Fe2+ 和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+转变成Fe2+,有利于人体吸收。
①在人体中进行Fe2+ 和Fe3+的转化时,其中的Fe2+作_______ 剂(填“氧化”或“还原”)。
②“服用维生素C,可使食物中的Fe3+转变成Fe2+”这句话指出,维生素C在这一反应中具有_______ 性。(填“氧化”或“还原”)
(1)火药是中国古代“四大发明”之一。黑火药爆炸时发生如下反应:2KNO3+C+S=K2S+2NO2↑+CO2↑。其中被还原的元素是
(2)阅读下列材料,回答有关问题:一个体重50kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而是以Fe2+ 和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+转变成Fe2+,有利于人体吸收。
①在人体中进行Fe2+ 和Fe3+的转化时,其中的Fe2+作
②“服用维生素C,可使食物中的Fe3+转变成Fe2+”这句话指出,维生素C在这一反应中具有
更新时间:2022-09-20 08:30:03
|
相似题推荐
填空题
|
容易
(0.94)
【推荐1】分类法在化学中起着非常重要的作用,现有下列物质:①Cl2、②NaOH溶液、③Cu、④冰水混合物、⑤ 、⑥稀硫酸、⑦CO2、⑧镁铝合金。请回答下列问题:
、⑥稀硫酸、⑦CO2、⑧镁铝合金。请回答下列问题:
(1)属于纯净物的有_______ ,属于氧化物的有_______ 。
(2)能导电的物质有_______ ,属于电解质的有_______ 。
(3)实验室中制取少量氢氧化铁胶体的离子方程式为_______ 。
(4)已知Cl2与NaOH反应的化学方程式是 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为_______ 。
(5)已知实验需要240mL0.5mol/L硫酸,但实验室中只有物质的量浓度为lmol/L的硫酸,该同学需要自己稀释,需要量取_______ mL1mol/L的硫酸。
 、⑥稀硫酸、⑦CO2、⑧镁铝合金。请回答下列问题:
、⑥稀硫酸、⑦CO2、⑧镁铝合金。请回答下列问题:(1)属于纯净物的有
(2)能导电的物质有
(3)实验室中制取少量氢氧化铁胶体的离子方程式为
(4)已知Cl2与NaOH反应的化学方程式是
 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为(5)已知实验需要240mL0.5mol/L硫酸,但实验室中只有物质的量浓度为lmol/L的硫酸,该同学需要自己稀释,需要量取
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】在Fe3O4 + 4CO 3Fe+4CO2的反应中,
3Fe+4CO2的反应中,___________ 是氧化剂,___________ 是还原剂, ___________ 元素被氧化,___________ 元素被还原。
 3Fe+4CO2的反应中,
3Fe+4CO2的反应中,
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐3】Ⅰ、按要求完成下列填空。
(1)漂白精主要成分的化学式:___________ 。
(2)硫酸铝在水溶液中的电离方程式:___________ 。
(3)用单线桥法 标出下列氧化还原反应电子转移的方向和数目并填空: 
___________ ,在该反应中,还原剂是___________ 。(填化学式)
II、根据所学知识,回答下列问题:
(4)标准状况下,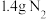 的体积是
的体积是___________ L。
(5)常温常压下,将等质量的镁带与铁片分别与足量稀硫酸反应,产生 的体积之比为
的体积之比为___________ 。
(6)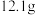 某硝酸盐
某硝酸盐 中含有
中含有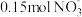 ,则该硝酸盐的摩尔质量为
,则该硝酸盐的摩尔质量为___________ 。
(1)漂白精主要成分的化学式:
(2)硫酸铝在水溶液中的电离方程式:
(3)用

II、根据所学知识,回答下列问题:
(4)标准状况下,
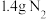 的体积是
的体积是(5)常温常压下,将等质量的镁带与铁片分别与足量稀硫酸反应,产生
 的体积之比为
的体积之比为(6)
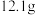 某硝酸盐
某硝酸盐 中含有
中含有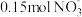 ,则该硝酸盐的摩尔质量为
,则该硝酸盐的摩尔质量为
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】硅是重要的无机非金属材料,工业上从硅的氧化物制取硅单质的主要反应为SiO2+2C=Si+2CO↑。其中,其中硅元素的化合价_______ (填“升高”或“降低”),氧化剂是_____ (填化学式),被氧化的物质是____ (填化学式);若反应中消耗了2molC,则生成_____ molSi。
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】基本概念
(1)氧化还原反应的特征:反应中物质所含元素化合价_______ 。
(2)氧化还原反应的实质
①氧化还原反应的概念
a.有_______ 的反应叫作氧化还原反应。
b.氧化反应:物质所含元素的原子_______ 的反应;
还原反应:物质所含元素的原子_______ 的反应。
如钠与氯气的反应,实质是钠原子_______ ,发生_______ 反应;氯原子_______ ,发生_______ 反应;可表示为 。
。
c.氧化剂与还原剂
氧化剂:在氧化还原反应中,所含元素的化合价_______ ,即_______ 电子的物质。
还原剂:在氧化还原反应中,所含元素的化合价_______ ,即_______ 电子的物质。
d.氧化产物与还原产物
氧化产物:还原剂失去电子被_______ 的产物。
还原产物:氧化剂得到电子被_______ 的产物。
e。氧化性与还原性
氧化性:物质_______ 电子的能力。
还原性:物质_______ 电子的性质。
②氧化还原反应概念之间的关系
化合价升高——_______ 电子——被_______ ——发生_______ 反应——是_______ 剂
化合价降低——_______ 电子——被_______ ——发生_______ 反应——是_______ 剂
(1)氧化还原反应的特征:反应中物质所含元素化合价
(2)氧化还原反应的实质
①氧化还原反应的概念
a.有
b.氧化反应:物质所含元素的原子
还原反应:物质所含元素的原子
如钠与氯气的反应,实质是钠原子
 。
。c.氧化剂与还原剂
氧化剂:在氧化还原反应中,所含元素的化合价
还原剂:在氧化还原反应中,所含元素的化合价
d.氧化产物与还原产物
氧化产物:还原剂失去电子被
还原产物:氧化剂得到电子被
e。氧化性与还原性
氧化性:物质
还原性:物质
②氧化还原反应概念之间的关系
化合价升高——
化合价降低——
您最近一年使用:0次



