回答下列问题:
(1)化合价是学习氧化还原反应的基础。写出以下几种物质中加点元素 的化合价。
H2O 2____ ,H2C 2O4____ ,C r2O
____ ,M nO
____ 。
(2)自然界中的含硫物质在一定条件下能够相互转化,这种转化在人工条件下也能发生。最近有人尝试用H2还原工业尾气中SO2,该反应分两步完成,如图所示。
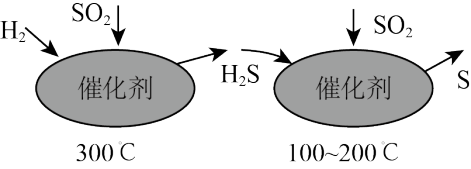
①第一步反应中被氧化的元素是____ (填元素符号)。
②写出第二步的化学方程式:____ 。
(3)将少量Cl2通入FeI2的溶液中,反应的离子方程式为2I—+Cl2=I2+2Cl—,比较还原性I—____ Fe2+(填“大于”、“小于”或“等于”)。
(4)按如图所示操作,充分反应后:
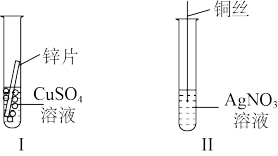
结合实验I、II反应原理推出Cu2+、Zn2+、Ag+的氧化性由弱到强的顺序为_____ 。
(1)化合价是学习氧化还原反应的基础。写出以下几种物质中
H2


(2)自然界中的含硫物质在一定条件下能够相互转化,这种转化在人工条件下也能发生。最近有人尝试用H2还原工业尾气中SO2,该反应分两步完成,如图所示。

①第一步反应中被氧化的元素是
②写出第二步的化学方程式:
(3)将少量Cl2通入FeI2的溶液中,反应的离子方程式为2I—+Cl2=I2+2Cl—,比较还原性I—
(4)按如图所示操作,充分反应后:

结合实验I、II反应原理推出Cu2+、Zn2+、Ag+的氧化性由弱到强的顺序为
更新时间:2022-09-15 22:46:43
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】“佛立苏”是一种常见补血剂,主要成分为FeSO4;FeSO4·7H2O俗称“绿矾”,在工业生产和日常生活中都有广泛的用途,回答下列问题:
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是______ (填字母)。
A.亚硝酸盐被还原B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+D.亚硝酸盐是还原剂
(2)已知Fe(OH)2是一种白色沉淀,极易被空气中的氧气氧化,反应的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3(红褐色沉淀),用双线桥法表示转移电子数和氧化还原反应______ 。
向FeSO4溶液中加入一小块金属钠,发现开始有气体和白色沉淀产生,过一段时间,白色沉淀变为红褐色,写出上述反应中涉及到的离子方程式________________________________ 。
(3)FeSO4可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾(K2FeO4),氧化性比Cl2、O2、ClO2、KMnO4更强,主要反应:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。
①上述反应中作还原剂的是______ (填化学式)。
②简要说明K2FeO4作为水处理剂时所起的作用____________ (写出一点即可)。
(4)将Na2O2固体加入酚酞溶液中产生的现象是_______ 。写出该反应的离子方程式______ 。
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是
A.亚硝酸盐被还原B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+D.亚硝酸盐是还原剂
(2)已知Fe(OH)2是一种白色沉淀,极易被空气中的氧气氧化,反应的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3(红褐色沉淀),用双线桥法表示转移电子数和氧化还原反应
向FeSO4溶液中加入一小块金属钠,发现开始有气体和白色沉淀产生,过一段时间,白色沉淀变为红褐色,写出上述反应中涉及到的离子方程式
(3)FeSO4可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾(K2FeO4),氧化性比Cl2、O2、ClO2、KMnO4更强,主要反应:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。
①上述反应中作还原剂的是
②简要说明K2FeO4作为水处理剂时所起的作用
(4)将Na2O2固体加入酚酞溶液中产生的现象是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氧化还原反应在生产、生活中具有广泛的用途。
I.过氧化氢( )中的氧的化合价为-1价,其水溶液俗称双氧水,医疗上利用它的氧化性作为杀菌消毒剂来清洗伤口,结合下列涉及
)中的氧的化合价为-1价,其水溶液俗称双氧水,医疗上利用它的氧化性作为杀菌消毒剂来清洗伤口,结合下列涉及 的反应,回答下列问题。
的反应,回答下列问题。
A.
B.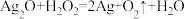
C.
D.
(1)上述反应不属于氧化还原反应的是_______ (填序号,下同)。 仅体现氧化性的反应是
仅体现氧化性的反应是_______ , 既体现氧化性又体现还原性的反应是
既体现氧化性又体现还原性的反应是_______ 。
(2)在B反应中,_______ 发生还原反应,_______ 是还原剂,_______ 是氧化产物。(用化学式表示)
(3)反应A的原料过氧化钡(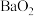 )可以由
)可以由 经过一系列反应来制备,请写出向氢氧化钡溶液中滴加硫酸氢钠溶液,至
经过一系列反应来制备,请写出向氢氧化钡溶液中滴加硫酸氢钠溶液,至 沉淀完全的离子方程式
沉淀完全的离子方程式_______ 。
II.储氢纳米碳管的研究成功体现了科技的进步,但用电弧法合成的碳纳米管常伴有大量的杂质:碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯。反应化学方程式为: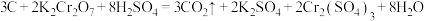
(4)用单线桥标出该反应中电子转移方向和数目_______ 。
(5) 在上述反应中表现出来的性质是_______(填选项编号)。
在上述反应中表现出来的性质是_______(填选项编号)。
(6)将反应产生的气体通入澄清石灰水中,产生白色沉淀,写出该反应的离子方程式_______ 。
I.过氧化氢(
 )中的氧的化合价为-1价,其水溶液俗称双氧水,医疗上利用它的氧化性作为杀菌消毒剂来清洗伤口,结合下列涉及
)中的氧的化合价为-1价,其水溶液俗称双氧水,医疗上利用它的氧化性作为杀菌消毒剂来清洗伤口,结合下列涉及 的反应,回答下列问题。
的反应,回答下列问题。A.

B.
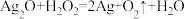
C.

D.

(1)上述反应不属于氧化还原反应的是
 仅体现氧化性的反应是
仅体现氧化性的反应是 既体现氧化性又体现还原性的反应是
既体现氧化性又体现还原性的反应是(2)在B反应中,
(3)反应A的原料过氧化钡(
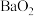 )可以由
)可以由 经过一系列反应来制备,请写出向氢氧化钡溶液中滴加硫酸氢钠溶液,至
经过一系列反应来制备,请写出向氢氧化钡溶液中滴加硫酸氢钠溶液,至 沉淀完全的离子方程式
沉淀完全的离子方程式II.储氢纳米碳管的研究成功体现了科技的进步,但用电弧法合成的碳纳米管常伴有大量的杂质:碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯。反应化学方程式为:
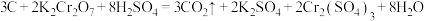
(4)用单线桥标出该反应中电子转移方向和数目
(5)
 在上述反应中表现出来的性质是_______(填选项编号)。
在上述反应中表现出来的性质是_______(填选项编号)。| A.氧化性 | B.氧化性和酸性 | C.还原性和酸性 | D.酸性 |
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)根据反应8NH3+3Cl2=6NH4Cl+N2
①氧化剂是___________ 还原剂是___________ 氧化产物是___________
②氧化剂与还原剂的质量之比为___________ 。
③当生成28gN2时被氧化的物质为___________ g。
(2)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
①该反应中氧化剂是___________ (用化学式表示,下同),___________ 元素被氧化,还原产物为___________ 。
②用双线桥在方程式中标出电子转移的情况:___________
(3)化合价是学习氧化还原反应的基础。写出以下几种物质中加点元素的化合价。
H2C 2O4___________ N H4NO3___________
(1)根据反应8NH3+3Cl2=6NH4Cl+N2
①氧化剂是
②氧化剂与还原剂的质量之比为
③当生成28gN2时被氧化的物质为
(2)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
①该反应中氧化剂是
②用双线桥在方程式中标出电子转移的情况:
(3)化合价是学习氧化还原反应的基础。写出以下几种物质中加点元素的化合价。
H2
您最近半年使用:0次
【推荐1】Ⅰ.实验室可用 和浓盐酸反应制取氯气,反应原理如下:
和浓盐酸反应制取氯气,反应原理如下: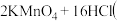 浓
浓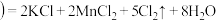
(1)用双线桥标出电子得失情况。_______
(2)由此反应可以推断氧化性强弱
_______ 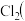 填“
填“ ”、“
”、“ ”、“
”、“ ”
”
(3)浓盐酸在反应中显示出来的性质是_______
(4)若参加反应的HCl是73g,则被氧化的HCl有_______  保留一位小数点
保留一位小数点 。
。
Ⅱ.某同学设计如下实验研究 的性质:
的性质:
(5)从理论上看 既有氧化性又有还原性,具有氧化性的原因是
既有氧化性又有还原性,具有氧化性的原因是_______ 。
(6)以上证明 具有还原性的实验中,可作为证据的实验现象是
具有还原性的实验中,可作为证据的实验现象是_______  填字母序号
填字母序号 。
。
Ⅲ.
(7)先将下述反应配平,再用单线桥标出该反应中电子转移的方向和数目_______ 。
_______
 和浓盐酸反应制取氯气,反应原理如下:
和浓盐酸反应制取氯气,反应原理如下: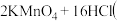 浓
浓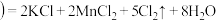
(1)用双线桥标出电子得失情况。
(2)由此反应可以推断氧化性强弱

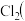 填“
填“ ”、“
”、“ ”、“
”、“ ”
”
(3)浓盐酸在反应中显示出来的性质是
(4)若参加反应的HCl是73g,则被氧化的HCl有
 保留一位小数点
保留一位小数点 。
。Ⅱ.某同学设计如下实验研究
 的性质:
的性质:| 序号 | 实验 | 实验现象 |
 | 向 溶液中滴加酸性 溶液中滴加酸性 溶液 溶液 |  溶液紫色褪去 溶液紫色褪去 有大量气泡产生 有大量气泡产生 |
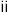 | 向 溶液中滴加淀粉碘化钾溶液 溶液中滴加淀粉碘化钾溶液 |  溶液变蓝 溶液变蓝 |
 既有氧化性又有还原性,具有氧化性的原因是
既有氧化性又有还原性,具有氧化性的原因是(6)以上证明
 具有还原性的实验中,可作为证据的实验现象是
具有还原性的实验中,可作为证据的实验现象是 填字母序号
填字母序号 。
。Ⅲ.
(7)先将下述反应配平,再用单线桥标出该反应中电子转移的方向和数目
_______

您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请用氧化还原反应相关知识回答下列问题:
某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X.
①已知KBrO3在反应中得到电子,则该反应的还原剂是_____ .
②KBrO3在反应中生成单质 X,则X的化学式为_____ .
③根据上述反应可推知_____ .
a.氧化性:KBrO3>H3AsO4 b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>X d.还原性:X>AsH3
某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X.
①已知KBrO3在反应中得到电子,则该反应的还原剂是
②KBrO3在反应中生成单质 X,则X的化学式为
③根据上述反应可推知
a.氧化性:KBrO3>H3AsO4 b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>X d.还原性:X>AsH3
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】I.某反应为:3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O,
(1)用单线桥表示出该反应中电子转移的方向和数目:______________________ 。
(2)该反应中氧化剂的化学式是__________ , 被氧化的元素是________ 。(填元素符号)。
II.有下列三个反应:
a.2FaC13 + 2KI =2FeCl2 + 2KCl + I2
b.2FeCl2+Cl2=2FeCl3
c.2KMnO4+ 16HCl(浓)=2KCl + 2MnCl2+ 5Cl2↑+ 8H2O
(1)上述三个反应中氧化剂氧化性强弱关系为_____________________ ;
(2)在反应c中,若被氧化的HCl为1. 5mol,则转移的电子数是___________________ 个。
(1)用单线桥表示出该反应中电子转移的方向和数目:
(2)该反应中氧化剂的化学式是
II.有下列三个反应:
a.2FaC13 + 2KI =2FeCl2 + 2KCl + I2
b.2FeCl2+Cl2=2FeCl3
c.2KMnO4+ 16HCl(浓)=2KCl + 2MnCl2+ 5Cl2↑+ 8H2O
(1)上述三个反应中氧化剂氧化性强弱关系为
(2)在反应c中,若被氧化的HCl为1. 5mol,则转移的电子数是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氨氮废水中的氮元素多以 、
、 的形式存在,是造成河流和湖泊富营养化的主要因素,科学家找到多种处理氨氮废水的方法。
的形式存在,是造成河流和湖泊富营养化的主要因素,科学家找到多种处理氨氮废水的方法。
(1)某研究团队设计的处理流程如下:

①过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30℃,通入空气将氨赶出并回收。
请用离子方程式表示加NaOH溶液时所发生的反应:_______ 。
②过程Ⅱ:在微生物的作用下实现 转化,称为硝化过程。在碱性条件下,
转化,称为硝化过程。在碱性条件下, 被氧气氧化成
被氧气氧化成 的总反应的离子方程式为
的总反应的离子方程式为_______ 。
③过程Ⅲ:在一定条件下向废水中加入甲醇( ),实现
),实现 转化,称为反硝化过程。
转化,称为反硝化过程。 中碳元素的化合价为
中碳元素的化合价为_______ ,当甲醇与6mol  完全反应,转化成
完全反应,转化成 时,消耗的甲醇的质量为
时,消耗的甲醇的质量为_______ 。
(2)折点氯化法是将氯气通入氨氮废水中达到某一点,在该点时水中游离氯含量最低,而氨氮的浓度降为零,该点称为折点,该状态下的氯化称为折点氯化。当氯气与氨氮的物质的量之比至少为_______ 时即“折点”。
 、
、 的形式存在,是造成河流和湖泊富营养化的主要因素,科学家找到多种处理氨氮废水的方法。
的形式存在,是造成河流和湖泊富营养化的主要因素,科学家找到多种处理氨氮废水的方法。(1)某研究团队设计的处理流程如下:

①过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30℃,通入空气将氨赶出并回收。
请用离子方程式表示加NaOH溶液时所发生的反应:
②过程Ⅱ:在微生物的作用下实现
 转化,称为硝化过程。在碱性条件下,
转化,称为硝化过程。在碱性条件下, 被氧气氧化成
被氧气氧化成 的总反应的离子方程式为
的总反应的离子方程式为③过程Ⅲ:在一定条件下向废水中加入甲醇(
 ),实现
),实现 转化,称为反硝化过程。
转化,称为反硝化过程。 中碳元素的化合价为
中碳元素的化合价为 完全反应,转化成
完全反应,转化成 时,消耗的甲醇的质量为
时,消耗的甲醇的质量为(2)折点氯化法是将氯气通入氨氮废水中达到某一点,在该点时水中游离氯含量最低,而氨氮的浓度降为零,该点称为折点,该状态下的氯化称为折点氯化。当氯气与氨氮的物质的量之比至少为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氧化还原反应原理在研究物质性质及物质转化方面具有重要的价值。
(1)化合价是学习氧化还原反应的基础。在括号中写出以下几种物质中加点元素 的化合价。
NaH _____ ,N H4NO3_____ ,H2C 2O4_____ ,Cu Cl _____ 。
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3→N2O3+H2 O;②NH3+NO→HNO2+H2O;③N2O4+H2O→HNO3+HNO2
根据氧化还原反应的原理,你认为不可能实现的是_____ (填序号)。
(3)配平下列离子方程式:_______________ 。
____H2C2O4+____ +_____H +=____ Mn2++______CO2↑+_____H2O
+_____H +=____ Mn2++______CO2↑+_____H2O
(4)氢化钠(NaH)为白色晶体,能与水剧烈反应:NaH+H2O=NaOH+H2↑,该反应中还原剂为_____ ,NaH 与液氨(NH3)也有类似反应,写出该反应的化学方程式:_________ 。
(1)化合价是学习氧化还原反应的基础。在括号中写出以下几种物质中
Na
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3→N2O3+H2 O;②NH3+NO→HNO2+H2O;③N2O4+H2O→HNO3+HNO2
根据氧化还原反应的原理,你认为不可能实现的是
(3)配平下列离子方程式:
____H2C2O4+____
 +_____H +=____ Mn2++______CO2↑+_____H2O
+_____H +=____ Mn2++______CO2↑+_____H2O(4)氢化钠(NaH)为白色晶体,能与水剧烈反应:NaH+H2O=NaOH+H2↑,该反应中还原剂为
您最近半年使用:0次
【推荐3】 K2FeO4是常见的水处理剂,其原理如图所示。请回答下列问题:
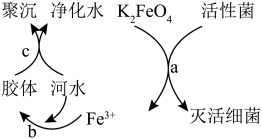
(1)高铁酸钾(K2FeO4)中铁元素的化合价为________ .
(2)过程a中K2FeO4体现________ (填“氧化”或“还原”)性,氧化产物是________ 。
(3)过程b反应的离子方程式为________ ,过程c属于________ (填“物理”或“化学”)变化。
(4)碱性条件下用Fe(OH)3和KClO反应制备K2FeO4。配平其反应的化学方程式:________ 。
Fe(OH)3+_______KOH+_______KClO=_______ K2FeO4+_______KCl+_______H2O
(5)根据以上K2FeO4净水原理,相比于Cl2,其优点是________ 。

(1)高铁酸钾(K2FeO4)中铁元素的化合价为
(2)过程a中K2FeO4体现
(3)过程b反应的离子方程式为
(4)碱性条件下用Fe(OH)3和KClO反应制备K2FeO4。配平其反应的化学方程式:
Fe(OH)3+_______KOH+_______KClO=_______ K2FeO4+_______KCl+_______H2O
(5)根据以上K2FeO4净水原理,相比于Cl2,其优点是
您最近半年使用:0次



