研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)Co基态原子核外电子排布式为_____ 。元素Mn与O中,第一电离能较大的是____ ,基态原子核外未成对电子数较多的是____ 。
(2)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为____ ,原因是____ 。
(3)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420nm,则r(O2-)为____ nm。MnO也属于NaCl型结构,晶胞参数为a'=0.448nm,则r(Mn2+)为____ nm。

(1)Co基态原子核外电子排布式为
(2)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为
(3)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420nm,则r(O2-)为

更新时间:2022-10-11 19:37:53
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】Na2SiF6 作杀虫剂和木材防腐剂,其制备反应为: 3SiF4 + 2Na2CO3 + 2H2O → 2Na2SiF6↓ + H4SiO4 + 2CO2↑,完成下列填空:
(1)上述所有物质中,某分子的空间构型为直线型,其电子式为_______ ,SiF4 是______ 分子(选填“极性”或“非极性”)。
(2)上述所有元素中,有两种元素位于周期表同一主族,该族元素原子的最外层电子排布通式为____ (用 n 表示电子层数),O、F、Na 三种元素形成的简单离子,半径由大到小顺序是______ 。
(3)H4SiO4 称为原硅酸,推测其是__ 酸(选填“强”或“弱”),从元素周期律角度解释上述推测_____ 。
(1)上述所有物质中,某分子的空间构型为直线型,其电子式为
(2)上述所有元素中,有两种元素位于周期表同一主族,该族元素原子的最外层电子排布通式为
(3)H4SiO4 称为原硅酸,推测其是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】尿素(H2NCONH2)是一种农业生产中常用的氮肥。在工业上,尿素还用于制造有机铁肥,如[Fe(H2NCONH2)6](NO3)3
(1)基态Fe3+的核外电子排布式为________ 。
(2)C、N、O三种元素的第一电离能由小到大的顺序是________ 。
(3)六氰合亚铁离子(Fe(CN) )中的配体CN-中C原子的杂化轨道类型是
)中的配体CN-中C原子的杂化轨道类型是________ ,写出一种与CN-互为等电子体的单质分子的结构式________ 。
(4)在一定条件下,NH3与CO2能合成尿素,1 mol尿素分子中,σ键的数目为________ 。
(5)有机铁肥[Fe(H2NCONH2)6](NO3)3化合物中,中心离子为____________ ,外界离子的中心原子的杂化方式:_____________ 外界离子的空间构型:___________ 。
(1)基态Fe3+的核外电子排布式为
(2)C、N、O三种元素的第一电离能由小到大的顺序是
(3)六氰合亚铁离子(Fe(CN)
 )中的配体CN-中C原子的杂化轨道类型是
)中的配体CN-中C原子的杂化轨道类型是(4)在一定条件下,NH3与CO2能合成尿素,1 mol尿素分子中,σ键的数目为
(5)有机铁肥[Fe(H2NCONH2)6](NO3)3化合物中,中心离子为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)合成氨反应是极其重要的氮的固定反应。已知键能数据如下:N≡N为E1kJ·mol—1、H—H为E2kJ·mol—1、N—H为E3 kJ·mol—1。则:
(2)HF与水可任意比混溶,其溶液中存在的分子间氢键有_____ 种;乙酸用五氧化二磷脱水,可得到乙烯酮( CH2=C=O),该分子中的羰基碳原子采用的杂化方式为________ ,一个分子中含有____________ 个 键。
键。
N2(g)+3H2(g)==2NH3(g);△H=
(2)HF与水可任意比混溶,其溶液中存在的分子间氢键有
 键。
键。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】晶体中Mg的原子堆积方式如图所示,这种堆积方式称为_______ 。已知镁原子半径为r,晶体中四个相邻的镁原子紧密堆积成正四面体,两层镁原子形成的正四面体高 ,晶胞的空间利用率为
,晶胞的空间利用率为_______ %(只写出化简式,不需计算结果)。

 ,晶胞的空间利用率为
,晶胞的空间利用率为
您最近一年使用:0次
【推荐2】Cu2O广泛应用于太阳能电池领域。以CuSO4、NaOH和抗坏血酸为原料,可制备Cu₂O。
(1)Cu2+基态核外电子排布式为________ 。
(2)SO42-的空间构型为_______ (用文字描述)。
(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为______ ;推测抗坏血酸在水中的溶解性:_______ (填“难溶于水”或“易溶于水”)。

(4)一个Cu2O晶胞(见图2)中,Cu原子的数目为_________ 。
(1)Cu2+基态核外电子排布式为
(2)SO42-的空间构型为
(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为

(4)一个Cu2O晶胞(见图2)中,Cu原子的数目为
您最近一年使用:0次

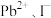 和有机碱离子
和有机碱离子 ,其晶胞如图(b)所示.其中
,其晶胞如图(b)所示.其中 与图(a)中
与图(a)中 ,则晶体密度为
,则晶体密度为 (列出计算式).
(列出计算式).
 的面心立方晶胞如图所示.设阿伏加德罗常数的值为
的面心立方晶胞如图所示.设阿伏加德罗常数的值为 ,则
,则


