下列反应方程式正确的是
A.向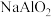 溶液中加入 溶液中加入 : :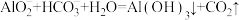 |
B.向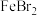 溶液中通入等量的 溶液中通入等量的 : :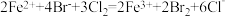 |
C.将少量 通入NaClO溶液中: 通入NaClO溶液中: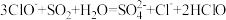 |
D.溴乙烷的消去反应: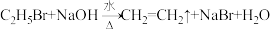 |
更新时间:2022-10-11 15:36:26
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列离子方程式正确的是
| A.向盐酸中滴加氨水:H+ + OH- = H2O |
| B.Fe(OH)3溶于氢碘酸:Fe(OH)3 + 3H+ = Fe3++ 3H2O |
C.铜溶于稀硝酸:3Cu + 8H+ + 2NO = 3Cu2+ + 2NO ↑+ 4H2O = 3Cu2+ + 2NO ↑+ 4H2O |
| D.向次氯酸钙溶液中通入SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列反应的离子方程式书写正确的是( )
| A.氯气溶于水:Cl2+H2O=2H++Cl-+ClO- |
| B.铜和硝酸银溶液反应:Cu+Ag+=Ag+Cu2+ |
| C.铁跟稀盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| D.大理石中滴加盐酸:CaCO3+2H+=Ca2++CO2↑+H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】某实验小组探究氨气与氯气的反应,装置如图所示,在常温常压下将氨气收集在薄膜保鲜袋(无弹性)中,氯气收集在反应管中,关闭K。如图连接好装置,将氨气压入反应管,充分反应后打开K,下列说法不正确的是
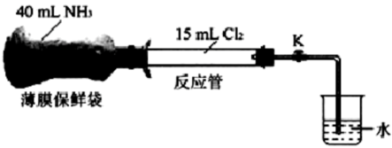

| A.该反应原理可应用于检验输送氯气的管道是否泄漏 |
| B.反应开始后,薄膜保鲜袋逐渐被吸入反应管中 |
| C.打开K后,烧杯内的水会倒吸入反应管 |
| D.反应过程中,反应管内气体颜色逐渐变浅,有白烟生成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】Na2SO3溶液是工业上常用的还原剂、防腐剂、去氯剂等。下列离子方程式正确的是
A.Na2SO3溶液在空气中易被氧化:SO +O2=SO +O2=SO |
B.Na2SO3溶液用作去氯剂:Cl2+SO +H2O=2H++2Cl-+SO +H2O=2H++2Cl-+SO |
C.0.1mol·L-1Na2SO3溶液pH>7:SO +2H2O +2H2O H2SO3+2OH- H2SO3+2OH- |
D.过量SO2与NaOH溶液反应生成Na2SO3溶液:SO2+2OH-=SO +H2O +H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】室温下,通过实验研究亚硫酸盐的性质,已知Ka1(H2SO3)=1.54×10-2,Ka2(H2SO3)=1.02×10-7
下列说法错误的是
| 实验 | 实验操作和现象 |
| 1 | 把SO2通入氨水,测得溶液pH=7 |
| 2 | 向0.1mol/LNa2SO3溶液中加入过量0.2mol/LCaCl2溶液,产生白色沉淀 |
| 3 | 向0.1mol/LNaHSO3溶液中滴入一定量NaOH溶液至pH=7 |
| 4 | 把少量氯气通入Na2SO3溶液中,测得pH变小 |
A.实验1中,可算出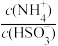 =3.04 =3.04 |
B.实验2反应静置后的上层清液中有c(Ca2+)·c(SO )=Ksp(CaSO3) )=Ksp(CaSO3) |
C.实验3中:c(Na+)>2[c(HSO )+c(SO )+c(SO )+c(H2SO3)] )+c(H2SO3)] |
D.实验4中反应的离子方程式为:H2O+Cl2+SO =SO =SO +2H++2Cl- +2H++2Cl- |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列各物质中,既能被催化氧化又能发生消去反应的是
| A.CH3OH | B.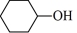 | C.(CH3)3CCH2OH | D.(CH3)3COH |
您最近一年使用:0次
【推荐2】深圳市卢洪洲研究团队于今年2月在《柳叶刀》刊发重要研究成果称,羟甲香豆素(Z)可用于治疗新冠病毒肺炎的普通型与重型。其合成涉及如图转化,下列有关说法正确的是
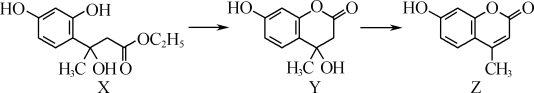

| A.强碱性氛围有利于物质Z的生成 |
| B.X和Y存在手性异构 |
C.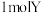 与足量 与足量 溶液反应,最多消耗 溶液反应,最多消耗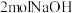 |
D.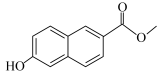 与Z互为同系物 与Z互为同系物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
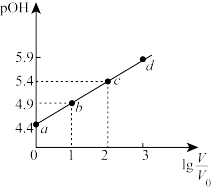
【推荐1】已知H3PO3与足量的NaOH溶液反应生成Na2HPO3。室温下向1 mol∙L−1Na2HPO3溶液中加水稀释,溶液的pOH与溶液稀释倍数关系如图。已知pOH=−lgc(OH-);lg4=0.60,  是开始溶液体积,V是加水后溶液体积。下列说法错误的是
是开始溶液体积,V是加水后溶液体积。下列说法错误的是
 是开始溶液体积,V是加水后溶液体积。下列说法错误的是
是开始溶液体积,V是加水后溶液体积。下列说法错误的是
| A.Na2HPO3的第一步水解常数约是10−8.8 |
| B.稀释100倍时溶液的pH=8.6 |
C.b点溶液中c(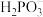 )+c( )+c( )+c(H3PO3)=1 mol∙L−1 )+c(H3PO3)=1 mol∙L−1 |
| D.H3PO3的第二步电离常数是6.4×10−6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】室温下,用0.100mol/LNaOH浴液分别滴定25.00mL0.1000mol/L一元弱酸HX、HY、HZ,已知三种弱酸的电离常数Ka(HX)>Ka(HY)>Ka(HZ)。滴定过程中,滴定曲线(pH-Φ)与一元弱酸电离常数的关系如图所示(滴定分数φ= ,R代表X、Y、Z)。下列说法错误的是
,R代表X、Y、Z)。下列说法错误的是
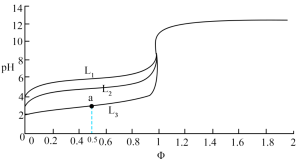
 ,R代表X、Y、Z)。下列说法错误的是
,R代表X、Y、Z)。下列说法错误的是
| A.L3代表HX的滴定曲线 |
| B.φ=0.5时,溶液中水的电离程度:HX>HY>HZ |
| C.a.点时,溶液中存在:c(HX)+2c(H+)=c(X-)+2c(OH-) |
| D.φ=0时,HZ的初始pH为4,则Ka(HZ)≈10-7 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】在室温下,下列叙述正确的是
| A.醋酸的电离平衡正向移动时,电离常数一定增大 |
| B.等浓度等体积的醋酸溶液和盐酸分别与氢氧化钠溶液反应,耗碱量相同 |
| C.用pH=1盐酸分别中和等体积pH=13氢氧化钠溶液和氨水,NaOH消耗盐酸的体积大 |
D.pH=2的盐酸与pH=1的硫酸比较,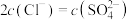 |
您最近一年使用:0次

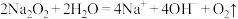


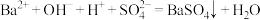
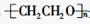 是通过加聚反应得到的产物
是通过加聚反应得到的产物

