用下图所示装置进行实验,证明过氧化钠( )可在呼吸面具和潜水艇中做供氧剂。
)可在呼吸面具和潜水艇中做供氧剂。

请回答:
(1)过氧化钠( )中氧元素的化合价是
)中氧元素的化合价是_______ (填序号)。
A.-1 B.-2
(2)装置B的作用是_______ 。
(3)装置C中过氧化钠与二氧化碳反应的化学方程式是_______ 。
(4)装置D中盛放的试剂是_______ 。
(5)用试管收集气体,该气体能_______ ,证明过氧化钠可做供氧剂。
 )可在呼吸面具和潜水艇中做供氧剂。
)可在呼吸面具和潜水艇中做供氧剂。
请回答:
(1)过氧化钠(
 )中氧元素的化合价是
)中氧元素的化合价是A.-1 B.-2
(2)装置B的作用是
(3)装置C中过氧化钠与二氧化碳反应的化学方程式是
(4)装置D中盛放的试剂是
(5)用试管收集气体,该气体能
更新时间:2022-10-11 20:02:10
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下列A~I九种物质之间的转化关系如图所示,其中部分生成物或反应条件已略去。已知A在常温下为黑色固体单质,常温下C、E、F都是无色气体。

请回答下列问题:
(1)C的固体名称________ ,F的化学式是________ 。
(2)B的浓溶液与A反应过程中,B体现的性质与下列反应中HNO3体现的性质完全相同的是_____ 。
A.C+4HNO3(浓) CO2+4NO2↑+2H2O
CO2+4NO2↑+2H2O
B.3Fe+8HNO3(稀 )=3Fe(NO3 )2+2NO↑+4H2O
C.Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O
D.2Fe2O3+6HNO3===2Fe(NO3)3+3H2O
(3)A与B反应的化学方程式是____________ 。
(4)G与H反应的离子方程式是_________________________ ;
C与淡黄色固体反应生成F与G的化学方程式__________________________ 。

请回答下列问题:
(1)C的固体名称
(2)B的浓溶液与A反应过程中,B体现的性质与下列反应中HNO3体现的性质完全相同的是
A.C+4HNO3(浓)
 CO2+4NO2↑+2H2O
CO2+4NO2↑+2H2OB.3Fe+8HNO3(稀 )=3Fe(NO3 )2+2NO↑+4H2O
C.Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O
D.2Fe2O3+6HNO3===2Fe(NO3)3+3H2O
(3)A与B反应的化学方程式是
(4)G与H反应的离子方程式是
C与淡黄色固体反应生成F与G的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】(Ⅰ)A、B、C三种无色可溶性盐分别是由Na+ 、Ag+ 、Ba2+、Cl-、NO 、CO
、CO 中不同的阴、阳离子所组成。经实验A溶液、B溶液均可以与盐酸反应,其中A产生白色沉淀,B产生气泡。则A为
中不同的阴、阳离子所组成。经实验A溶液、B溶液均可以与盐酸反应,其中A产生白色沉淀,B产生气泡。则A为___________ 、B为_________ 。将B和C的溶液混合反应的化学方程式为:___________________ 。
(Ⅱ)现有NaCl、Na2O2、Fe2O3、NaHCO3和Al2O3等多种重要化合物。
(1)常作为潜水艇和呼吸面具中氧气来源的淡黄色固体是___________ ;(写化学式,下同)
(2)常用于焙制糕点,也可用作抗酸药的是___________ ;
(3)属于两性氧化物的是___________ ; (4)属于红棕色固体是___________ 。
(III)只用试管和胶头滴管就可以鉴别的下列各组溶液是________ (填序号)
①AlCl3溶液和NaOH溶液 ②Ca(HCO3)2溶液和NaOH溶液
③NaAlO2溶液和盐酸 ④Al2(SO4)3溶液和氨水
 、CO
、CO 中不同的阴、阳离子所组成。经实验A溶液、B溶液均可以与盐酸反应,其中A产生白色沉淀,B产生气泡。则A为
中不同的阴、阳离子所组成。经实验A溶液、B溶液均可以与盐酸反应,其中A产生白色沉淀,B产生气泡。则A为(Ⅱ)现有NaCl、Na2O2、Fe2O3、NaHCO3和Al2O3等多种重要化合物。
(1)常作为潜水艇和呼吸面具中氧气来源的淡黄色固体是
(2)常用于焙制糕点,也可用作抗酸药的是
(3)属于两性氧化物的是
(III)只用试管和胶头滴管就可以鉴别的下列各组溶液是
①AlCl3溶液和NaOH溶液 ②Ca(HCO3)2溶液和NaOH溶液
③NaAlO2溶液和盐酸 ④Al2(SO4)3溶液和氨水
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】过氧化钠常用作漂白剂、杀菌剂、消毒剂,能与水和二氧化碳等物质发生反应,保存不当时容易变质。某实验小组以过氧化钠为研究对象进行了如下实验,请回答以下问题:
(1)纯净的Na2O2是________ 色固体,其中氧元素的化合价为_________ 价。
(2)该实验小组为了粗略测定过氧化钠的质量分数,称取了20.0 g样品,并设计用如图装置通过排水法测定E中收集到的O2的体积,来测定过氧化钠的质量分数。
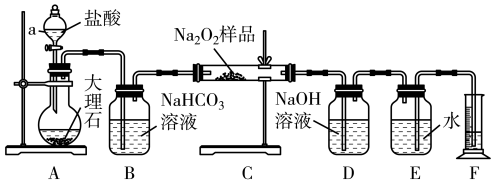
①将仪器连接好以后、加药品之前必须进行的一步操作_____ ,A中主要反应的离子方程式:_____ ;
②装置B的作用是除去二氧化碳气体中的______ 气体,写出相应的化学方程式_____ 。读出量筒内水的体积后,将其折算成标准状况下氧气的体积为2.24L,则样品中过氧化钠的质量分数为_____ 。
(1)纯净的Na2O2是
(2)该实验小组为了粗略测定过氧化钠的质量分数,称取了20.0 g样品,并设计用如图装置通过排水法测定E中收集到的O2的体积,来测定过氧化钠的质量分数。

①将仪器连接好以后、加药品之前必须进行的一步操作
②装置B的作用是除去二氧化碳气体中的
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X是固体,B和G是液体,其余均为气体。根据下图关系推断:
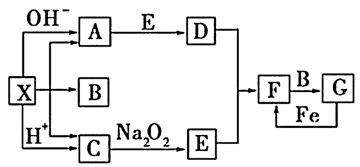
(1)化学式X____________ ,A__________ ,B________ 。
(2)实验室收集气体D和F的方法依次是____________ 法、__________ 法。
(3)写出C→E的化学反应方程式_____________________________ 。
(4)请写出A与E反应生成D的化学方程式____________________________ 。

(1)化学式X
(2)实验室收集气体D和F的方法依次是
(3)写出C→E的化学反应方程式
(4)请写出A与E反应生成D的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、F五种物质的焰色反应均为黄色,A、B、C、D与盐酸反应均生成E,此外B还生成一种可燃气体。而C、D还生成一种无色无味气体H,该气体能使澄清石灰水变浑浊。D和A可反应生成C,F和H也可反应生成C和另一种无色无味气体。请回答下列问题:
(1)写出A、B、C、D、E、F的化学式A、______ B、______ C、______ D、______ E、______ F、______ 。
(2)写出F和H反应的化学方程式______ 。
(3)写出下列反应的离子方程式:D+盐酸______ 。
(1)写出A、B、C、D、E、F的化学式A、
(2)写出F和H反应的化学方程式
(3)写出下列反应的离子方程式:D+盐酸
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】现有mg含有Na2O杂质的Na2O2样品,某同学在实验室用如图装置(部分夹持仪器已省略)测定其杂质含量:
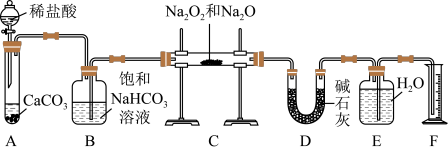
回答下列问题:
(1)装置A中反应的离子方程式为___________ 。
(2)图中有一处明显错误,请指出并改正:___________ 。
(3)装置B的作用是___________ ;装置D的作用是___________ ;若无装置D,样品中杂质的质量分数___________ (填“偏高”“偏低”或“无影响”)。
(4)写出装置C中Na2O2和CO2反应的化学方程式:___________ 。
(5)实验结束后,装置F中水的体积为VmL,已知氧气的密度为1.43g·L-1,样品的质量分数为___________ (用含m、V的代数式表示,列出计算式即可)。

回答下列问题:
(1)装置A中反应的离子方程式为
(2)图中有一处明显错误,请指出并改正:
(3)装置B的作用是
(4)写出装置C中Na2O2和CO2反应的化学方程式:
(5)实验结束后,装置F中水的体积为VmL,已知氧气的密度为1.43g·L-1,样品的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某班同学为验证酸的化学通性,做了五组实验。分析并回答问题。
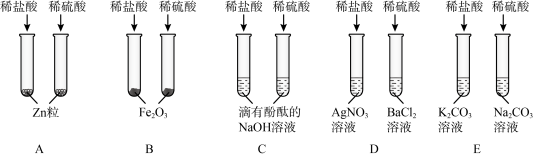
(1)A组试管中都产生H2。若要制得较纯的H2,选稀硫酸而不选盐酸的原因是___ 。
(2)B组试管中实验现象相同,该现象是___ 。
(3)写出D组任一试管中发生反应的化学方程式___ 。
(4)上述五组实验中没有体现酸的通性的是___ (填序号)。

(1)A组试管中都产生H2。若要制得较纯的H2,选稀硫酸而不选盐酸的原因是
(2)B组试管中实验现象相同,该现象是
(3)写出D组任一试管中发生反应的化学方程式
(4)上述五组实验中没有体现酸的通性的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】学习小组在实验室中利用下图装置制备SO2并进行相关性质的探究。
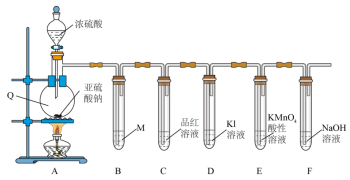
回答下列问题:
(1)盛放浓硫酸的仪器名称为___________ ;装置A中反应的化学方程式为___________ 。
(2)装置B是为了观察气体的流速,则试剂M为___________(填字母)。
(3)装置C中出现的现象说明SO2具有___________ 性。
(4)装置E中出现___________ (填现象)可说明SO2具有还原性, 被还原为Mn2+,该反应的离子方程式为
被还原为Mn2+,该反应的离子方程式为___________ 。
(5)装置F中过量的NaOH溶液吸收尾气发生的离子方程式为___________ 。
(6)实验开始后,发现装置D中的溶液迅速变黄,继续通入SO2,装置D中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应:SO2+4I-+4H+ S↓+2I2+2H2O。
S↓+2I2+2H2O。
探究I:探究浓度对上述可逆反应的影响
有同学认为除SO2的浓度外,其他离子的浓度对该可逆反应也有影响。完成实验设计进行验证(SO2体积已折算为标准状况下体积)。
限选试剂:0.1mol/LKI溶液、1.0mol/LKI溶液、2.0mol/LKI溶液、蒸馏水、浓盐酸、浓硝酸
探究II:探究SO2在KI溶液体系中的反应产物
有同学提出上述可逆反应生成的I2可与SO2进一步发生反应:SO2+I2+2H2O= +2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。
+2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。
综上可知,SO2在KI溶液中发生了歧化反应(KI是催化剂,只有硫元素变价),其反应的离子方程式为________ 。

回答下列问题:
(1)盛放浓硫酸的仪器名称为
(2)装置B是为了观察气体的流速,则试剂M为___________(填字母)。
| A.NaOH溶液 | B.饱和NaHSO3溶液 | C.Na2S溶液 | D.Na2SO3溶液 |
(4)装置E中出现
 被还原为Mn2+,该反应的离子方程式为
被还原为Mn2+,该反应的离子方程式为(5)装置F中过量的NaOH溶液吸收尾气发生的离子方程式为
(6)实验开始后,发现装置D中的溶液迅速变黄,继续通入SO2,装置D中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应:SO2+4I-+4H+
 S↓+2I2+2H2O。
S↓+2I2+2H2O。探究I:探究浓度对上述可逆反应的影响
有同学认为除SO2的浓度外,其他离子的浓度对该可逆反应也有影响。完成实验设计进行验证(SO2体积已折算为标准状况下体积)。
限选试剂:0.1mol/LKI溶液、1.0mol/LKI溶液、2.0mol/LKI溶液、蒸馏水、浓盐酸、浓硝酸
| 影响因素 | 编号 | 操作 | 现象 |
| c(I-) | i | 取50mL | 溶液变为浅黄色 |
| ii | 取50mL1.0mol/LKI溶液于锥形瓶中,向其中通入20mLSO2 | 溶液迅速变黄 | |
| c(H+) | iii | 取50mL1.0mol/LKI溶液和5mL | 溶液迅速变黄 |
| iv | 取50mL1.0mol/LKI溶液和5mL | 溶液迅速变黄,且出现乳黄色浑浊 |
有同学提出上述可逆反应生成的I2可与SO2进一步发生反应:SO2+I2+2H2O=
 +2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。
+2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。| 方案。 | 操作 | 预期现象 | 结论 |
| i | 取适量装置D中浊液,向其中滴加几滴 | 无明显变化 | 浊液中无I2 |
| ii | 将装置D中浊液进行分离 | 得淡黄色固体和澄清溶液 | 产物有 |
| 取适量分离后的澄清溶液于试管中,先加入盐酸酸化,再加入 | 产生 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】为了探究和验证氯气的性质,某研究性学习小组以MnO2和浓盐酸为主要原料,设计了如图所示装置(其中a是连有注射器针头的橡皮管,针头已插入并穿过橡皮塞)进行了研究。

(资料:氯气与铁反应制取氯化铁要在无水条件下进行)
试回答下列问题:
(l)装置A中发生反应的化学方程式为_____________________ 。
(2)装置B中的试剂为_________ ,装置D作用是________ 。
(3)装置C中发生反应的离子方程式为_____________________________ 。
(4)反应开始后,装置E发生反应的化学方程式为____________________________ 。
(5)装置F中发生反应的化学方程式为________________________ 。

(资料:氯气与铁反应制取氯化铁要在无水条件下进行)
试回答下列问题:
(l)装置A中发生反应的化学方程式为
(2)装置B中的试剂为
(3)装置C中发生反应的离子方程式为
(4)反应开始后,装置E发生反应的化学方程式为
(5)装置F中发生反应的化学方程式为
您最近一年使用:0次



