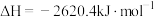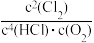题型:
难度:0.65
引用次数:582
题号:17128804
某可逆反应aA(g)+bB(g) cC(g) △H,在某温度下的平衡常数为K(K≠1),反应热为△H。保持温度不变,将方程式的书写作如下改变,则△H和K数值的相应变化为
cC(g) △H,在某温度下的平衡常数为K(K≠1),反应热为△H。保持温度不变,将方程式的书写作如下改变,则△H和K数值的相应变化为
 cC(g) △H,在某温度下的平衡常数为K(K≠1),反应热为△H。保持温度不变,将方程式的书写作如下改变,则△H和K数值的相应变化为
cC(g) △H,在某温度下的平衡常数为K(K≠1),反应热为△H。保持温度不变,将方程式的书写作如下改变,则△H和K数值的相应变化为A.写成2aA(g)+2bB(g) 2cC(g),△H、K均扩大了一倍 2cC(g),△H、K均扩大了一倍 |
B.写成2aA(g)+2bB(g) 2cC(g),△H扩大了一倍,K保持不变 2cC(g),△H扩大了一倍,K保持不变 |
C.写成:cC(g) aA(g)+bB(g),△H、K变为原来的相反数 aA(g)+bB(g),△H、K变为原来的相反数 |
D.写成cC(g) aA(g)+bB(g),△H变为原来的相反数,K变为原来的倒数 aA(g)+bB(g),△H变为原来的相反数,K变为原来的倒数 |
更新时间:2022-10-24 21:04:47
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】利用CO2和CH4重整可制合成气(主要成分为CO、H2)。下列有关说法正确的是
① CH4(g) = C(s)+2H2(g) △H1 = + 75.0 kJ·mol-1
② CO2(g)+H2(g) = CO(g)+H2O(g) △H2 = + 41.0 kJ·mol-1
③ CO(g)+H2(g) = C(s)+H2O(g) △H3 = -131.0 kJ·mol-1
| A.反应②为放热反应 |
| B.反应①中化学能转化为热能 |
| C.反应③使用催化剂,ΔH3减小 |
| D.反应CO2(g)+CH4(g)=2CO (g)+2H2 (g)的ΔH4 = +247kJ·mol–1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于反应能量的说法正确的是
| A.已知2C(s)+O2(g) = 2CO(g) ΔH,ΔH表示碳的摩尔燃烧焓 |
| B.已知2C(s)+2O2(g) = 2CO2(g) ΔH1;2C(s)+O2(g) = 2CO(g) ΔH2,则ΔH1>ΔH2 |
| C.若C(s,石墨) = C(s,金刚石) ΔH=+1.9 kJ·mol−1 ,则石墨比金刚石稳定 |
| D.H+ (aq)+OH− (aq) = H2O(l) ΔH=-57.3 kJ·mol−1,含1molNaOH的氢氧化钠溶液与含0.5mol H2SO4的浓硫酸混合后放出57.3kJ的热量 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知反应①:CO(g)+CuO(s)⇌CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)⇌Cu(s)+H2O(g)在相同温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)⇌CO2(g)+H2(g)的平衡常数为K.则下列说法正确的是
A.反应①的平衡常数K1= |
B.反应③的平衡常数K=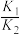 |
| C.对于反应③,恒容时,若温度升高,H2的浓度减小,则该反应的焓变为正值 |
| D.对于反应②,恒温恒容时,若加入CuO,平衡向正向移动,H2的浓度减小 |
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】化学反应原理在科研和生产中有广泛应用。
(1)利用“化学蒸气转移法”制备TaS2晶体,发生如下反应:TaS2(s)+2I2(g) TaI4(g)+S2(g) ΔH>0(Ⅰ),反应(Ⅰ)的平衡常数表达式K=
TaI4(g)+S2(g) ΔH>0(Ⅰ),反应(Ⅰ)的平衡常数表达式K=___________ ,若K=1,向某恒容容器中加入1 mol I2(g)和足量TaS2(s),I2(g)的平衡转化率为___________ 。
(2)利用I2的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,所用指示剂为___________ ,滴定反应的离子方程式为___________ 。
(3)25℃时,H2SO3 HSO
HSO +H +的电离常数Ka=1×10-2mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kh=
+H +的电离常数Ka=1×10-2mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kh=___________ mol·L-1。
(1)利用“化学蒸气转移法”制备TaS2晶体,发生如下反应:TaS2(s)+2I2(g)
 TaI4(g)+S2(g) ΔH>0(Ⅰ),反应(Ⅰ)的平衡常数表达式K=
TaI4(g)+S2(g) ΔH>0(Ⅰ),反应(Ⅰ)的平衡常数表达式K=(2)利用I2的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,所用指示剂为
(3)25℃时,H2SO3
 HSO
HSO +H +的电离常数Ka=1×10-2mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kh=
+H +的电离常数Ka=1×10-2mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kh=
您最近半年使用:0次


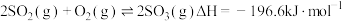
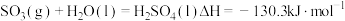
 作催化剂,则释放出的热量更多
作催化剂,则释放出的热量更多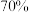 的浓硫酸吸收
的浓硫酸吸收
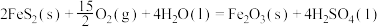 的焓变
的焓变