CO、 、
、 是工业上重要的化工原料。
是工业上重要的化工原料。
已知:①
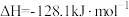
②
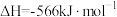
③
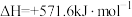
请回答下列问题:
(1)上述反应中属于放热反应的是_______ (填标号)。
(2)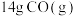 完全燃烧放出的热量为
完全燃烧放出的热量为_______ 。
(3)表示 的燃烧热的热化学方程式为
的燃烧热的热化学方程式为_______ 。
(4)1.5mol由CO和 组成的混合气体在足量氧气中充分燃烧放出的热量为425.9kJ,则混合气体中CO、
组成的混合气体在足量氧气中充分燃烧放出的热量为425.9kJ,则混合气体中CO、 的物质的量分别为
的物质的量分别为_______ mol、_______ mol。
(5)等质量的 、
、 、
、 完全燃烧,放热最多的是
完全燃烧,放热最多的是_______ (填化学式)。
(6)某些常见化学键的键能数据如下表:
则

_______  。
。
 、
、 是工业上重要的化工原料。
是工业上重要的化工原料。已知:①

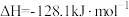
②

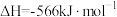
③

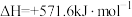
请回答下列问题:
(1)上述反应中属于放热反应的是
(2)
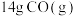 完全燃烧放出的热量为
完全燃烧放出的热量为(3)表示
 的燃烧热的热化学方程式为
的燃烧热的热化学方程式为(4)1.5mol由CO和
 组成的混合气体在足量氧气中充分燃烧放出的热量为425.9kJ,则混合气体中CO、
组成的混合气体在足量氧气中充分燃烧放出的热量为425.9kJ,则混合气体中CO、 的物质的量分别为
的物质的量分别为(5)等质量的
 、
、 、
、 完全燃烧,放热最多的是
完全燃烧,放热最多的是(6)某些常见化学键的键能数据如下表:
| 化学键 | C=O | H—O | H—H |  |
键能 | 803 | 463 | 436 | 1076 |


 。
。
更新时间:2022-11-07 09:10:28
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】(1)①H2(g)+ O2(g)= H2O(l) △H= —285.8 kJ/mol
O2(g)= H2O(l) △H= —285.8 kJ/mol
②H2(g)+ O2(g)= H2O(g) △H= —241.8kJ/mol
O2(g)= H2O(g) △H= —241.8kJ/mol
③C(s)+ O2 (g) = CO (g) △H= —110.5kJ/mol
O2 (g) = CO (g) △H= —110.5kJ/mol
④C(s)+ O2 (g) = CO2 (g) △H= —393.5kJ/mol
回答下列问题:
上述反应中属于放热的是_________ ;H2的燃烧热为________ ;C的燃烧热为_____ ;
(2)汽油的重要成分是辛烷(C8H18),1 mol C8H18(l)在O2(g)中燃烧,生成CO2(g)和H2O(l),放出5518 kJ热量。请写出此反应的热化学方程式___________
(3)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,若1g水蒸气转化成液态水时放热2.444kJ,试写出氢气的燃烧热的热化学方程式________
 O2(g)= H2O(l) △H= —285.8 kJ/mol
O2(g)= H2O(l) △H= —285.8 kJ/mol②H2(g)+
 O2(g)= H2O(g) △H= —241.8kJ/mol
O2(g)= H2O(g) △H= —241.8kJ/mol ③C(s)+
 O2 (g) = CO (g) △H= —110.5kJ/mol
O2 (g) = CO (g) △H= —110.5kJ/mol④C(s)+ O2 (g) = CO2 (g) △H= —393.5kJ/mol
回答下列问题:
上述反应中属于放热的是
(2)汽油的重要成分是辛烷(C8H18),1 mol C8H18(l)在O2(g)中燃烧,生成CO2(g)和H2O(l),放出5518 kJ热量。请写出此反应的热化学方程式
(3)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,若1g水蒸气转化成液态水时放热2.444kJ,试写出氢气的燃烧热的热化学方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】①C(s)+ O2(g)=CO(g) ΔH=-110.5 kJ/mol,②C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol,则CO的燃烧热为
O2(g)=CO(g) ΔH=-110.5 kJ/mol,②C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol,则CO的燃烧热为_______ ,其热化学方程式为________ 。
 O2(g)=CO(g) ΔH=-110.5 kJ/mol,②C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol,则CO的燃烧热为
O2(g)=CO(g) ΔH=-110.5 kJ/mol,②C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol,则CO的燃烧热为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】(1) 乙醇常被用做饮料的添加剂,在一定的条件下能被氧化为乙醛,乙醇氧化为乙醛的反应方程式为________________ ;乙醇_________ (“能”或“不能”)使酸性KMnO4溶液褪色;已知常温下,2.3 g乙醇和一定量的氧气混合后点燃,恰好完全燃烧,放出68.35 kJ热量,则该反应的热化学方程式为_______________________ 。
(2) 已知:
且硅晶体中每个硅原子和其他4个硅原子形成4个共价键,工业上制取高纯硅的反应方程式为:SiCl4(g)+2H2(g)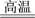 Si(s)+4HCl(g),该反应的反应热为
Si(s)+4HCl(g),该反应的反应热为________ kJ·mol-1。
(3) 已知水的比热容为4.18×10-3 kJ·g-1·oC-1。10 g硫黄在O2中完全燃烧生成气态SO2,放出的热量能使500 g H2O的温度由18 ℃升至62.4 ℃,则硫黄的燃烧热为_____________ ,热化学方程式为__________________________ 。
(2) 已知:
| 化学键 | Si—Cl | H—H | H—Cl | Si—Si |
| 键能/kJ·mol-1 | 360 | 436 | 431 | 176 |
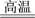 Si(s)+4HCl(g),该反应的反应热为
Si(s)+4HCl(g),该反应的反应热为(3) 已知水的比热容为4.18×10-3 kJ·g-1·oC-1。10 g硫黄在O2中完全燃烧生成气态SO2,放出的热量能使500 g H2O的温度由18 ℃升至62.4 ℃,则硫黄的燃烧热为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】I已知下列热化学方程式:
①H2(g)+ O2(g)═H2O(l);△H=-285.8kJ•mol-1
O2(g)═H2O(l);△H=-285.8kJ•mol-1
②H2(g)+ O2(g)═H2O(g);△H=-241.8kJ•mol-1
O2(g)═H2O(g);△H=-241.8kJ•mol-1
③CO(g)═C(s)+ O2(g);△H=+110.5kJ•mol-1
O2(g);△H=+110.5kJ•mol-1
④C(s)+O2(g)═CO2(g);△H=-393.5kJ•mol-1
回答下列问题:
(1)上述反应中属于放热反应的是_________________
(2)H2的燃烧热△H=___________________
(3)燃烧10gH2生成液态水,放出的热量为________________
(4)表示CO燃烧热的热化学方程式为.________________
II已知:(1)P4(s,白磷)+5O2(g)==P4O10(s)△H1=-2983.2kJ/mol
(2)P(s,红磷)+ O2(g)=
O2(g)=  P4O10(s) △H1=-738.5kJ/mol,则白磷转化为红磷的热化学方程式
P4O10(s) △H1=-738.5kJ/mol,则白磷转化为红磷的热化学方程式_________________ 。相同的状况下,能量较低的是_________________ ;白磷的稳定性比红磷_________________ (填“高”或“低”)
①H2(g)+
 O2(g)═H2O(l);△H=-285.8kJ•mol-1
O2(g)═H2O(l);△H=-285.8kJ•mol-1②H2(g)+
 O2(g)═H2O(g);△H=-241.8kJ•mol-1
O2(g)═H2O(g);△H=-241.8kJ•mol-1③CO(g)═C(s)+
 O2(g);△H=+110.5kJ•mol-1
O2(g);△H=+110.5kJ•mol-1④C(s)+O2(g)═CO2(g);△H=-393.5kJ•mol-1
回答下列问题:
(1)上述反应中属于放热反应的是
(2)H2的燃烧热△H=
(3)燃烧10gH2生成液态水,放出的热量为
(4)表示CO燃烧热的热化学方程式为.
II已知:(1)P4(s,白磷)+5O2(g)==P4O10(s)△H1=-2983.2kJ/mol
(2)P(s,红磷)+
 O2(g)=
O2(g)=  P4O10(s) △H1=-738.5kJ/mol,则白磷转化为红磷的热化学方程式
P4O10(s) △H1=-738.5kJ/mol,则白磷转化为红磷的热化学方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生下列反应:2N2(g)+6H2O(l)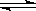 4NH3(g)+3O2(g) △H = akJ•mol-1
4NH3(g)+3O2(g) △H = akJ•mol-1
进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下:
①该反应的a______ 0(填“>”、“<”或“=”)
②已知:N2(g)+3H2(g)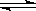 3NH3(g) △H = -92.4kJ•mol-1
3NH3(g) △H = -92.4kJ•mol-1
2H2(g) + O2(g)==2H2O(l) △H = -571.6 kJ•mol-1
则2N2(g) + 6H2O(l)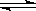 4NH3(g) + 3O2(g)△H =
4NH3(g) + 3O2(g)△H = _________ 。
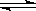 4NH3(g)+3O2(g) △H = akJ•mol-1
4NH3(g)+3O2(g) △H = akJ•mol-1进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下:
T/K | 303 | 313 | 323 |
NH3生成量/(10-6mol) | 4.8 | 5.8 | 6.0 |
①该反应的a
②已知:N2(g)+3H2(g)
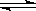 3NH3(g) △H = -92.4kJ•mol-1
3NH3(g) △H = -92.4kJ•mol-12H2(g) + O2(g)==2H2O(l) △H = -571.6 kJ•mol-1
则2N2(g) + 6H2O(l)
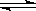 4NH3(g) + 3O2(g)△H =
4NH3(g) + 3O2(g)△H =
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】由碳元素构成的各种单质和化合物始终都是科学家研究的重要对象。
Ⅰ.甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用转化中得到的合成气制备甲醇。反应为CO(g)+2H2(g) CH3OH(g),某温度下,在容积为2L的密闭容器中进行该反应,其相关数据见图:
CH3OH(g),某温度下,在容积为2L的密闭容器中进行该反应,其相关数据见图:
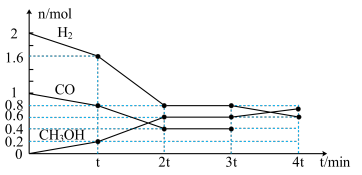
①根据图计算,从反应开始到tmin时,用H2浓度变化表示的平均反应速率υ(H2)=__ 。
②tmin至2tmin时速率变化的原因可能是__ (要求答出所有可能原因)。
Ⅱ.一定温度下,向一容积为5L的恒容密闭容器中充入0.4molSO2和0.2molO2,发生反应:2SO2(g)+O2(g) 2SO3(g) ΔH=-196kJ·mol-1。当反应达到平衡时,容器内压强变为起始时的
2SO3(g) ΔH=-196kJ·mol-1。当反应达到平衡时,容器内压强变为起始时的 。请回答下列问题:
。请回答下列问题:
①SO2的转化率为__ ;
②达到平衡时反应放出的热量为__ 。
Ⅰ.甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用转化中得到的合成气制备甲醇。反应为CO(g)+2H2(g)
 CH3OH(g),某温度下,在容积为2L的密闭容器中进行该反应,其相关数据见图:
CH3OH(g),某温度下,在容积为2L的密闭容器中进行该反应,其相关数据见图:
①根据图计算,从反应开始到tmin时,用H2浓度变化表示的平均反应速率υ(H2)=
②tmin至2tmin时速率变化的原因可能是
Ⅱ.一定温度下,向一容积为5L的恒容密闭容器中充入0.4molSO2和0.2molO2,发生反应:2SO2(g)+O2(g)
 2SO3(g) ΔH=-196kJ·mol-1。当反应达到平衡时,容器内压强变为起始时的
2SO3(g) ΔH=-196kJ·mol-1。当反应达到平衡时,容器内压强变为起始时的 。请回答下列问题:
。请回答下列问题:①SO2的转化率为
②达到平衡时反应放出的热量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)已知乙炔(C2H2)气体的燃烧热为ΔH=-1 299.6 kJ·mol-1,请写出表示乙炔燃烧热的热化学方程式____________________________________ 。
(2)已知:CH4(g)+4NO2( g)=4NO(g)+CO2(g)+2H2O(g) △H= -560 kJ·mol-l;
CH4(g)+4NO(g)=2N2 (g)+CO2 (g)+2H2O(g) △H=-1160 kJ·mol-1;
①若用标准状况下4.48 L CH4还原NO2生成N2,反应中转移的电子总数为_________ ,(用NA表示阿伏加 德罗常数值),放出的热量为_________ kJ。
②若1 mol CH4还原NO2时放出的热量为710 kJ,则生成的N2和NO的物质的量之比为_____ 。
(3)工业合成氨的反应N2+3H2=2NH3的能量变化如图所示,请回答有关问题:
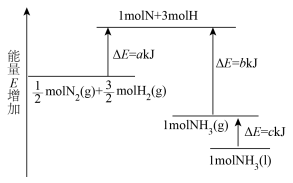
①合成1 mol NH3(l)________ (填“吸收”或“放出”)________ kJ的热量。
②已知:拆开 1 mol H—H键、1 mol N—H键、1 mol N≡N 键分别需要的能量是436 kJ、391 kJ、946 kJ。则图中的a=________ kJ;1 mol N2(g) 完全反应生成NH3(g)产生的能量变化为________ kJ。
(2)已知:CH4(g)+4NO2( g)=4NO(g)+CO2(g)+2H2O(g) △H= -560 kJ·mol-l;
CH4(g)+4NO(g)=2N2 (g)+CO2 (g)+2H2O(g) △H=-1160 kJ·mol-1;
①若用标准状况下4.48 L CH4还原NO2生成N2,反应中转移的电子总数为
②若1 mol CH4还原NO2时放出的热量为710 kJ,则生成的N2和NO的物质的量之比为
(3)工业合成氨的反应N2+3H2=2NH3的能量变化如图所示,请回答有关问题:

①合成1 mol NH3(l)
②已知:拆开 1 mol H—H键、1 mol N—H键、1 mol N≡N 键分别需要的能量是436 kJ、391 kJ、946 kJ。则图中的a=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题
(1)已知:2SO2(g)+O2(g)=2SO3(g) ΔH= -x kJ·mol-1
2NO(g)+O2(g)=2NO2(g) ΔH= -y kJ·mol-1
则反应NO2(g)+SO2(g)=SO3(g)+NO(g)的ΔH=_______ kJ·mol-1。
(2)已知:2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ·mol-1
查阅文献资料,化学键的键能如下表:
①氨分解反应NH3(g)= N2(g)+
N2(g)+ H2(g)的活化能Eal=300kJ·mol-1,则合成氨反应
H2(g)的活化能Eal=300kJ·mol-1,则合成氨反应 N2(g)+
N2(g)+ H2(g)=NH3(g)的活化能Ea2=
H2(g)=NH3(g)的活化能Ea2=_______ kJ·mol-1。
②氨气完全燃烧生成N2(g)和气态水的热化学方程式为_______ 。
(3)研究氮氧化物与悬浮的大气中海盐粒子的相互作用时,涉及如下反应:
I.2NO2(g)+NaCl(s)=NaNO3(s)+ClNO(g) ΔH1<0
II.2NO(g)+Cl2(g)=2ClNO(g) ΔH2<0
则反应4NO2(g)+2NaCl(s)=2NaNO3(s)+2NO(g)+Cl2(g)的ΔH=_______ (用ΔH1、ΔH2表示);
(1)已知:2SO2(g)+O2(g)=2SO3(g) ΔH= -x kJ·mol-1
2NO(g)+O2(g)=2NO2(g) ΔH= -y kJ·mol-1
则反应NO2(g)+SO2(g)=SO3(g)+NO(g)的ΔH=
(2)已知:2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ·mol-1
查阅文献资料,化学键的键能如下表:
| 化学键 | H—H键 | N≡N键 | N—H键 |
| E/(kJ·mol-1) | 436 | 946 | 391 |
①氨分解反应NH3(g)=
 N2(g)+
N2(g)+ H2(g)的活化能Eal=300kJ·mol-1,则合成氨反应
H2(g)的活化能Eal=300kJ·mol-1,则合成氨反应 N2(g)+
N2(g)+ H2(g)=NH3(g)的活化能Ea2=
H2(g)=NH3(g)的活化能Ea2=②氨气完全燃烧生成N2(g)和气态水的热化学方程式为
(3)研究氮氧化物与悬浮的大气中海盐粒子的相互作用时,涉及如下反应:
I.2NO2(g)+NaCl(s)=NaNO3(s)+ClNO(g) ΔH1<0
II.2NO(g)+Cl2(g)=2ClNO(g) ΔH2<0
则反应4NO2(g)+2NaCl(s)=2NaNO3(s)+2NO(g)+Cl2(g)的ΔH=
您最近一年使用:0次
【推荐1】(1)室温下,2 g 苯(C6H6)完全燃烧生成液态水和CO2,放出83.6 kJ的热量,写出 1 mol C6H6完全燃烧的热化学方程式:______________________ 。
(2)已知:Fe2O3(s)+ C(s)=
C(s)= CO2(g)+2Fe(s) ΔH=+a kJ/mol
CO2(g)+2Fe(s) ΔH=+a kJ/mol
C(s)+O2(g)=CO2(g) ΔH=-b kJ/mol
则2Fe(s)+ O2(g)=Fe2O3(s)的ΔH=
O2(g)=Fe2O3(s)的ΔH=_____ 。
(3)已知下列两个热化学方程式:
H2(g)+ O2(g) =H2O(l) ΔH=-285.8 kJ/mol
O2(g) =H2O(l) ΔH=-285.8 kJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-2220.0 kJ/mol
①实验测得H2和C3H8的混合气体共 5 mol,完全燃烧生成液态水时放热6264.5 kJ,则混合气体中H2和C3H8的体积之比为____________ 。
②已知:H2O(l)=H2O(g) ΔH=+44.0 kJ/mol
求1mol丙烷燃烧生成CO2和气态水的ΔH=______ 。
(4)已知2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l) ΔH=-1225 kJ/mol
则使 1 mol N2O4(l)完全分解成相应的原子时需要吸收的能量是________ 。
(2)已知:Fe2O3(s)+
 C(s)=
C(s)= CO2(g)+2Fe(s) ΔH=+a kJ/mol
CO2(g)+2Fe(s) ΔH=+a kJ/molC(s)+O2(g)=CO2(g) ΔH=-b kJ/mol
则2Fe(s)+
 O2(g)=Fe2O3(s)的ΔH=
O2(g)=Fe2O3(s)的ΔH=(3)已知下列两个热化学方程式:
H2(g)+
 O2(g) =H2O(l) ΔH=-285.8 kJ/mol
O2(g) =H2O(l) ΔH=-285.8 kJ/molC3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-2220.0 kJ/mol
①实验测得H2和C3H8的混合气体共 5 mol,完全燃烧生成液态水时放热6264.5 kJ,则混合气体中H2和C3H8的体积之比为
②已知:H2O(l)=H2O(g) ΔH=+44.0 kJ/mol
求1mol丙烷燃烧生成CO2和气态水的ΔH=
(4)已知2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l) ΔH=-1225 kJ/mol
| 化学键 | N—H | N—N | N≡N | O—H |
| 键能 (kJ/mol) | 390 | 190 | 946 | 460 |
则使 1 mol N2O4(l)完全分解成相应的原子时需要吸收的能量是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】 已知几种共价键的键能数据如下:
(1)通过计算,写出合成氨反应的热化学方程式____________________ 。
(2)某温度下,以1 mol N2和3mol H2作为初始反应物,在体积为2 L的恒容密闭容器中进行合成氨反应,达到平衡时测得反应放热68.1 kJ,试计算N2的转化率__________ 和该温度下的化学平衡常数________________ 。
| 共价键 | N≡N | H-H | N-H |
| 键能/(kJ·mol-1) | 946 | 436 | 390.8 |
(2)某温度下,以1 mol N2和3mol H2作为初始反应物,在体积为2 L的恒容密闭容器中进行合成氨反应,达到平衡时测得反应放热68.1 kJ,试计算N2的转化率
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】(1)已知单质硫在通常条件下以S8(斜方硫)的形式存在,而在蒸气状态时,含有S2、S4、S6及S8等多种同素异形体,其中S4、S6和S8具有相似的结构特点,其结构如图所示:
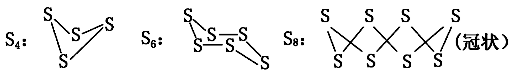
①在一定温度下,测得硫蒸气的平均摩尔质量为80 g·mol-1,则该蒸气中S2分子的体积分数不小于_______ 。
②若已知硫氧键的键能为d kJ·mol-1,氧氧键的键能为e kJ·mol-1,S(s)+O2(g)===SO2(g) ΔH=-a kJ·mol-1,则S8分子硫硫键的键能为________ 。
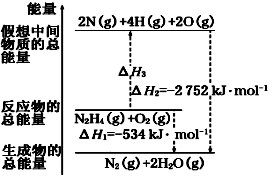
(2)肼(H2N—NH2)是一种高能燃料,有关化学反应的能量变化如图所示。已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O===O为500、N—N为154,则断裂1 mol N—H键所需的能量是_____________ kJ
(3)如表所示是某些物质的燃烧热数据:
①煤油的组成可看作C12H26,煤油燃烧生成液态水时的热化学方程式为________________ 。
②由上表中的数据_____ (填“能”或“不能”)计算出反应:C2H4(g)+H2(g)―→C2H6(g)的反应热。若能,该反应△H= _____ (若不能,此空不填);若不能,原因是 (若能, 此空不填)。

①在一定温度下,测得硫蒸气的平均摩尔质量为80 g·mol-1,则该蒸气中S2分子的体积分数不小于
②若已知硫氧键的键能为d kJ·mol-1,氧氧键的键能为e kJ·mol-1,S(s)+O2(g)===SO2(g) ΔH=-a kJ·mol-1,则S8分子硫硫键的键能为
(2)肼(H2N—NH2)是一种高能燃料,有关化学反应的能量变化如图所示。已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O===O为500、N—N为154,则断裂1 mol N—H键所需的能量是

(3)如表所示是某些物质的燃烧热数据:
| 物质 | C(s) | H2(g) | C2H4(g) | C2H6(g) | C3H8(g) | C12H26(l) |
| ΔH/ kJ·mol-1 | -393.5 | -285.8 | -1 411.0 | -1 559.8 | -2 219.9 | -8 571.4 |
①煤油的组成可看作C12H26,煤油燃烧生成液态水时的热化学方程式为
②由上表中的数据
您最近一年使用:0次

 催化重整不仅可以得到合成气(CO和
催化重整不仅可以得到合成气(CO和 。
。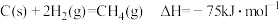
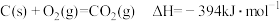
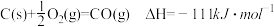
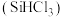 是制备硅烷、多晶硅的重要原料。回答下列问题:
是制备硅烷、多晶硅的重要原料。回答下列问题: 在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成
在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成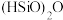 等,写出该反应的化学方程式:
等,写出该反应的化学方程式:

 的
的 为
为

