18. 碳酸钠和碳酸氢钠是中学化学常见的化合物,某化学兴趣小组对碳酸钠和碳酸氢钠与稀盐酸的反应进行了如下实验:
Ⅰ:验证

和
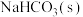
分别与稀盐酸反应的快慢
向2支具支试管中分别加入0.1 g碳酸钠和0.08 g碳酸氢钠粉末,2支注射器中各抽取5 mL 1

稀盐酸,如图所示,用注射器同压板同时按下注射器活塞,注入稀盐酸,观察现象。
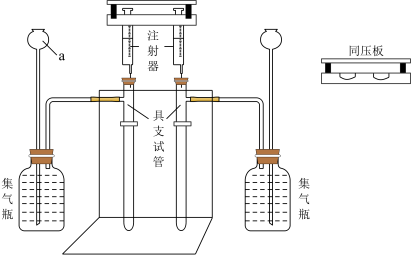
(1)仪器a的名称是
_______。
(2)加入试剂前需
_______。
(3)集气瓶中的试剂最优选择是
_______(填标号),使用同压板的优点有
_______(填一条即可)。
A.滴有红墨水的水
B.滴有红墨水的饱和碳酸钠溶液
C.滴有红墨水的饱和碳酸氢钠溶液
(4)为验证

和
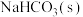
分别与稀盐酸反应的快慢,需测量的数据是
_______。
Ⅱ:探究

和
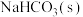
与稀盐酸反应的热效应(实验中所用盐酸浓度均为1.0

)
实验一:向试剂1中加入试剂2,搅拌、测温,记录结果如表所示。
| 试剂1 | 试剂2混合前的温度/℃ | 混合后最高或最低温度/℃ |
1.0 g  | 20 mL HCl 22.0 | 25.5 |
1.0 g 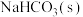 | 20 mL HCl 22.0 | 19.4 |
实验二:向试剂3中加入试剂4,搅拌、测温,静置、测温,再加入试剂5,搅拌、测温,记录结果如表所示。
| 试剂3 | 试剂4温度/C | 溶解后温度/℃ | 静置后温度/℃ | 试剂5温度/℃ | 混合后温度/c |
1.0 g  | 20 mL  22.0 22.0 | 23.8 | 22.0 | 20 mL HCl
22.0 | 23.5 |
1.0 g 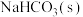 | 20 mL  22.0 22.0 | 19.5 | 22.0 | 20 mL HCl
22.0 | 21.4 |
(5)通过实验一的数据计算:(可近似地认为实验中所用溶液的密度、比热容与水的相同,并忽略容器的比热容,水的比热容为
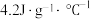
)
①
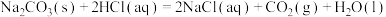
 _______
_______(保留四位有效数字,下同)

。
②
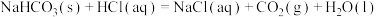
 _______
_______
。
(6)分析实验二可知,
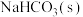
溶于水是
_______(填“放热”或“吸热”,下同)过程,
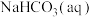
与稀盐酸的反应是
_______反应。
(7)该小组同学通过查阅资料发现,实验中测得的

、

均偏小,排除实验中的误差,出现该结果的原因可能是
_______。