现有以下物质:①NaOH溶液,②液氨,③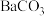 固体,④熔融
固体,④熔融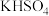 ,⑤
,⑤ 胶体,⑥铜,⑦
胶体,⑥铜,⑦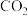 ,⑧
,⑧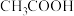 。
。
(1)以上物质中属于非电解质的是_______ (填序号,下同),能导电的物质有_______ 。
(2)写出①和⑧的水溶液反应的离子方程式_______ 。
(3)写出④的电离方程式_______ 。
(4)在足量④的水溶液中加入少量③,发生反应的离子方程式为_______ 。
(5)在含①的溶液中缓缓通少量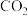 ,该过程的离子反应方程式为
,该过程的离子反应方程式为_______ 。
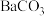 固体,④熔融
固体,④熔融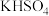 ,⑤
,⑤ 胶体,⑥铜,⑦
胶体,⑥铜,⑦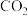 ,⑧
,⑧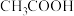 。
。(1)以上物质中属于非电解质的是
(2)写出①和⑧的水溶液反应的离子方程式
(3)写出④的电离方程式
(4)在足量④的水溶液中加入少量③,发生反应的离子方程式为
(5)在含①的溶液中缓缓通少量
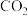 ,该过程的离子反应方程式为
,该过程的离子反应方程式为
更新时间:2022-10-31 19:48:04
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现有以下物质,回答有关问题。
A.氢氧化铝胶体;B.食盐水;C.铜;D.硝酸;E.烧碱;F.蔗糖;G.泥水;H.一氧化碳;I. CuSO4·5H2O晶体;J. CO2 ;K.HCl气体;L.CaO固体;M.食醋(含醋酸的溶液)
(1)以上物质中属于电解质的是_________ (填序号)。
(2)以上物质中的酸性氧化物与足量氢氧化钠反应的方程式__________________ 。
(3)写出下列物质在水溶液中的电离方程式:
Ca(OH)2__________________ ;
K2CO3__________________ ;
NaHSO4__________________ ;
醋酸(CH3COOH)__________________ 。
A.氢氧化铝胶体;B.食盐水;C.铜;D.硝酸;E.烧碱;F.蔗糖;G.泥水;H.一氧化碳;I. CuSO4·5H2O晶体;J. CO2 ;K.HCl气体;L.CaO固体;M.食醋(含醋酸的溶液)
(1)以上物质中属于电解质的是
(2)以上物质中的酸性氧化物与足量氢氧化钠反应的方程式
(3)写出下列物质在水溶液中的电离方程式:
Ca(OH)2
K2CO3
NaHSO4
醋酸(CH3COOH)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有下列十二种物质:①H2 ②铜 ③CaO固体 ④CO2 ⑤H2SO4溶液 ⑥Ba(OH)2⑦熔融的KNO3 ⑧液氨 ⑨稀硝酸 ⑩Al2(SO4)3 ⑪葡萄糖 ⑫FeCl3
(1)⑩在水中的电离方程式为_______
(2)以上属于电解质的共有_______ 种,属于非电解质的是_______ (填序号,下同),能导电的物质有_______ 。
(3)将少量的④通入⑥的溶液中反应的离子方程式:_______ 。上述十二种物质中有两物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学方程式为:_______ 。
(4)将FeCl3的饱和溶液滴入沸水中可以制得Fe(OH)3胶体,写出该化学方程式为:_______ 。
(1)⑩在水中的电离方程式为
(2)以上属于电解质的共有
(3)将少量的④通入⑥的溶液中反应的离子方程式:
(4)将FeCl3的饱和溶液滴入沸水中可以制得Fe(OH)3胶体,写出该化学方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下列物质中①Fe ②NH3 ③稀盐酸 ④酒精 ⑤H2SO4 ⑥熔融BaSO4(填相应的编号)
(1)属于电解质的是________________________ ;
(2)属于酸的是_______________________ ;
(3)所给状态下能导电的物质____________________ ;
(4)写出⑤在水中的电离方程式__________________________________________ ;写出①和③反应的离子方程式:________________________________________ 。
(1)属于电解质的是
(2)属于酸的是
(3)所给状态下能导电的物质
(4)写出⑤在水中的电离方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求回答下列问题:
(1)现有下列物质:①二氧化碳;②硝酸钾晶体;③铝;④空气;⑤熔融氯化钠;⑥稀硫酸;⑦氢氧化钠固体.请用序号回答下列问题:
其中属于混合物的是______ ;属于盐的是______ ;属于电解质的是______ ;能够导电的是______ .
(2)实验室里迅速制备少量氯气可利用如下反应: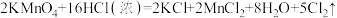
①该反应中,氧化剂是______ (填化学式).
②请用双线桥标出上述氧化还原反应中电子转移的方向和数目:______________________________ .
③当有0.5mol氧化剂参加反应时,被氧化的还原剂的物质的量是____________ .
(1)现有下列物质:①二氧化碳;②硝酸钾晶体;③铝;④空气;⑤熔融氯化钠;⑥稀硫酸;⑦氢氧化钠固体.请用序号回答下列问题:
其中属于混合物的是
(2)实验室里迅速制备少量氯气可利用如下反应:
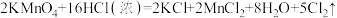
①该反应中,氧化剂是
②请用双线桥标出上述氧化还原反应中电子转移的方向和数目:
③当有0.5mol氧化剂参加反应时,被氧化的还原剂的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请回答下列问题:
(1)现有以下物质:① 固体 ②
固体 ② ③液态醋酸 ④铜 ⑤盐酸 ⑥酒精(C2H5OH) ⑦熔融
③液态醋酸 ④铜 ⑤盐酸 ⑥酒精(C2H5OH) ⑦熔融 ;请回答下列问题(用序号填写);其中能导电的是
;请回答下列问题(用序号填写);其中能导电的是___________ ;属于电解质的是___________ ;属于非电解质的是___________ 。
(2)某溶液的溶质可能由下列离子组成: 、
、 、
、 、
、 、
、 、
、 ,某同学进行了如下实验:
,某同学进行了如下实验:
Ⅰ.向溶液中加入过量的 溶液,有白色沉淀产生,过滤;
溶液,有白色沉淀产生,过滤;
Ⅱ.向Ⅰ中滤液中加入 溶液,有白色沉淀产生;
溶液,有白色沉淀产生;
Ⅲ.将Ⅰ中的沉淀加入足量稀盐酸中,沉淀部分消失,有气体产生。
依据以上实验可以推断,原溶液中一定含有___________ ;一定没有___________ ;写出Ⅲ中发生反应的离子方程式___________ 。
(1)现有以下物质:①
 固体 ②
固体 ② ③液态醋酸 ④铜 ⑤盐酸 ⑥酒精(C2H5OH) ⑦熔融
③液态醋酸 ④铜 ⑤盐酸 ⑥酒精(C2H5OH) ⑦熔融 ;请回答下列问题(用序号填写);其中能导电的是
;请回答下列问题(用序号填写);其中能导电的是(2)某溶液的溶质可能由下列离子组成:
 、
、 、
、 、
、 、
、 、
、 ,某同学进行了如下实验:
,某同学进行了如下实验:Ⅰ.向溶液中加入过量的
 溶液,有白色沉淀产生,过滤;
溶液,有白色沉淀产生,过滤;Ⅱ.向Ⅰ中滤液中加入
 溶液,有白色沉淀产生;
溶液,有白色沉淀产生;Ⅲ.将Ⅰ中的沉淀加入足量稀盐酸中,沉淀部分消失,有气体产生。
依据以上实验可以推断,原溶液中一定含有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有下列物质:①铜;②冰醋酸(纯醋酸晶体);③熔融的KNO3;④稀盐酸;⑤CO2;⑥KHSO4晶体;⑦蔗糖;⑧Fe(OH)3胶体;⑨液氯;⑩BaSO4固体
(1)属于电解质的是___________ 。属于非电解质的是___________ ,既不是电解质也不是非电解质的是___________ 。
(2)写出⑥在水中的电离方程式___________ ;写出除去Na2CO3固体中的NaHCO3的化学方程式___________ ;在沸水中滴入饱和氯化铁溶液制备⑧的化学方程式是___________ 。
(3)等质量的CO和CO2物质的量之比为___________ ;氧原子个数之比为___________ ;V L Al2(SO4)3溶液中含Al3+ a mol,该Al2(SO4)3溶液的物质的量浓度为___________ mol/L(用含a的式子表示,下同),取出0.5V L再加入水稀释到4V L,则稀释后的溶液中SO 的物质的量浓度为
的物质的量浓度为___________ 。
(1)属于电解质的是
(2)写出⑥在水中的电离方程式
(3)等质量的CO和CO2物质的量之比为
 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】现有以下物质:①汞 ②氨水 ③液态的醋酸 ④ NaCl晶体 ⑤硫酸溶液 ⑥SO2 ⑦BaSO4固体 ⑧酒精 ⑨氢氧化钠 ⑩熔化的KNO3 ,请回答下列问题(用序号)
a.能导电的是_____________________________________ ,
b.属于电解质的是_________________________________ ,
c.属于非电解质的是________________________________ ,
d.既不属于电解质也不属于非电解质的是________________________________
a.能导电的是
b.属于电解质的是
c.属于非电解质的是
d.既不属于电解质也不属于非电解质的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】钙元素存在如图循环转化关系。回答下列问题:
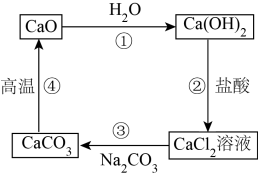
(1)上述转化关系中的 、
、 、
、 、
、 溶液、
溶液、 、
、 六种物质中,属于电解质的有
六种物质中,属于电解质的有_______ 种,能导电有_______ 种,属于氧化物的是_______ (填化学式);
(2)反应①~④中不涉及四个基本反应类型中的_______ ;
(3)写出反应③的化学方程式:_______ 。

(1)上述转化关系中的
 、
、 、
、 、
、 溶液、
溶液、 、
、 六种物质中,属于电解质的有
六种物质中,属于电解质的有(2)反应①~④中不涉及四个基本反应类型中的
(3)写出反应③的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)写出明矾[KAl(SO4)2•12H2O]在水中的电离方程式________________ ,明矾净水的原因是因为它与水反应产生的Al(OH)3胶体具有___________ 性。
(2)溶液的导电能力大小主要是由离子浓度大小决定的,利用“液体导电性的实验装置”(如图所示)作下列实验,灯泡能出现由亮—暗—熄灭—亮现象的是_______
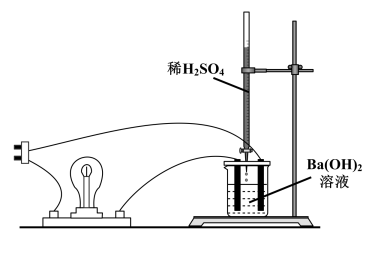
A.向BaCl2溶液中滴入稀H2SO4
B.向Ba(OH)2溶液中滴入稀H2SO4
C.向NaOH溶液中滴入盐酸
写出所选项的离子反应方程式_______________ (若上题选错,该项不得分)。
(3)Mn2+、Bi3+、BiO 、MnO
、MnO 、H+、H2O组成的一个氧化还原反应体系中,发生BiO
、H+、H2O组成的一个氧化还原反应体系中,发生BiO →Bi3+的反应过程。
→Bi3+的反应过程。
①该反应中,被氧化的元素是_______ ,氧化剂是______ 。
②将以上物质分别填入下面对应的横线上,组成一个未配平 的化学方程式_______ _____+ ______+ ________→ ______+ ________+ H2O
③反应中若产生0.2mol的还原产物,则有____ mol电子转移。
(1)写出明矾[KAl(SO4)2•12H2O]在水中的电离方程式
(2)溶液的导电能力大小主要是由离子浓度大小决定的,利用“液体导电性的实验装置”(如图所示)作下列实验,灯泡能出现由亮—暗—熄灭—亮现象的是

A.向BaCl2溶液中滴入稀H2SO4
B.向Ba(OH)2溶液中滴入稀H2SO4
C.向NaOH溶液中滴入盐酸
写出所选项的离子反应方程式
(3)Mn2+、Bi3+、BiO
 、MnO
、MnO 、H+、H2O组成的一个氧化还原反应体系中,发生BiO
、H+、H2O组成的一个氧化还原反应体系中,发生BiO →Bi3+的反应过程。
→Bi3+的反应过程。①该反应中,被氧化的元素是
②将以上物质分别填入下面对应的横线上,组成一个
③反应中若产生0.2mol的还原产物,则有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】实验室制备氯酸钾、次氯酸钠和氯水的装置如图所示。
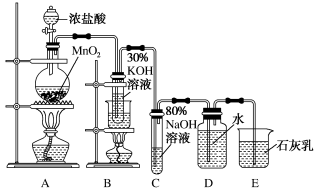
制备KClO3需在70~80℃进行,写出制备KClO3的离子方程式:___ 。

制备KClO3需在70~80℃进行,写出制备KClO3的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
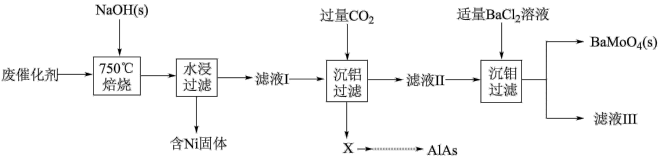
【推荐2】对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝( )、钼(
)、钼( )、镍(
)、镍( )等元素的氧化物,一种回收利用工艺的部分流程如下:
)等元素的氧化物,一种回收利用工艺的部分流程如下:
已知:25℃时, 的
的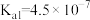 ,
, ;
;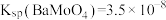 ;
;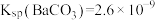 ;该工艺中,
;该工艺中,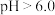 时,溶液中
时,溶液中 元素以
元素以 的形态存在。
的形态存在。
“沉钼”中, 为7.0。
为7.0。
生成 的离子方程式为
的离子方程式为_______ 。
 )、钼(
)、钼( )、镍(
)、镍( )等元素的氧化物,一种回收利用工艺的部分流程如下:
)等元素的氧化物,一种回收利用工艺的部分流程如下:
已知:25℃时,
 的
的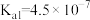 ,
, ;
;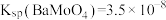 ;
;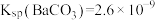 ;该工艺中,
;该工艺中,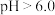 时,溶液中
时,溶液中 元素以
元素以 的形态存在。
的形态存在。“沉钼”中,
 为7.0。
为7.0。生成
 的离子方程式为
的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某学校化学兴趣小组在课外活动中,对某工厂的废液进行了多次检测,其中两次检测结果如表所示,请回答下列问题:
(1)两次检测结果中仅有一次是正确的,第_______ 次检测结果不正确。
(2)在检测时,为了检验溶液中是否存在 、
、 和
和 ,进行以下实验:
,进行以下实验:
①向溶液中滴加过量的_______ (填化学式)溶液,其目的是检验 并将其除去;
并将其除去;
②往①的溶液中加入过量的_______ (填化学式)溶液,其目的是检验并除去_______ (填离子符号);发生反应的离子方程式为_______ ;
③取②中混合物过滤,再向滤液中加入_______ (填化学式)溶液,发生反应的离子方程式为_______ 。
| 检测次数 | 溶液中检测出的离子 |
| 第I次 |  、 、 、 、 、 、 、 、 、 、 |
| 第Ⅱ次 |  、 、 、 、 、 、 、 、 |
(1)两次检测结果中仅有一次是正确的,第
(2)在检测时,为了检验溶液中是否存在
 、
、 和
和 ,进行以下实验:
,进行以下实验:①向溶液中滴加过量的
 并将其除去;
并将其除去;②往①的溶液中加入过量的
③取②中混合物过滤,再向滤液中加入
您最近一年使用:0次



