在加热条件下,用MnO2与足量浓盐酸反应,制得氯气1.12L(标况下),已知反应后溶液体积为50mL。试计算:
(1)写出该反应的化学方程式_______ ;
(2)理论上需要消耗MnO2的质量为_______ ;
(3)若将上述反应后的溶液稀释至250mL,则稀释后的溶液中MnCl2的物质的量浓度为_____ 。
(1)写出该反应的化学方程式
(2)理论上需要消耗MnO2的质量为
(3)若将上述反应后的溶液稀释至250mL,则稀释后的溶液中MnCl2的物质的量浓度为
更新时间:2022-11-14 19:11:08
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】光卤石是生产钾盐和镁盐的原料,易溶于水。某课外小组通过下列实验测定某光卤石试样(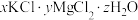 )的组成。
)的组成。
(1)取样品6.170g,加热至全部失去结晶水(杂质不分解),称得剩余固体的质量为4.010g,则样品中H2O的物质的量为___________ 。
(2)另取样品6.170g溶于水,加入过量氢氧化钠溶液,过滤、洗涤、干燥,得固体1.160g,试样中 的物质的量为
的物质的量为___________ 。
(3)另取样品6.170g溶于水,加入过量硝酸银溶液,过滤、洗涤、干燥,得固体8.610g,试样中 KCl的物质的量为___________ 。
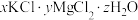 )的组成。
)的组成。(1)取样品6.170g,加热至全部失去结晶水(杂质不分解),称得剩余固体的质量为4.010g,则样品中H2O的物质的量为
(2)另取样品6.170g溶于水,加入过量氢氧化钠溶液,过滤、洗涤、干燥,得固体1.160g,试样中
 的物质的量为
的物质的量为(3)另取样品6.170g溶于水,加入过量硝酸银溶液,过滤、洗涤、干燥,得固体8.610g,试样中 KCl的物质的量为
您最近一年使用:0次
【推荐2】磷及部分重要化合物的相互转化如图所示。
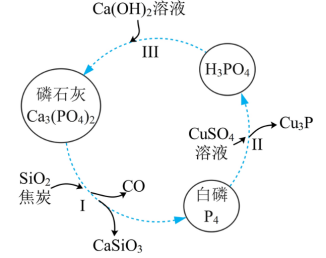
(1)不慎将白磷沾到皮肤上,可用0.2mol/L CuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol CuSO4所能氧化的白磷的物质的量为______ 。
(2)步骤Ⅲ中,反应物的比例不同可获得不同的产物,除Ca3(PO4)2外可能的产物还有______ 。
磷灰石是生产磷肥的原料,它的组成可以看作是Ca3(PO4)2、CaF2、CaSO4、CaCO3、SiO2的混合物,部分元素的分析结果如下(各元素均以氧化物形式表示):
(3)磷灰石中,碳元素的质量分数为______ %(保留两位小数)。
(4)取100g磷灰石粉末,加入足量的浓硫酸,并加热,钙元素全部以CaSO4的形式存在,可以得到CaSO4______ g(保留两位小数)。
(5)取m g 磷灰石粉末,用50.00mL混酸溶液(磷酸为0.5mol/L、硫酸为0.1mol/L)与其反应,结果Ca、S、P元素全部以CaSO4和Ca(H2PO4)2的形式存在,求m的值______ 。

(1)不慎将白磷沾到皮肤上,可用0.2mol/L CuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol CuSO4所能氧化的白磷的物质的量为
(2)步骤Ⅲ中,反应物的比例不同可获得不同的产物,除Ca3(PO4)2外可能的产物还有
磷灰石是生产磷肥的原料,它的组成可以看作是Ca3(PO4)2、CaF2、CaSO4、CaCO3、SiO2的混合物,部分元素的分析结果如下(各元素均以氧化物形式表示):
| 成分 | CaO | P2O5 | SO3 | CO2 |
| 质量分数(%) | 47.30 | 28.40 | 3.50 | 6.10 |
(3)磷灰石中,碳元素的质量分数为
(4)取100g磷灰石粉末,加入足量的浓硫酸,并加热,钙元素全部以CaSO4的形式存在,可以得到CaSO4
(5)取m g 磷灰石粉末,用50.00mL混酸溶液(磷酸为0.5mol/L、硫酸为0.1mol/L)与其反应,结果Ca、S、P元素全部以CaSO4和Ca(H2PO4)2的形式存在,求m的值
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】8.34g FeSO4·7H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。回答下列问题:
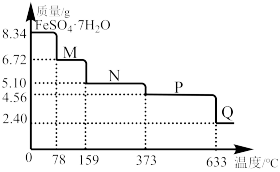
(1)试确定200℃时固体物质N的化学式___________ 。
(2)取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,试写出该反应的化学方程式___________ 。
(3)某兴趣小组用如图所示装置设计实验,验证(2)中生成的气态物质,并测定已分解的P的质量(不考虑装置内空气的影响)。
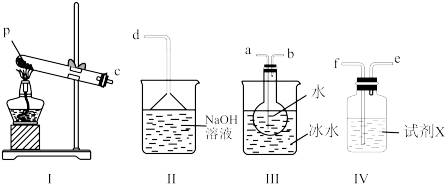
①试剂X的名称是___________ 。
②按气流方向连接仪器,用字母表示接口的连接顺序:c→___________ 。
③充分反应后,利用装置III中圆底烧瓶内混合物测定已分解的P的质量,其操作步骤为:第一步,向圆底烧瓶内逐滴加入BaCl2溶液,直至沉淀完全;第二步,过滤混合物,在过滤器上将沉淀洗净后,烘干并冷却至室温,称重;第三步,继续烘干冷却并称量,直至连续两次称量质量差不超过0. 1g为止。若最终所得沉淀质量为wg,则已分解的P的质量为___________ g.(填计算式)

(1)试确定200℃时固体物质N的化学式
(2)取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,试写出该反应的化学方程式
(3)某兴趣小组用如图所示装置设计实验,验证(2)中生成的气态物质,并测定已分解的P的质量(不考虑装置内空气的影响)。

①试剂X的名称是
②按气流方向连接仪器,用字母表示接口的连接顺序:c→
③充分反应后,利用装置III中圆底烧瓶内混合物测定已分解的P的质量,其操作步骤为:第一步,向圆底烧瓶内逐滴加入BaCl2溶液,直至沉淀完全;第二步,过滤混合物,在过滤器上将沉淀洗净后,烘干并冷却至室温,称重;第三步,继续烘干冷却并称量,直至连续两次称量质量差不超过0. 1g为止。若最终所得沉淀质量为wg,则已分解的P的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】现有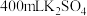 和
和 的混合溶液,将其分为两等份,向其中一份中加入1mol/L BaCl2溶液,至恰好不再产生沉淀,消耗50mL,将沉淀过滤、洗涤、干燥,称其质量为a g;向另一份溶液中加入铁片,充分反应后,取出铁片,洗涤、烘干,称其质量比原来减轻了0.56g。(已知Fe+2FeCl3=3FeCl2)试计算:
的混合溶液,将其分为两等份,向其中一份中加入1mol/L BaCl2溶液,至恰好不再产生沉淀,消耗50mL,将沉淀过滤、洗涤、干燥,称其质量为a g;向另一份溶液中加入铁片,充分反应后,取出铁片,洗涤、烘干,称其质量比原来减轻了0.56g。(已知Fe+2FeCl3=3FeCl2)试计算:
(1)a=___________ g;
(2)原溶液中 的物质的量浓度为
的物质的量浓度为___________  。
。
(3)在0.3 L由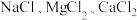 组成的混合液中,部分离子浓度大小如图所示,该混合液中
组成的混合液中,部分离子浓度大小如图所示,该混合液中 的物质的量为
的物质的量为___________ ;将该混合液加水稀释至体积为0.5 L,稀释后溶液中 的物质的量浓度为
的物质的量浓度为___________ 。

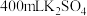 和
和 的混合溶液,将其分为两等份,向其中一份中加入1mol/L BaCl2溶液,至恰好不再产生沉淀,消耗50mL,将沉淀过滤、洗涤、干燥,称其质量为a g;向另一份溶液中加入铁片,充分反应后,取出铁片,洗涤、烘干,称其质量比原来减轻了0.56g。(已知Fe+2FeCl3=3FeCl2)试计算:
的混合溶液,将其分为两等份,向其中一份中加入1mol/L BaCl2溶液,至恰好不再产生沉淀,消耗50mL,将沉淀过滤、洗涤、干燥,称其质量为a g;向另一份溶液中加入铁片,充分反应后,取出铁片,洗涤、烘干,称其质量比原来减轻了0.56g。(已知Fe+2FeCl3=3FeCl2)试计算:(1)a=
(2)原溶液中
 的物质的量浓度为
的物质的量浓度为 。
。(3)在0.3 L由
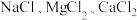 组成的混合液中,部分离子浓度大小如图所示,该混合液中
组成的混合液中,部分离子浓度大小如图所示,该混合液中 的物质的量为
的物质的量为 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】太空探索永无止境,探索浩瀚宇宙是全人类的共同梦想。回答下列问题:
(1)建造太空电梯的材料为单质碳。假设太空电梯重达
 ,则碳原子的物质的量为
,则碳原子的物质的量为(2)太阳阵闪是指当太阳内部温度升到
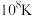 时,3个
时,3个 发生核聚变生成
发生核聚变生成 。
。 发生氦闪可生成
发生氦闪可生成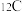 的质量为
的质量为(3)月球上有丰富的
 (摩尔质量为
(摩尔质量为 )气体核聚变发电燃料,我国每天用电量只需
)气体核聚变发电燃料,我国每天用电量只需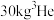 气体,则由
气体,则由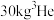 组成的气体在标准状况下所占的体积为
组成的气体在标准状况下所占的体积为(4)发射嫦娥四号用的是长征三号乙运载火箭,该火箭推进剂[燃料为
 和助燃剂为
和助燃剂为 ]共
]共 ,点燃时二者恰好反应,发生的反应为
,点燃时二者恰好反应,发生的反应为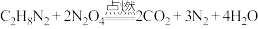 ,则其中燃料
,则其中燃料 的质量为
的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】MnO2又名黑锰矿,主要用于生产优质软磁铁氧体。MnO2的合成方法按制备工艺中所用原料的不同,分为固相合成和液相合成。已知:MnO2不溶于水,其中锰的价态有+2价,也可能有+3价和+4价。请回答下列问题:
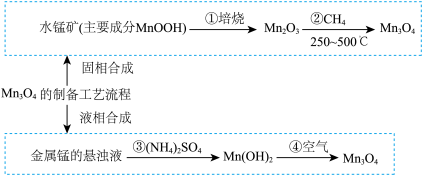
(1)若Mn3O4中锰的价态看作由+2和+4价组成,写出它由氧化物形成的表达式:_____
(2)MnOOH中锰的价态为________ 价,写出②的化学方程式:____ ;碱性锌锰干电池的电池反应为:Zn+2MnO2 + 2H2O=Zn(OH)2 + 2MnOOH,写出该电池正极的电极反应式______
(3)将(NH4)2SO4溶于水使锰的悬浊液显酸性,随即缓慢地产生气泡,试用相应的离子方程式解释原因____________ 。过滤出的Mn(OH)2需要洗涤,简要说明洗涤沉淀的操作过程:________ 。
(4)若③中收集到672mL(标准状况下)的H2,则理论上可以得到_________ g Mn3O4。

(1)若Mn3O4中锰的价态看作由+2和+4价组成,写出它由氧化物形成的表达式:
(2)MnOOH中锰的价态为
(3)将(NH4)2SO4溶于水使锰的悬浊液显酸性,随即缓慢地产生气泡,试用相应的离子方程式解释原因
(4)若③中收集到672mL(标准状况下)的H2,则理论上可以得到
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】84消毒液、ClO2是常见的含氯消毒剂。
资料:84消毒液中含氟微粒主要有ClO-、Cl-、HClO;相同浓度时,HClO的氧化性强于ClO-;ORP是反映物质的氧化一还原性,ORP值越大,氧化性越强。通常情况下,应将84消毒液原液稀释后使用;一般不用于衣服等纺织品的洗涤消毒。
(1)制备ClO2的一种反应为:2NaClO3+2NaCl+2H2SO4=2ClO2↑+Cl2↑+2Na2SO4+2H2O,用单线桥法标出其电子转移的方向和数目_______ 。
(2)取含次氯酸钠0.2mol·L-1的消毒液1mL,加水稀释至200mL,则稀释后次氯酸钠的物质的量浓度为_______ mol·L-1。
(3)为研究84消毒液的性质与使用条件,进行下列实验:
【实验1】向两支试管中分别加入2mL84消毒液,在试管l中加入2mL水,试管2中加入2mL白醋,再分别放入相同的红色纸片。观察到试管2中纸片褪色更快。
①实验中在试管l中加入2mL水的目的是_______ 。
②试管2中纸片褪色更快的原因是_______ 。
③如果实验中加浓盐酸,会有黄绿色气体产生,反应的离子方程式是_______ 。
【实验2】测定84消毒液在不同温度时ORP随时间的变化情况,结果如图所示。
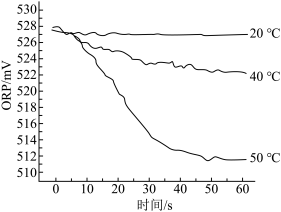
④实验表明,随温度升高,ORP值下降。50℃时ORP值下降较快的原因是_______ 。
资料:84消毒液中含氟微粒主要有ClO-、Cl-、HClO;相同浓度时,HClO的氧化性强于ClO-;ORP是反映物质的氧化一还原性,ORP值越大,氧化性越强。通常情况下,应将84消毒液原液稀释后使用;一般不用于衣服等纺织品的洗涤消毒。
(1)制备ClO2的一种反应为:2NaClO3+2NaCl+2H2SO4=2ClO2↑+Cl2↑+2Na2SO4+2H2O,用单线桥法标出其电子转移的方向和数目
(2)取含次氯酸钠0.2mol·L-1的消毒液1mL,加水稀释至200mL,则稀释后次氯酸钠的物质的量浓度为
(3)为研究84消毒液的性质与使用条件,进行下列实验:
【实验1】向两支试管中分别加入2mL84消毒液,在试管l中加入2mL水,试管2中加入2mL白醋,再分别放入相同的红色纸片。观察到试管2中纸片褪色更快。
①实验中在试管l中加入2mL水的目的是
②试管2中纸片褪色更快的原因是
③如果实验中加浓盐酸,会有黄绿色气体产生,反应的离子方程式是
【实验2】测定84消毒液在不同温度时ORP随时间的变化情况,结果如图所示。

④实验表明,随温度升高,ORP值下降。50℃时ORP值下降较快的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据所学知识,回答下列问题:
(1)分类在化学学习中起着非常重要的作用,下列分类标准合理的是___ (填标号)。
(2)现有以下六种物质:①NaCl溶液,②Cl2,③HClO,④蔗糖,⑤NaOH固体,⑥稀硫酸。其中属于电解质的是___ (填序号)。
(3)化学计量是化学定量研究的基础。
①3.01×1023个CH4分子的物质的量为___ mol,质量为___ g。
②将30mL0.5mol•L-1NaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为___ mol•L-1。
③等质量的H2S和NH3,其分子个数比N(H2S):N(NH3)=___ ,标准状况下气体的体积比V(H2S):V(NH3)= ___ 。
(4)食品干燥剂的作用是降低食品包装袋中的温度,防止食品变质腐败。CaO、CaCl2均可用作食品干燥剂。
①CaO吸水能力强的原理为____ (填化学方程式),CaO的保存方法为___ 。
②检验CaCl2溶液中Cl-存在的具体操作及现象为___ 。
(1)分类在化学学习中起着非常重要的作用,下列分类标准合理的是
| A.根据物质溶于水后形成的溶液呈碱性,可将此类物质归类为碱 |
| B.根据物质能否导电,将物质分为电解质和非电解质 |
| C.根据反应中是否有电子的转移,将化学反应分为氧化还原反应和非氧化还原反应 |
| D.根据分散系中分散质粒子的直径大小,将分散系分为溶液,胶体和浊液 |
(3)化学计量是化学定量研究的基础。
①3.01×1023个CH4分子的物质的量为
②将30mL0.5mol•L-1NaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为
③等质量的H2S和NH3,其分子个数比N(H2S):N(NH3)=
(4)食品干燥剂的作用是降低食品包装袋中的温度,防止食品变质腐败。CaO、CaCl2均可用作食品干燥剂。
①CaO吸水能力强的原理为
②检验CaCl2溶液中Cl-存在的具体操作及现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求填写下列空白
KOH是实验室里常用的一种试剂,实验室里配制KOH溶液时,既可以使用浓溶液稀释法配制也可以使用固体KOH来配制。实验室现在需要配制480mL 2.0mol/L的KOH溶液,请回答下列问题:
(1)若用固体KOH配制,则需用托盘天平称取KOH的质量_______ g
(2)若用10mol/L KOH的浓溶液来配制,则使用量筒量取该溶液的体积为_______ mL
(3)容量瓶上需标有以下五项中的_______ 。
①温度②浓度③容量④压强⑤刻度线
(4)浓溶液稀释法中配制KOH过程中,若使用量筒量取一定体积的浓KOH溶液时,读数时俯视刻度线,则所配制溶液的物质的量浓度会_______ (填偏高、偏低或不变)
(5)取出配制好的KOH溶液100mL,与标准状况下4.48L CO2充分反应,请写出该反应的化学方程式_______ 。
KOH是实验室里常用的一种试剂,实验室里配制KOH溶液时,既可以使用浓溶液稀释法配制也可以使用固体KOH来配制。实验室现在需要配制480mL 2.0mol/L的KOH溶液,请回答下列问题:
(1)若用固体KOH配制,则需用托盘天平称取KOH的质量
(2)若用10mol/L KOH的浓溶液来配制,则使用量筒量取该溶液的体积为
(3)容量瓶上需标有以下五项中的
①温度②浓度③容量④压强⑤刻度线
(4)浓溶液稀释法中配制KOH过程中,若使用量筒量取一定体积的浓KOH溶液时,读数时俯视刻度线,则所配制溶液的物质的量浓度会
(5)取出配制好的KOH溶液100mL,与标准状况下4.48L CO2充分反应,请写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】完成下列化学用语填空:
(1)水分子的电子式_______ ;S2-的离子结构示意图_______ 。
(2)短周期元素原子半径最大的元素(不考虑稀有气体)_______ (用元素符号表示)。
(3)实验室制氯气的离子方程式_______ 。
(4)铜与稀硝酸反应,装置上部有红棕色气体产生的原因(用化学方程式表示)_______ 。
(5)盛放NaOH溶液的试剂瓶为什么不能用玻璃瓶塞(用化学方程式表示)_______ 。
(1)水分子的电子式
(2)短周期元素原子半径最大的元素(不考虑稀有气体)
(3)实验室制氯气的离子方程式
(4)铜与稀硝酸反应,装置上部有红棕色气体产生的原因(用化学方程式表示)
(5)盛放NaOH溶液的试剂瓶为什么不能用玻璃瓶塞(用化学方程式表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】完成下列问题
(1)18世纪70年代,瑞典化学家舍勒将软锰矿(主要成分为 )与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体。该反应的化学方程式为
)与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体。该反应的化学方程式为_______ ,该反应中氧化剂和还原剂的个数比为_______ ,该反应每生成2个 转移
转移_______ 个电子。
(2)某同学拟用该原理按如下装置制备并收集纯净的 ,在虚线框内选用的发生装置
,在虚线框内选用的发生装置_______ (填“甲”“乙”或“丙”)。 中除
中除 外还含有
外还含有_______ (填化学式),试剂X是_______ 。
(4)通过大量实验证明, 与
与 反应生成HClO,HClO能杀菌消毒。可利用数字化实验探究HClO的化学性质,用强光照射氯水,得到氯水的pH随时间变化如
反应生成HClO,HClO能杀菌消毒。可利用数字化实验探究HClO的化学性质,用强光照射氯水,得到氯水的pH随时间变化如_______ 所示(图1或图2),氯离子浓度随时间变化如_______ 所示(图1或图2),请在图3中画出氧气的体积随时间变化的趋势图_______ 。
(1)18世纪70年代,瑞典化学家舍勒将软锰矿(主要成分为
 )与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体。该反应的化学方程式为
)与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体。该反应的化学方程式为 转移
转移(2)某同学拟用该原理按如下装置制备并收集纯净的
 ,在虚线框内选用的发生装置
,在虚线框内选用的发生装置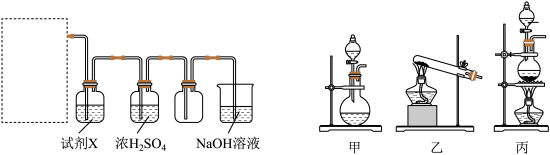
 中除
中除 外还含有
外还含有(4)通过大量实验证明,
 与
与 反应生成HClO,HClO能杀菌消毒。可利用数字化实验探究HClO的化学性质,用强光照射氯水,得到氯水的pH随时间变化如
反应生成HClO,HClO能杀菌消毒。可利用数字化实验探究HClO的化学性质,用强光照射氯水,得到氯水的pH随时间变化如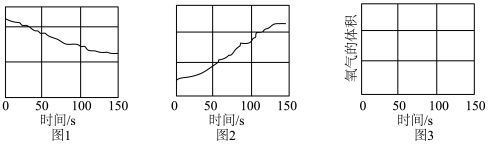
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氧化还原反应在生产、生活和生命活动中起着十分重要的作用.例如,饮用水处理和污水净化问题中就广泛应用了氧化还原反应的原理.
Ⅰ.高铁酸钠 是一种新型绿色消毒剂,主要用于饮用水处理.工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用化学方程式表示为:
是一种新型绿色消毒剂,主要用于饮用水处理.工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用化学方程式表示为:
(1)在 中,
中, 的化合价为
的化合价为___________ 价;上述反应中,每生成 ,有
,有___________  电子转移.
电子转移.
(2)制备 的另外一种方法是在碱性条件下用
的另外一种方法是在碱性条件下用 和
和 反应,请配平下列离子方程式:
反应,请配平下列离子方程式:_____
__ ____
____ _____
_____ ____
____ _____
_____ _____
_____
Ⅱ.含氯消毒剂在自来水净化过程中也起到了重要作用.
(3)很多自来水厂用氯气来杀菌、消毒,实验室不能用自来水配制硝酸银溶液,用离子方程式表示其原因___________ .实验室常用浓盐酸与二氧化锰反应来制取 ,请写出反应的化学方程式
,请写出反应的化学方程式___________ .
(4)亚氯酸钠 是一种高效的漂白剂和氧化剂,其制备方法如下:
是一种高效的漂白剂和氧化剂,其制备方法如下: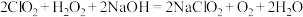
根据氧化剂的氧化性强于氧化产物这一规律,从上述反应中可知氧化性_________ >__________;
(5)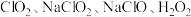 都常被用作消毒剂,上述物质消毒效率最高的是___________(填序号).(已知:消毒效率是以单位物质的量的物质得电子的数目多少表示,得电子越多效率越高)
都常被用作消毒剂,上述物质消毒效率最高的是___________(填序号).(已知:消毒效率是以单位物质的量的物质得电子的数目多少表示,得电子越多效率越高)
Ⅰ.高铁酸钠
 是一种新型绿色消毒剂,主要用于饮用水处理.工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用化学方程式表示为:
是一种新型绿色消毒剂,主要用于饮用水处理.工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用化学方程式表示为:
(1)在
 中,
中, 的化合价为
的化合价为 ,有
,有 电子转移.
电子转移.(2)制备
 的另外一种方法是在碱性条件下用
的另外一种方法是在碱性条件下用 和
和 反应,请配平下列离子方程式:
反应,请配平下列离子方程式:__
 ____
____ _____
_____ ____
____ _____
_____ _____
_____
Ⅱ.含氯消毒剂在自来水净化过程中也起到了重要作用.
(3)很多自来水厂用氯气来杀菌、消毒,实验室不能用自来水配制硝酸银溶液,用离子方程式表示其原因
 ,请写出反应的化学方程式
,请写出反应的化学方程式(4)亚氯酸钠
 是一种高效的漂白剂和氧化剂,其制备方法如下:
是一种高效的漂白剂和氧化剂,其制备方法如下: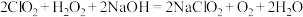
根据氧化剂的氧化性强于氧化产物这一规律,从上述反应中可知氧化性
(5)
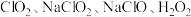 都常被用作消毒剂,上述物质消毒效率最高的是___________(填序号).(已知:消毒效率是以单位物质的量的物质得电子的数目多少表示,得电子越多效率越高)
都常被用作消毒剂,上述物质消毒效率最高的是___________(填序号).(已知:消毒效率是以单位物质的量的物质得电子的数目多少表示,得电子越多效率越高)A. | B. | C. | D. |
您最近一年使用:0次



