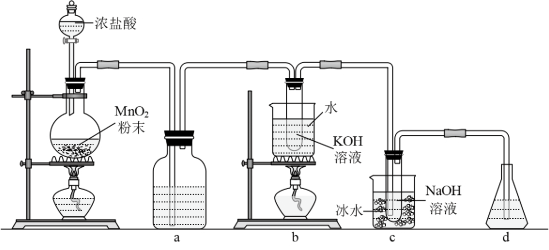
氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备KClO3和NaClO。
已知:氯气和碱反应在室温下生成氯化物和次氯酸盐,温度升高时主要产物是氯化物和氯酸盐,氯气和碱的反应释放热量。
回答下列问题:
(1)盛放浓盐酸的仪器名称是_______ ,a中的试剂为_______ 。
(2)c中化学反应的离子方程式是_______ ,采用冰水浴冷却的目的是_______ 。
(3)d的作用是_______ ,下列可选用的最佳试剂为_______ (填标号)。
A.KI溶液 B.饱和食盐水 C.Ca(OH)2溶液 D.浓H2SO4
(4)反应结束后,取出b中试管,经冷却结晶、_______ 、_______ 、干燥,得到KClO3晶体。(填写操作名称)
(5)称取上述制备出的KClO3粗产品3.0g并加入适量MnO2再称量后加热至质量不再改变(假设杂质受热不分解),测得固体总质量减轻0.96g,则制备的粗产品中氯酸钾纯度为_______ 。(保留到小数点后1位)
(6)反应结束后,c试管中溶液具有消毒、漂白作用,向c中通入或加入下列物质,能使其消毒、漂白效果明显增强的有_______。
已知:氯气和碱反应在室温下生成氯化物和次氯酸盐,温度升高时主要产物是氯化物和氯酸盐,氯气和碱的反应释放热量。

回答下列问题:
(1)盛放浓盐酸的仪器名称是
(2)c中化学反应的离子方程式是
(3)d的作用是
A.KI溶液 B.饱和食盐水 C.Ca(OH)2溶液 D.浓H2SO4
(4)反应结束后,取出b中试管,经冷却结晶、
(5)称取上述制备出的KClO3粗产品3.0g并加入适量MnO2再称量后加热至质量不再改变(假设杂质受热不分解),测得固体总质量减轻0.96g,则制备的粗产品中氯酸钾纯度为
(6)反应结束后,c试管中溶液具有消毒、漂白作用,向c中通入或加入下列物质,能使其消毒、漂白效果明显增强的有_______。
| A.NH3 | B.CO2 | C.饱和食盐水 | D.NaOH溶液 |
更新时间:2022-11-11 18:11:50
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某化学兴趣小组为探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),请按要求回答问题:
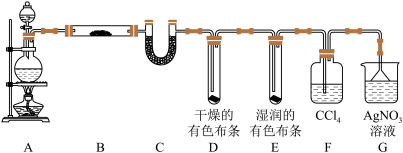
(1)如图A装置中分液漏斗盛有浓盐酸,圆底烧瓶中的固体是二氯化锰。写出A中发生的化学反应方程式___________ 。并用双线桥法表示该反应的电子转移情况。
(2)①装置B中盛有无水硫酸铜,其中的现象是___________ 。
②装置C的作用是___________ 。
③装置D、E出现不同的现象说明___________ 。
(3)装置F吸收反应生成的Cl2,装置G验证HCl挥发出来。乙同学认为此处有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种,为了确保实验结论的可靠性,证明最终通入G中的气体只有一种,乙同学提出在F、G之间再增加一个装置。你认为该装管中应该盛放___________ (填写试剂或用品名称)。
(4)实验室也可用高锰酸钾和浓盐酸常温下反应制取氯气,写出该反应的化学方程式:___________ 。

(1)如图A装置中分液漏斗盛有浓盐酸,圆底烧瓶中的固体是二氯化锰。写出A中发生的化学反应方程式
(2)①装置B中盛有无水硫酸铜,其中的现象是
②装置C的作用是
③装置D、E出现不同的现象说明
(3)装置F吸收反应生成的Cl2,装置G验证HCl挥发出来。乙同学认为此处有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种,为了确保实验结论的可靠性,证明最终通入G中的气体只有一种,乙同学提出在F、G之间再增加一个装置。你认为该装管中应该盛放
(4)实验室也可用高锰酸钾和浓盐酸常温下反应制取氯气,写出该反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】 是一种重要的化工原料,常用于生产次氯酸钠、漂白粉、溴素、三氯化磷等无机化工产品。回答下列问题:
是一种重要的化工原料,常用于生产次氯酸钠、漂白粉、溴素、三氯化磷等无机化工产品。回答下列问题:
(1)甲同学在实验室欲制备一瓶纯净的 ,装置如图所示。
,装置如图所示。
①装置的连接顺序为___________ (按气流方向,用小写字母表示)。

②检验装置A气密性的具体操作是___________ 。
③装置D中所装试剂为___________ 。
(2)乙同学结合甲同学的装置,又添加一些装置(如下图),在实验室利用 和
和 在活性炭催化作用下制取亚硫酰氯
在活性炭催化作用下制取亚硫酰氯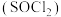 。亚硫酰氯是重要的化工试剂,易水解。
。亚硫酰氯是重要的化工试剂,易水解。

①H仪器的名称为___________ 。
②G仪器的进水口是___________ (填“a”或“b”)。
③F仪器的作用是___________ 。
(3)已知 具有还原性,
具有还原性, 和
和 能发生氧化还原反应。丙同学做以下实验:取少量
能发生氧化还原反应。丙同学做以下实验:取少量 和
和 反应后的混合物于试管中,加水充分溶解后……丙同学猜想二者能否发生氧化还原反应,接下来的实验操作和现象都正确且能验证丙同学猜想的是___________(填字母序号)。
反应后的混合物于试管中,加水充分溶解后……丙同学猜想二者能否发生氧化还原反应,接下来的实验操作和现象都正确且能验证丙同学猜想的是___________(填字母序号)。
 是一种重要的化工原料,常用于生产次氯酸钠、漂白粉、溴素、三氯化磷等无机化工产品。回答下列问题:
是一种重要的化工原料,常用于生产次氯酸钠、漂白粉、溴素、三氯化磷等无机化工产品。回答下列问题:(1)甲同学在实验室欲制备一瓶纯净的
 ,装置如图所示。
,装置如图所示。①装置的连接顺序为

②检验装置A气密性的具体操作是
③装置D中所装试剂为
(2)乙同学结合甲同学的装置,又添加一些装置(如下图),在实验室利用
 和
和 在活性炭催化作用下制取亚硫酰氯
在活性炭催化作用下制取亚硫酰氯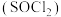 。亚硫酰氯是重要的化工试剂,易水解。
。亚硫酰氯是重要的化工试剂,易水解。
①H仪器的名称为
②G仪器的进水口是
③F仪器的作用是
(3)已知
 具有还原性,
具有还原性, 和
和 能发生氧化还原反应。丙同学做以下实验:取少量
能发生氧化还原反应。丙同学做以下实验:取少量 和
和 反应后的混合物于试管中,加水充分溶解后……丙同学猜想二者能否发生氧化还原反应,接下来的实验操作和现象都正确且能验证丙同学猜想的是___________(填字母序号)。
反应后的混合物于试管中,加水充分溶解后……丙同学猜想二者能否发生氧化还原反应,接下来的实验操作和现象都正确且能验证丙同学猜想的是___________(填字母序号)。| A.滴加几滴KSCN溶液,溶液变为红色 |
B.滴加几滴 溶液,有白色沉淀生成 溶液,有白色沉淀生成 |
C.加入少量稀硝酸,再滴加几滴 溶液,有白色沉淀生成 溶液,有白色沉淀生成 |
D.滴加几滴酸性 溶液,紫红色消失 溶液,紫红色消失 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某化学兴趣小组设计了如图装置,该装置能制取 ,并进行相关性质实验,且可利用装置G储存多余的氯气。
,并进行相关性质实验,且可利用装置G储存多余的氯气。
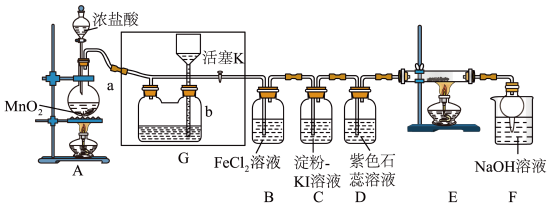
(1)A中发生反应的化学方程式为___________ 。
(2)①实验开始时,打开分液漏斗旋塞和活塞K。先点燃___________ (填“A”或“E”)处酒精灯。
②在装置D中能看到的实验现象是___________ 。
③由C中出现的现象可以判断两种非金属单质的氧化性强弱为___________ 。
④装置F中发生反应的离子方程式为___________ 。
(3)装置F中球形干燥管的作用是___________ 。
(4)储气瓶b内盛放的试剂是___________ 。
 ,并进行相关性质实验,且可利用装置G储存多余的氯气。
,并进行相关性质实验,且可利用装置G储存多余的氯气。
(1)A中发生反应的化学方程式为
(2)①实验开始时,打开分液漏斗旋塞和活塞K。先点燃
②在装置D中能看到的实验现象是
③由C中出现的现象可以判断两种非金属单质的氧化性强弱为
④装置F中发生反应的离子方程式为
(3)装置F中球形干燥管的作用是
(4)储气瓶b内盛放的试剂是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某兴趣小组利用下列装置,进行与氯气相关的实验。
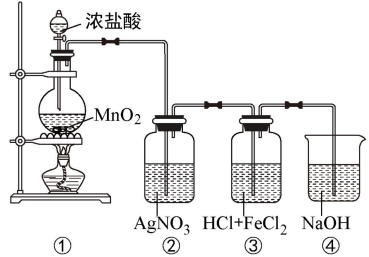
(1)写出实验中盛放MnO2的仪器名称___________ 。
(2)装置③中反应的离子方程式:___________ 。
(3)装置②中出现白色沉淀,据此现象能否推测装置①中生成Cl2,请说明理由___________ 。

(1)写出实验中盛放MnO2的仪器名称
(2)装置③中反应的离子方程式:
(3)装置②中出现白色沉淀,据此现象能否推测装置①中生成Cl2,请说明理由
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某学习小组欲制备氯水和漂白粉,并利用所制溶液进行相关实验探究。实验装置如图所示。回答有关问题。
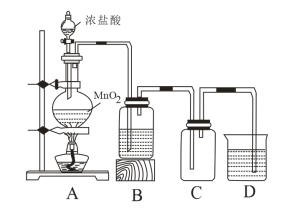
(1)装置A中生成氯气的离子方程式为___________ 。
(2)装置B的作用是吸收氯气带出的HCl气体,所装的试剂为___________ 。装置C用于制备氯水,应装入的试剂是___________ ,装置D中盛有___________ ,可以在防止___________ 的同时制备漂白粉。
(3)小组同学用上述实验中得到的氯水进行如下实验
根据该小组的实验报告,回答下列问题:
①实验i中发生反应的离子方程式为___________ 。
②实验ii的结论是否严谨?___________ (填“是”或“否”),理由是___________ 。
③实验iii中溶液红色褪去的原因,除了酸碱中和反应外,还有一种可能:___________ 。如要证明到底是什么原因使溶液褪色,还需进一步设计实验验证。

(1)装置A中生成氯气的离子方程式为
(2)装置B的作用是吸收氯气带出的HCl气体,所装的试剂为
(3)小组同学用上述实验中得到的氯水进行如下实验
| 实验序号 | 试剂和操作 | 实验现象 | 结论 |
| i | 在4mLNaBr溶液中加入1mL氯水 | 溶液变黄色 | 氯气的氧化性比溴强 |
| ii | 在4mLKI溶液中加入实验i所得黄色溶液 | 溶液变为棕黄色 | 溴的氧化性比碘强 |
| iii | 在滴有酚酞的NaOH溶液中滴加氯水 | 当氯水滴到一定量时,溶液红色突然褪去 | 氯水显酸性 |
①实验i中发生反应的离子方程式为
②实验ii的结论是否严谨?
③实验iii中溶液红色褪去的原因,除了酸碱中和反应外,还有一种可能:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】I.某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表。
请你帮助该同学整理并完成实验报告:
实验目的:探究同周期元素的金属性和非金属性的递变规律。
实验用品:
仪器:①试管 ②酒精灯 ③胶头滴管 ④试管夹⑤镊子⑥小刀⑦玻璃片⑧砂纸 ⑨烧杯等。
药品:钠、镁带、铝条、2 mol·L-1的盐酸、新制的氯水、饱和的H2S溶液等。
(1)实验内容:(填写与实验方案相对应的实验现象)
①________ ②________ ③________ ④________ ⑤________ (用A-E表示)
写出③的离子方程式_____________________________________ 。
(2)实验结论:________________________________________ 。
Ⅱ. 实验室利用如图装置进行中和热的测定,请回答下列问题:
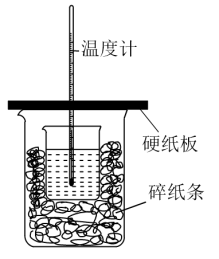
(3)从实验装置上看,图中尚缺少一种玻璃仪器是______________________ 。
(4)做1次完整的中和热测定实验,温度计需使用__________________ 次。
(5)某同学为了省去清洗温度计的麻烦,建议实验时使用两支温度计分别测量酸和碱的温度,你是否同意该同学的观点,为什么?____________________________________ 。
| 实验方案 | 实验现象 |
| ①用砂纸擦后的镁带与沸水反应,再向反应后溶液中滴加酚酞 | (A)浮于水面,熔成一个小球,在水面上无定向移动,随之消失,溶液变红色 |
| ②向新制的H2S饱和溶液中滴加新制的氯水 | (B)产生气体,可在空气中燃烧,溶液变成浅红色 |
| ③钠与滴有酚酞试液的冷水反应 | (C)反应不十分强烈,产生的气体可以在空气中燃烧 |
| ④镁带与2 mol·L-1的盐酸反应 | (D)剧烈反应,产生可燃性气体 |
| ⑤铝条与2 mol·L-1的盐酸反应 | (E) 生成淡黄色沉淀 |
实验目的:探究同周期元素的金属性和非金属性的递变规律。
实验用品:
仪器:①试管 ②酒精灯 ③胶头滴管 ④试管夹⑤镊子⑥小刀⑦玻璃片⑧砂纸 ⑨烧杯等。
药品:钠、镁带、铝条、2 mol·L-1的盐酸、新制的氯水、饱和的H2S溶液等。
(1)实验内容:(填写与实验方案相对应的实验现象)
①
写出③的离子方程式
(2)实验结论:
Ⅱ. 实验室利用如图装置进行中和热的测定,请回答下列问题:

(3)从实验装置上看,图中尚缺少一种玻璃仪器是
(4)做1次完整的中和热测定实验,温度计需使用
(5)某同学为了省去清洗温度计的麻烦,建议实验时使用两支温度计分别测量酸和碱的温度,你是否同意该同学的观点,为什么?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验室拟用浓盐酸与二氧化锰反应制取纯净的氯气。并验证氯气的性质。
(Ⅰ)制取氯气:
(1)按气体从左到右流动的方向将下列装置进行连接(填字母〉,H→_____ 、_______ → _______ 。广口瓶Ⅱ中的试剂为________ 。
(2)仪器N的名称是_______ ;M是连通上下玻璃仪器的橡胶管,其目的是__________________ ;写出圆底烧瓶中发生反应的离子方程式_________________ 。
(3)连接好仪器后,上述装置存在一个明显的缺陷,你的改进方法是_______________ 。
(Ⅱ)验证氯气的性质:将从上述发生装置H处导出的气体依次经过下列装置验证氯气的性质(其他相关装置已略去)
(4)丁中出现的现象是__________________ ,该反应证明了氯气的____________ 性。
(5)证明HClO具有漂白性的实验现象是__________________ ,甲中的试剂是_________ 。
(Ⅰ)制取氯气:
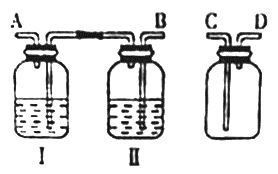
(1)按气体从左到右流动的方向将下列装置进行连接(填字母〉,H→

(2)仪器N的名称是
(3)连接好仪器后,上述装置存在一个明显的缺陷,你的改进方法是
(Ⅱ)验证氯气的性质:将从上述发生装置H处导出的气体依次经过下列装置验证氯气的性质(其他相关装置已略去)

(4)丁中出现的现象是
(5)证明HClO具有漂白性的实验现象是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】①A、B、C、D四种物质均含有元素X,有的还可能含有元素Y或者元素Z。元素Y、X、Z的相对原子质量依次递增。
②X在A、B、C、D中的化合价分别为0价、-1价、+1价、+5价。
③室温下单质A与某种常见一元强碱溶液反应,可得到B和C。
④化合物D受热催化分解,可制得元素Y的单质。
请完成下列问题:
(1)写出元素X、Y、Z的元素符号:X.______ ;Y.______ ;Z.______ 。
(2)写出A、B、C、D的化学式:A.______ ;B.______ ;C.______ ; D.______ 。
(3)写出③中反应的化学方程式:___________ 。
(4)写出④中反应的化学方程式:___________ 。
②X在A、B、C、D中的化合价分别为0价、-1价、+1价、+5价。
③室温下单质A与某种常见一元强碱溶液反应,可得到B和C。
④化合物D受热催化分解,可制得元素Y的单质。
请完成下列问题:
(1)写出元素X、Y、Z的元素符号:X.
(2)写出A、B、C、D的化学式:A.
(3)写出③中反应的化学方程式:
(4)写出④中反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式: F_____________ 。
(2)反应⑤的离子方程式为_______________________________ 。
(3)反应①-⑦的7个反应属于氧化还原反应反应的有 (填选项代号)。
(4)向纯碱溶液中通入气体乙,可制得某种生产生活中常用的漂白、消毒的物质,同时有小苏打生成。该反应的化学方程式为___________ 。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式: F
(2)反应⑤的离子方程式为
(3)反应①-⑦的7个反应属于氧化还原反应反应的有 (填选项代号)。
| A.①②④⑤⑥ | B.②③④⑥⑦ | C.①②③④⑤⑦ | D.全部 |
(4)向纯碱溶液中通入气体乙,可制得某种生产生活中常用的漂白、消毒的物质,同时有小苏打生成。该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】用中和滴定法测定某烧碱样品的纯度。根据实验回答下列问题:
(1)准确称量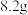 含有少量中性易溶杂质的样品,配成
含有少量中性易溶杂质的样品,配成 待测溶液。称量时,样品可放在
待测溶液。称量时,样品可放在__________ (填仪器名称)称量。
(2)滴定时,用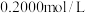 的盐酸来滴定待测液,用
的盐酸来滴定待测液,用__________ (填仪器名称)进行滴定操作,可选用__________ 作指示剂,滴定过程中,眼睛应注视__________ ,滴定终点的现象是__________ 。
(3)根据下表数据,计算被测烧碱溶液的浓度是__________  ,烧碱样品的纯度是
,烧碱样品的纯度是__________ (保留4位有效数字)。
(4)下列关于中和滴定的说法错误的是__________。
(5)叙述排碱式滴定管尖嘴内的气泡,正确操作方法__________ 。
(1)准确称量
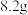 含有少量中性易溶杂质的样品,配成
含有少量中性易溶杂质的样品,配成 待测溶液。称量时,样品可放在
待测溶液。称量时,样品可放在(2)滴定时,用
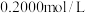 的盐酸来滴定待测液,用
的盐酸来滴定待测液,用(3)根据下表数据,计算被测烧碱溶液的浓度是
 ,烧碱样品的纯度是
,烧碱样品的纯度是滴定次数 | 待测溶液体积(mL) | 标准酸液体积 | |
滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
第一次 | 10.00 | 0.40 | 20.50 |
第二次 | 10.00 | 4.10 | 24.00 |
第三次 | 10.00 | 0.02 | 22.20 |
| A.中和滴定操作中所需标准溶液越浓越好 |
| B.中和滴定实验时,滴定管、锥形瓶均用待测液润洗 |
| C.滴定前滴定管中有气泡,滴定后滴定管中无气泡,则滴定结果偏高 |
| D.用碱式滴定管取待测液时,调整好初始值后放液,放液后俯视刻度线,滴定结果偏高 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】过氧化钙(CaO2)微溶于水,可作医用防腐剂、消毒剂,以下是制备CaO2的一种方法。

回答下列问题:
(1)步骤Ⅰ中反应的离子方程式是___________ 。
(2)步骤Ⅱ中反应的化学方程式是:___________ = CaO2·8H2O↓ + 2NH4Cl,反应在冰水浴中进行,是为了防止NH3·H2O挥发、___________ (答1条即可)。
(3)待CaO2·8H2O固体结晶析出后通过___________ (填操作)分离。
(4)CaO2中阴阳离子的个数比为___________ ,其与水缓慢反应,常用作鱼塘的供氧剂,其反应的化学方程式是___________ 。CaO2还可用于长途运输鱼苗,这体现了CaO2的___________ (填字母)性质。
a.可缓慢供氧 b.能吸收鱼苗呼出的CO2 c.能潮解 d.可抑菌
(5)CaO2久置于空气中会生成CaCO3.为测定某CaO2样品的纯度,取10 g样品加入足量稀盐酸,测得生成CO2的质量为2.2 g,则样品中CaO2的质量分数为___________ 。

回答下列问题:
(1)步骤Ⅰ中反应的离子方程式是
(2)步骤Ⅱ中反应的化学方程式是:
(3)待CaO2·8H2O固体结晶析出后通过
(4)CaO2中阴阳离子的个数比为
a.可缓慢供氧 b.能吸收鱼苗呼出的CO2 c.能潮解 d.可抑菌
(5)CaO2久置于空气中会生成CaCO3.为测定某CaO2样品的纯度,取10 g样品加入足量稀盐酸,测得生成CO2的质量为2.2 g,则样品中CaO2的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某同学将一定浓度的Na2CO3溶液加入CuSO4溶液中,发现生成了沉淀,其对沉淀的成分进行如下探究:
[提出假设]
假设1:沉淀是CuCO3;
假设2:(1)________________________________________ ;
假设3沉淀是CuCO3和Cu(OH)2的混合物。
[验证假设]
(2)如果假设1成立,则反应的离子方程式为_______________________________
(3)用离子方程式表示假设3中有Cu(OH)2生成的理论依据:_________________________
(4)为证明以上哪种假设成立,该同学用如图装置测定沉淀样品中CuCO3的质量分数:
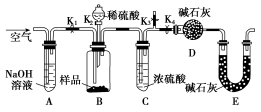
①实验时的步骤依次为a.打开K1、K3,关闭K2、K4,通入过量空气;b.关闭K1、K3,打开K2、K4,充分反应;c.打开K1、K4,关闭K2、K3,通入过量空气,若未进行步骤a,将使测定结果________ (填“偏低”“偏高”或“无影响”)。实验结束时通入过量空气的目的是_________________ 。
②若沉淀样品的质量为10.0 g,装置D的质量增加了2.2 g,则沉淀中CuCO3的质量分数为__________ 。
③由以上实验可知,假设____________ 成立。
[提出假设]
假设1:沉淀是CuCO3;
假设2:(1)
假设3沉淀是CuCO3和Cu(OH)2的混合物。
[验证假设]
(2)如果假设1成立,则反应的离子方程式为
(3)用离子方程式表示假设3中有Cu(OH)2生成的理论依据:
(4)为证明以上哪种假设成立,该同学用如图装置测定沉淀样品中CuCO3的质量分数:

①实验时的步骤依次为a.打开K1、K3,关闭K2、K4,通入过量空气;b.关闭K1、K3,打开K2、K4,充分反应;c.打开K1、K4,关闭K2、K3,通入过量空气,若未进行步骤a,将使测定结果
②若沉淀样品的质量为10.0 g,装置D的质量增加了2.2 g,则沉淀中CuCO3的质量分数为
③由以上实验可知,假设
您最近一年使用:0次



