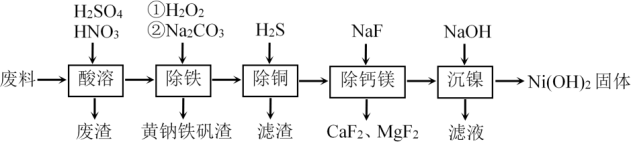
氢氧化镍[Ni(OH)2]常用于制备金属镍及镍的重要化合物。一种用铁镍合金废料(还含有少量铜、钙、镁、硅的氧化物)制备纯度较高氢氧化镍的工艺流程如图:
已知:H2S的电离常数K1=1.3×10-7,K2=7.1×10-15;Ksp[CuS]=6.0×10-36;Ksp[Ni(OH)2]=1.0×10-15.6。
回答下列问题:
(1)合金中的镍难溶于稀硫酸,“酸溶”时除了加入稀硫酸,还要边搅拌边缓慢加入稀硝酸,还原产物为N2,金属镍溶解的离子方程式是_____ 。
(2)“除铁”加入Na2CO3时,生成黄钠铁矾(NaFe3(SO4)2(OH)6)的离子方程式是____ ;“除铁”时,将“铁”转化成颗粒较大的黄钠铁矾沉淀对后续操作较为有利,原因是____ 。
(3)“除铜”时,反应的离子方程式为H2S+Cu2+=CuS+2H+,该反应平衡常数K=____ 。
(4)“除钙镁”过程在陶瓷容器中进行,NaF的实际用量为理论用量的1.1倍,用量不宜过大的原因是_____ 。
(5)“沉镍”前c(Ni2+)=1.0mol/L,加入少量浓NaOH溶液,若忽略加入浓NaOH溶液对溶液体积的影响,则开始沉淀时溶液的pH=____ 。

已知:H2S的电离常数K1=1.3×10-7,K2=7.1×10-15;Ksp[CuS]=6.0×10-36;Ksp[Ni(OH)2]=1.0×10-15.6。
回答下列问题:
(1)合金中的镍难溶于稀硫酸,“酸溶”时除了加入稀硫酸,还要边搅拌边缓慢加入稀硝酸,还原产物为N2,金属镍溶解的离子方程式是
(2)“除铁”加入Na2CO3时,生成黄钠铁矾(NaFe3(SO4)2(OH)6)的离子方程式是
(3)“除铜”时,反应的离子方程式为H2S+Cu2+=CuS+2H+,该反应平衡常数K=
(4)“除钙镁”过程在陶瓷容器中进行,NaF的实际用量为理论用量的1.1倍,用量不宜过大的原因是
(5)“沉镍”前c(Ni2+)=1.0mol/L,加入少量浓NaOH溶液,若忽略加入浓NaOH溶液对溶液体积的影响,则开始沉淀时溶液的pH=
更新时间:2022-11-09 12:50:28
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】从钒铬锰矿渣(主要成分为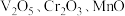 )中提铬的一种工艺流程如图所示:
)中提铬的一种工艺流程如图所示:

已知: 较大时,二价锰
较大时,二价锰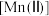 在空气中易被氧化。回答下列问题:
在空气中易被氧化。回答下列问题:
(1) 元素位于元素周期表第
元素位于元素周期表第___________ 周期第___________ 族。
(2)用 溶液制备
溶液制备 胶体的化学方程式为
胶体的化学方程式为___________ 。
(3)“转化”过程中生成 的离子方程式为
的离子方程式为___________ 。
(4)“提纯”过程中 的作用为
的作用为___________ 。
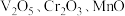 )中提铬的一种工艺流程如图所示:
)中提铬的一种工艺流程如图所示:
已知:
 较大时,二价锰
较大时,二价锰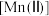 在空气中易被氧化。回答下列问题:
在空气中易被氧化。回答下列问题:(1)
 元素位于元素周期表第
元素位于元素周期表第(2)用
 溶液制备
溶液制备 胶体的化学方程式为
胶体的化学方程式为(3)“转化”过程中生成
 的离子方程式为
的离子方程式为(4)“提纯”过程中
 的作用为
的作用为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】甲、乙、丙、丁分别是盐酸、碳酸钠、氯化钙、硝酸银4种溶液中的一种。将它们两两混合后,观察到的现象是:①甲与乙或丙混合都产生沉淀;②丙与乙或丁混合也产生沉淀;③丁与乙混合产生无色气体。回答下面问题:
(1)写出丁与乙反应的离子方程式:
___________ 。
(2)写出甲和丙反应的化学方程式及离子方程式:
化学方程式;___________ ;
离子方程式:___________ 。
(3)这四种溶液分别是甲:___________ 、乙:___________ 丙:___________ 、丁:___________ 。
(1)写出丁与乙反应的离子方程式:
(2)写出甲和丙反应的化学方程式及离子方程式:
化学方程式;
离子方程式:
(3)这四种溶液分别是甲:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】高铁酸钾( )是一种有暗紫色光泽的粉末,极易溶于水而形成浅紫色的溶液。高铁酸钾是一种集氧化、吸附、絮凝、沉淀、灭菌、消毒、脱色、除臭八大特点为一体的新型、高效、多功能绿色水处理剂。
)是一种有暗紫色光泽的粉末,极易溶于水而形成浅紫色的溶液。高铁酸钾是一种集氧化、吸附、絮凝、沉淀、灭菌、消毒、脱色、除臭八大特点为一体的新型、高效、多功能绿色水处理剂。
资料:①高铁酸钾在低温、碱性环境中稳定,高温、中性和酸性条件下不稳定,易分解生成氧气;
②高铁酸钾易溶于水,不溶于乙醇等有机溶剂;
③高铁酸钾具有强氧化性,且氧化性强于高锰酸钾。
实验室常用次氯酸钠氧化法制备高铁酸钾,具体实验步骤如下:
Ⅰ.用托盘天平称取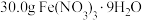 ,另取25.5g NaClO配成100mL溶液;
,另取25.5g NaClO配成100mL溶液;
Ⅱ.在冰水冷却的环境中向NaClO溶液中加入足量NaOH固体,直至无法溶解,得到NaClO的强碱性饱和溶液,缓慢少量分批加入 ,水浴温度控制在26℃,并不断搅拌1.5h左右,至溶液成深紫红色;
,水浴温度控制在26℃,并不断搅拌1.5h左右,至溶液成深紫红色;
Ⅲ.继续充分搅拌,向上述反应液中加入固体NaOH至饱和,直至溶液成粘稠状,过滤,得到滤液;
Ⅳ.向上述滤液中加入KOH固体至饱和,过滤、用乙醇洗涤所得固体,在80℃真空条件下烘干得到产品。
回答下列问题:
(1)配制Ⅰ中的NaClO溶液,下列仪器不需要的是___________ (填仪器名称)。___________ 。实验中若以 代替
代替 作铁源,
作铁源, 的产率和纯度都会降低的原因之一是在反应温度和强碱环境下NaCl的溶解度比
的产率和纯度都会降低的原因之一是在反应温度和强碱环境下NaCl的溶解度比 大,使得NaCl结晶去除率较低;另一个原因是
大,使得NaCl结晶去除率较低;另一个原因是___________ 。
(3)Ⅳ中加入KOH固体至饱和的作用是___________ ,说明此温度下
___________ 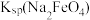 (填“>”“<”或“=”)
(填“>”“<”或“=”)
(4)高铁酸钾溶液在中性条件下不稳定的原因是___________ (用离子方程式解释)。
(5)滴定法测定高铁酸钾样品的纯度,其方法是:称取2.0g产品溶于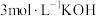 溶液中,加入足量
溶液中,加入足量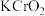 ,充分反应后得到铬酸钾和氢氧化铁沉淀,过滤,滤液在250mL容量瓶中定容;定容后取25.00mL加入稀硫酸酸化,加入二苯胺磺酸钠作指示剂,用
,充分反应后得到铬酸钾和氢氧化铁沉淀,过滤,滤液在250mL容量瓶中定容;定容后取25.00mL加入稀硫酸酸化,加入二苯胺磺酸钠作指示剂,用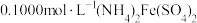 标准溶液滴定至终点,重复操作3次,平均消耗
标准溶液滴定至终点,重复操作3次,平均消耗 溶液的体积为24.00mL。
溶液的体积为24.00mL。
①定容后,加入稀硫酸酸化的目的是___________ ;
②该 产品的纯度为
产品的纯度为___________ (保留三位有效数字)。
 )是一种有暗紫色光泽的粉末,极易溶于水而形成浅紫色的溶液。高铁酸钾是一种集氧化、吸附、絮凝、沉淀、灭菌、消毒、脱色、除臭八大特点为一体的新型、高效、多功能绿色水处理剂。
)是一种有暗紫色光泽的粉末,极易溶于水而形成浅紫色的溶液。高铁酸钾是一种集氧化、吸附、絮凝、沉淀、灭菌、消毒、脱色、除臭八大特点为一体的新型、高效、多功能绿色水处理剂。资料:①高铁酸钾在低温、碱性环境中稳定,高温、中性和酸性条件下不稳定,易分解生成氧气;
②高铁酸钾易溶于水,不溶于乙醇等有机溶剂;
③高铁酸钾具有强氧化性,且氧化性强于高锰酸钾。
实验室常用次氯酸钠氧化法制备高铁酸钾,具体实验步骤如下:
Ⅰ.用托盘天平称取
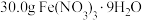 ,另取25.5g NaClO配成100mL溶液;
,另取25.5g NaClO配成100mL溶液;Ⅱ.在冰水冷却的环境中向NaClO溶液中加入足量NaOH固体,直至无法溶解,得到NaClO的强碱性饱和溶液,缓慢少量分批加入
 ,水浴温度控制在26℃,并不断搅拌1.5h左右,至溶液成深紫红色;
,水浴温度控制在26℃,并不断搅拌1.5h左右,至溶液成深紫红色;Ⅲ.继续充分搅拌,向上述反应液中加入固体NaOH至饱和,直至溶液成粘稠状,过滤,得到滤液;
Ⅳ.向上述滤液中加入KOH固体至饱和,过滤、用乙醇洗涤所得固体,在80℃真空条件下烘干得到产品。
回答下列问题:
(1)配制Ⅰ中的NaClO溶液,下列仪器不需要的是
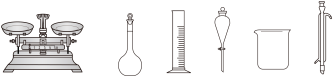
 代替
代替 作铁源,
作铁源, 的产率和纯度都会降低的原因之一是在反应温度和强碱环境下NaCl的溶解度比
的产率和纯度都会降低的原因之一是在反应温度和强碱环境下NaCl的溶解度比 大,使得NaCl结晶去除率较低;另一个原因是
大,使得NaCl结晶去除率较低;另一个原因是(3)Ⅳ中加入KOH固体至饱和的作用是

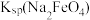 (填“>”“<”或“=”)
(填“>”“<”或“=”)(4)高铁酸钾溶液在中性条件下不稳定的原因是
(5)滴定法测定高铁酸钾样品的纯度,其方法是:称取2.0g产品溶于
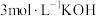 溶液中,加入足量
溶液中,加入足量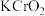 ,充分反应后得到铬酸钾和氢氧化铁沉淀,过滤,滤液在250mL容量瓶中定容;定容后取25.00mL加入稀硫酸酸化,加入二苯胺磺酸钠作指示剂,用
,充分反应后得到铬酸钾和氢氧化铁沉淀,过滤,滤液在250mL容量瓶中定容;定容后取25.00mL加入稀硫酸酸化,加入二苯胺磺酸钠作指示剂,用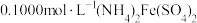 标准溶液滴定至终点,重复操作3次,平均消耗
标准溶液滴定至终点,重复操作3次,平均消耗 溶液的体积为24.00mL。
溶液的体积为24.00mL。①定容后,加入稀硫酸酸化的目的是
②该
 产品的纯度为
产品的纯度为
您最近一年使用:0次
【推荐1】二甲醚是重要的有机中间体,利用二氧化碳加氢合成二甲醚能变废为宝,且可替代汽油作为新型清洁燃料。常温常压下,二氧化碳加氢可选择性生成二甲醚或一氧化碳:
①CO2(g)+3H2(g)=CH3OH(l)+H2O(l)△H1=﹣55.7kJ/mol
②2CH3OH(l)═CH3OCH3(g)+H2O(l)△H2=﹣23.4kJ/mol
③CO2(g)+H2(g)═CO(g)+H2O(l) △H3
④H2O(l)=H2O(g) △H4=+44.0kJ/mol
(1)已知反应CO2(g)+H2(g)=CO(g)+H2O(g)△H,中相关的化学键键能数据如下:
由此计算△H=______ ,则△H3=_______ 。
(2)CO2(g)加氢转化为CH3OCH3(g)和H2O(l)的热化学方程式是___ 。
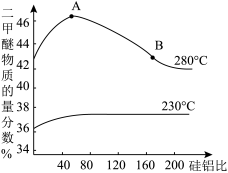
(3)合成二甲醚往往选用硅铝混合物作催化剂,硅铝比例不同,生成二甲醚或一氧化碳的物质的量分数不同。硅铝比与产物选择性如图所示,图中A点和B点的平衡常数比较:KA___ KB(填“>、=、<”)。根据以上两条曲线,写出其中一条变化规律:a.___ 。b.___ 。
(4)常温常压下,向一个2.00L的密闭恒容容器中加入等量2.00mol二氧化碳和氢气,平衡时二甲醚的浓度为0.150mol/L,计算此时二氧化碳的转化率及该反应的平衡常数,要求写出计算过程(计算结果保留3位有效数字)________ 、_________ 。
①CO2(g)+3H2(g)=CH3OH(l)+H2O(l)△H1=﹣55.7kJ/mol
②2CH3OH(l)═CH3OCH3(g)+H2O(l)△H2=﹣23.4kJ/mol
③CO2(g)+H2(g)═CO(g)+H2O(l) △H3
④H2O(l)=H2O(g) △H4=+44.0kJ/mol
(1)已知反应CO2(g)+H2(g)=CO(g)+H2O(g)△H,中相关的化学键键能数据如下:
| 化学键 | H-H | C=O | H-O | C-H | C=O |
| E/(kJ·mol-1) | 436 | 1076 | 465 | 413 | 745 |
由此计算△H=
(2)CO2(g)加氢转化为CH3OCH3(g)和H2O(l)的热化学方程式是
(3)合成二甲醚往往选用硅铝混合物作催化剂,硅铝比例不同,生成二甲醚或一氧化碳的物质的量分数不同。硅铝比与产物选择性如图所示,图中A点和B点的平衡常数比较:KA
(4)常温常压下,向一个2.00L的密闭恒容容器中加入等量2.00mol二氧化碳和氢气,平衡时二甲醚的浓度为0.150mol/L,计算此时二氧化碳的转化率及该反应的平衡常数,要求写出计算过程(计算结果保留3位有效数字)

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】氨、硝酸、硝酸铵、硝酸铜是重要的化工产品。工业合成氨与制备硝酸一般可连续生产,流程如下:
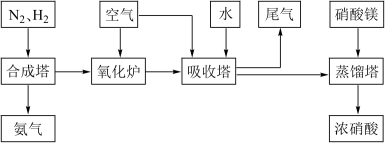
请回答下列问题:
(1)吸收塔中通入空气的作用是_________________ 。
下列可以代替硝酸镁加入到蒸馏塔中的是________ 。
(2)制硝酸尾气中的氮氧化物常用尿素[CO(NH2)2]作为吸收剂,其主要的反应为:NO、NO2混合气与水反应生成亚硝酸,亚硝酸再与尿素[CO(NH2)2]反应生成CO2 和N2,请写出反应的化学方程式_____ 、_______ 。
(3)在氧化炉里,催化剂存在时氨气和氧气反应:
4NH3 + 5O2 4NO + 6H2O 4NH3 + 3O2
4NO + 6H2O 4NH3 + 3O2 2N2+ 6H2O
2N2+ 6H2O
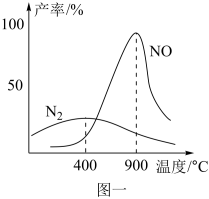
在不同温度时生成产物如图一所示。在氧化炉里,反应温度通常控制在800℃~900℃的理由是______ 。

(4)如图二所示装置可用于电解NO制备 NH4NO3,电解总反应方程式为________ ,需补充氨气的理由是_________________ 。
(5)工业上通常用铜与浓硝酸反应制得光谱纯硝酸铜晶体(化学式为Cu(NO3)2·3H2O,摩尔质量为242g/mol)。已知:25℃、1.01×105 Pa时,在密闭容器发生反应:2NO2、N2O4,达到平衡时,c(NO2)=0.0400 mol/L,c(N2O4)=0.0100mol/L。
现用一定量的Cu与足量的浓高纯度硝酸反应,制得5.00 L已达到平衡的N2O4和NO2的混合气体(25℃、1.01×105 Pa),理论上生成光谱纯硝酸铜晶体的质量为________ g。

请回答下列问题:
(1)吸收塔中通入空气的作用是
下列可以代替硝酸镁加入到蒸馏塔中的是
| A.浓硫酸 | B.氯化钙 | C.生石灰 | D.硝酸亚铁 |
(3)在氧化炉里,催化剂存在时氨气和氧气反应:
4NH3 + 5O2
 4NO + 6H2O 4NH3 + 3O2
4NO + 6H2O 4NH3 + 3O2 2N2+ 6H2O
2N2+ 6H2O在不同温度时生成产物如图一所示。在氧化炉里,反应温度通常控制在800℃~900℃的理由是


(4)如图二所示装置可用于电解NO制备 NH4NO3,电解总反应方程式为
(5)工业上通常用铜与浓硝酸反应制得光谱纯硝酸铜晶体(化学式为Cu(NO3)2·3H2O,摩尔质量为242g/mol)。已知:25℃、1.01×105 Pa时,在密闭容器发生反应:2NO2、N2O4,达到平衡时,c(NO2)=0.0400 mol/L,c(N2O4)=0.0100mol/L。
现用一定量的Cu与足量的浓高纯度硝酸反应,制得5.00 L已达到平衡的N2O4和NO2的混合气体(25℃、1.01×105 Pa),理论上生成光谱纯硝酸铜晶体的质量为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】N2O是一种大气污染物,不仅具有强烈的温室效应,其增温潜能是CO2的数百倍,而且会对大气臭氧层造成破坏。目前全球由制造业、农业、工业以及航天领域等人为活动产生的N2O排放量迅速增加,对人类生存环境造成了潜在的威胁。因此,N2O的排放控制和去除引起了研究者的重视。回答下列问题:
(1)理论计算环丁烯负离子(C4H )去除N2O的一种反应过程及相对能量变化如图所示。
)去除N2O的一种反应过程及相对能量变化如图所示。

C4H (g)+N2O(g)=C4H5O-(g)+N2(g)的△H=
(g)+N2O(g)=C4H5O-(g)+N2(g)的△H=______ ;生成( )的能垒为0,原因是
)的能垒为0,原因是_____ ;下列各步反应中,决定总反应速率的是_______ (填标号)。
a.IM1→IM2 b.IM2→IM3 c.IM3→IM4 d.IM4→C4H5O-(g)+N2(g)
(2)将N2O直接催化分解为N2和O2是最有前途和最经济的技术之一。
①N2O的催化分解机理之一为(*表示催化剂表面活性位):
N2O+* N2O*
N2O*
N2O* O*+N2
O*+N2
2O* O2*+*
O2*+*
O2*=O2+*
研究发现,N2O混有O2时,O2对催化剂有抑制作用,原因是_______ .
②相同条件下,将流速为50mL·min-1的N2O/Ar混合气体分别通过装有不同物质的反应管,测得N2O的转化率随温度的变化如图所示(HAP、FAP分别代表羟基磷灰石、氟磷灰石)。分析图象可知:300~600°C,HAP、FAP对N2O直接分解没有催化作用;无催化剂时,N2O的热分解温度高于520°C;催化剂可降低N2O直接分解所需温度。据图至少还可以得出的两个结论是________________ 。

(3)温度恒为TK,总压恒为pkPa,在体积可变的密闭容器中投入nmolN2O,初始体积为V0L,发生反应2N2O 2N2+O2,达到平衡时,体积变为VL,则N2O的平衡转化率α=
2N2+O2,达到平衡时,体积变为VL,则N2O的平衡转化率α=_____ ,该温度下反应的平衡常数K=______ mol·L-1。
(1)理论计算环丁烯负离子(C4H
 )去除N2O的一种反应过程及相对能量变化如图所示。
)去除N2O的一种反应过程及相对能量变化如图所示。
C4H
 (g)+N2O(g)=C4H5O-(g)+N2(g)的△H=
(g)+N2O(g)=C4H5O-(g)+N2(g)的△H= )的能垒为0,原因是
)的能垒为0,原因是a.IM1→IM2 b.IM2→IM3 c.IM3→IM4 d.IM4→C4H5O-(g)+N2(g)
(2)将N2O直接催化分解为N2和O2是最有前途和最经济的技术之一。
①N2O的催化分解机理之一为(*表示催化剂表面活性位):
N2O+*
 N2O*
N2O*N2O*
 O*+N2
O*+N22O*
 O2*+*
O2*+*O2*=O2+*
研究发现,N2O混有O2时,O2对催化剂有抑制作用,原因是
②相同条件下,将流速为50mL·min-1的N2O/Ar混合气体分别通过装有不同物质的反应管,测得N2O的转化率随温度的变化如图所示(HAP、FAP分别代表羟基磷灰石、氟磷灰石)。分析图象可知:300~600°C,HAP、FAP对N2O直接分解没有催化作用;无催化剂时,N2O的热分解温度高于520°C;催化剂可降低N2O直接分解所需温度。据图至少还可以得出的两个结论是

(3)温度恒为TK,总压恒为pkPa,在体积可变的密闭容器中投入nmolN2O,初始体积为V0L,发生反应2N2O
 2N2+O2,达到平衡时,体积变为VL,则N2O的平衡转化率α=
2N2+O2,达到平衡时,体积变为VL,则N2O的平衡转化率α=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】现有含有少量NaCl、Na2SO4、Na2CO3等杂质的NaNO3溶液,选择适当的试剂除去杂质,得到纯净的NaNO3固体,实验流程如图所示。

(1)沉淀A的主要成分是___ 、___ (填化学式)。
(2)③中加入过量的Na2CO3溶液的目的是___ 。
(3)溶液3经过处理可以得到NaNO3固体,溶液3中肯定含有的杂质是___ ,为了除去杂质,可向溶液3中加入适量的____ 。

(1)沉淀A的主要成分是
(2)③中加入过量的Na2CO3溶液的目的是
(3)溶液3经过处理可以得到NaNO3固体,溶液3中肯定含有的杂质是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】黏土钒矿主要成分为钒的+3、+4、+5价的化合物以及 、
、 等,采用如图所示工艺流程可由黏土钒矿制备
等,采用如图所示工艺流程可由黏土钒矿制备 。
。

已知:①钒的化合物溶于酸后多以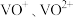 形式存在。
形式存在。
②钒元素的存在形态较多,部分四价钒和五价钒物种的分布分数 与
与 的关系如图所示。
的关系如图所示。
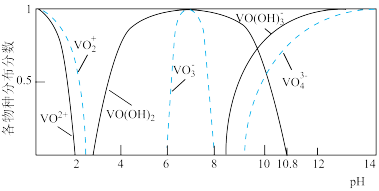
(1)基态V原子的价电子排布图为:_______ , 的空间构型为:
的空间构型为:_______ 。
(2)写出“酸浸氧化”时 转化为
转化为 发生反应的离子方程式
发生反应的离子方程式_______ 。
(3)加入 控制溶液的
控制溶液的 ,其目的是
,其目的是_______ 。
(4)“滤液1”中主要的阴离子有 以及
以及_______ 。写出形成“滤渣2”主要成分发生反应的离子方程式_______ 。
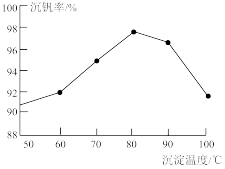
(5)“沉钒”时控制溶液 约为7,生成偏钒酸铵
约为7,生成偏钒酸铵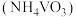 固体。沉钒率随温度变化如图,温度高于
固体。沉钒率随温度变化如图,温度高于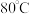 ,沉钒率下降的原因是
,沉钒率下降的原因是_______ 。
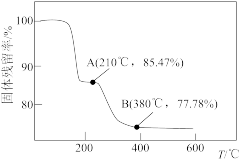
(6)在“煅烧” 的过程中,残留固体的质量随温度变化的曲线如图所示,则A点剩余固体的成分为
的过程中,残留固体的质量随温度变化的曲线如图所示,则A点剩余固体的成分为_______ (填化学式)。
 、
、 等,采用如图所示工艺流程可由黏土钒矿制备
等,采用如图所示工艺流程可由黏土钒矿制备 。
。
已知:①钒的化合物溶于酸后多以
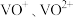 形式存在。
形式存在。②钒元素的存在形态较多,部分四价钒和五价钒物种的分布分数
 与
与 的关系如图所示。
的关系如图所示。
(1)基态V原子的价电子排布图为:
 的空间构型为:
的空间构型为:(2)写出“酸浸氧化”时
 转化为
转化为 发生反应的离子方程式
发生反应的离子方程式(3)加入
 控制溶液的
控制溶液的 ,其目的是
,其目的是(4)“滤液1”中主要的阴离子有
 以及
以及(5)“沉钒”时控制溶液
 约为7,生成偏钒酸铵
约为7,生成偏钒酸铵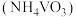 固体。沉钒率随温度变化如图,温度高于
固体。沉钒率随温度变化如图,温度高于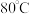 ,沉钒率下降的原因是
,沉钒率下降的原因是
(6)在“煅烧”
 的过程中,残留固体的质量随温度变化的曲线如图所示,则A点剩余固体的成分为
的过程中,残留固体的质量随温度变化的曲线如图所示,则A点剩余固体的成分为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】明矾[KAl(SO4) 2·12H2O]易溶于水,不易溶于乙醇,在生产、生活中有广泛用途。利用炼铝厂的废料——铝灰(含Al、Al2O3及少量的SiO2、FeO·xFe2O2)制备明矾的工艺流程如下:
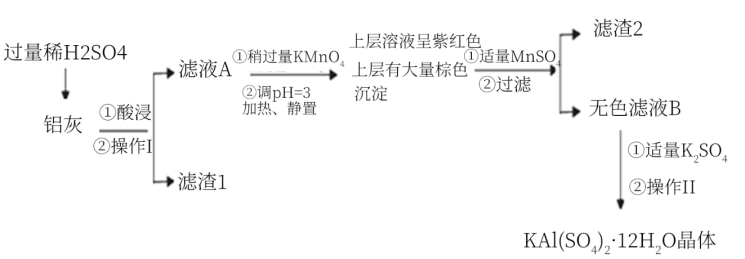
回答下列问题:
(1)酸浸时为提高铝的浸取虑,可采取的措施是_________ (填标号)。
a 改用同浓度的硝酸 b 用硫酸多次浸取 c 浸取时间缩短一半 d 适当升高温度
(2)滤渣1的成分是__________ ;滤渣2经过处理可以制得一种高效的无机高分子混凝剂,其化学式为[Fe2(OH)n(SO4)(3-0.5n)]m,则该物质中铁元素的化合价为___________ 。
(3)检验滤液A中含有Fe2+的实验方案及现象是________________________________________ 。
(4)已知常温下Ksp[Fe(OH)3]=4.0×10-38,当调节溶液的pH=3时,溶液中c(Fe3+)=____________ 。
(5)操作Ⅱ中包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等操作,使用酒精洗涤明矾晶体的目的是______ ;明矾净水的原理是__________________ (写离子方程式)。
(6)已知在pH=3和加热条件下,MnO4-可与Mn2+反应生成MnO2,则上述流程图中加入适量MnSO4发生反应的离子方程式为_________________________ 。

回答下列问题:
(1)酸浸时为提高铝的浸取虑,可采取的措施是
a 改用同浓度的硝酸 b 用硫酸多次浸取 c 浸取时间缩短一半 d 适当升高温度
(2)滤渣1的成分是
(3)检验滤液A中含有Fe2+的实验方案及现象是
(4)已知常温下Ksp[Fe(OH)3]=4.0×10-38,当调节溶液的pH=3时,溶液中c(Fe3+)=
(5)操作Ⅱ中包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等操作,使用酒精洗涤明矾晶体的目的是
(6)已知在pH=3和加热条件下,MnO4-可与Mn2+反应生成MnO2,则上述流程图中加入适量MnSO4发生反应的离子方程式为
您最近一年使用:0次



