按要求回答下列问题:
(1)已知H2和O2反应时放热,且断裂1molH-H键、1molO=O键、1molO-H键需要吸收的能量分别为Q1kJ、Q2kJ、Q3kJ。下列关系一定正确的是_________。
(2)下列变化中满足如图图示的是_________ (填选项字母)。
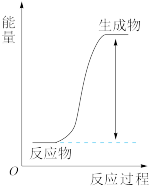
A镁和稀盐酸的反应 B.Ba(OH)2•8H2O与NH4Cl的反应 C.氯化铵固体加入水中 D.氢气燃烧 E.H-O-H→2H+O
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为_________ (填选项字母)。
A铝片、铜片 B.铜片、铝片 C.铝片、铝片
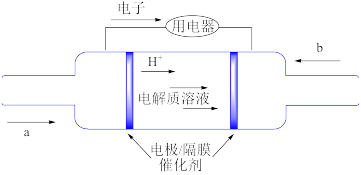
(4)2020年上海进博会展览中,诸多氢能源汽车纷纷亮相。氢燃料电池被誉为氢能源汽车的心脏。某种氢燃料电池的内部结构如图所示,a 处通入气体的是_________ ,左侧的电极为电池的_________ (填“正极”或“负极”), 右侧电极发生的反应为:_________ 。
(1)已知H2和O2反应时放热,且断裂1molH-H键、1molO=O键、1molO-H键需要吸收的能量分别为Q1kJ、Q2kJ、Q3kJ。下列关系一定正确的是_________。
| A.Q1+Q2>Q3 | B.2Q1+Q2>2Q3 | C.2Q1+Q2<4Q3 | D.2Q1+Q2>4Q3 |

A镁和稀盐酸的反应 B.Ba(OH)2•8H2O与NH4Cl的反应 C.氯化铵固体加入水中 D.氢气燃烧 E.H-O-H→2H+O
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为
A铝片、铜片 B.铜片、铝片 C.铝片、铝片
(4)2020年上海进博会展览中,诸多氢能源汽车纷纷亮相。氢燃料电池被誉为氢能源汽车的心脏。某种氢燃料电池的内部结构如图所示,a 处通入气体的是

21-22高一·全国·假期作业 查看更多[3]
(已下线)第05讲 化学能转化为电能-【寒假自学课】2022年高一化学寒假精品课(苏教版必修第二册)(已下线)第06讲 化学电源-【寒假自学课】2022年高一化学寒假精品课(苏教版必修第二册)广东省潮州市饶平县第二中学2021-2022学年高一下学期期中化学试题
更新时间:2022-11-11 10:59:38
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】化学反应中伴随着能量变化,探究各种能量变化是一永恒的主题。
(1) 和
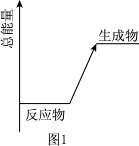
和 反应时的能量变化关系如图1所示,则该反应为
反应时的能量变化关系如图1所示,则该反应为_______ 反应(选填:吸热、放热)。
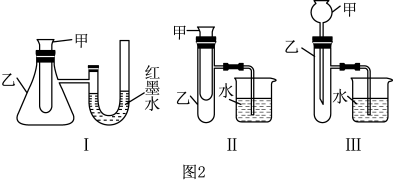
(2)某实验小组设计了上述图2中的三套实验装置,其中不能用来证明“ 和
和 反应的能量变化情况”的是
反应的能量变化情况”的是_______ (填序号)。
(3)某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管里加入 和
和 发生上述反应,U形管中可观察到的现象是
发生上述反应,U形管中可观察到的现象是_____
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重要贡献。现有如图原电池装置,插入电解质溶液前 和
和 电极的质量相等。
电极的质量相等。
(4)当图3中的电解质溶液为氯化铁时,铜片作_______ 极,图中箭头的方向表示_______ (填“电子”或“电流”)的流向,铁片上发生反应的电极方程式为_______ .
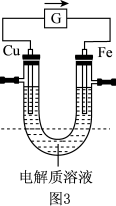
(5)当图3中电解质溶液更换为X溶液时,两电极的质量变化曲线如图4所示:
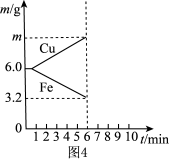
①该电解质溶液X可以是下列中的_______ (填字母)。
A.稀硫酸B. 溶液C.稀盐酸D.
溶液C.稀盐酸D. 溶液
溶液
② 电极的电极反应式为
电极的电极反应式为_______ ;6min时 电极的质量为
电极的质量为_______ g。
(1)
 和
和 反应时的能量变化关系如图1所示,则该反应为
反应时的能量变化关系如图1所示,则该反应为
(2)某实验小组设计了上述图2中的三套实验装置,其中不能用来证明“
 和
和 反应的能量变化情况”的是
反应的能量变化情况”的是
(3)某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管里加入
 和
和 发生上述反应,U形管中可观察到的现象是
发生上述反应,U形管中可观察到的现象是原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重要贡献。现有如图原电池装置,插入电解质溶液前
 和
和 电极的质量相等。
电极的质量相等。(4)当图3中的电解质溶液为氯化铁时,铜片作

(5)当图3中电解质溶液更换为X溶液时,两电极的质量变化曲线如图4所示:

①该电解质溶液X可以是下列中的
A.稀硫酸B.
 溶液C.稀盐酸D.
溶液C.稀盐酸D. 溶液
溶液②
 电极的电极反应式为
电极的电极反应式为 电极的质量为
电极的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学反应常伴随能量变化,是人类获得能量的重要途径。
(1)一种即热饭盒的结构如图所示,这种饭盒使用起来非常方便,撤去底部的隔板几分钟后,饭菜就变热了。
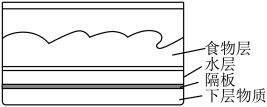
①下层物质可以是由镁粉、铁粉和食盐组成的混合物,则镁粉和铁粉的作用依次为___________ 、___________ 。
②化学能转化为热能在生产或生活中的应用还有___________ (填一种)。
③某种冷敷袋盛装的物质是硝酸铵,加少量水即可达到冷却效果,该冷敷袋的主要工作原理为___________ 热(填“吸”或“放”)的___________ 变化(填“物理”或“化学”)。
(2)借鉴中和反应反应热的测定方法,某同学测定放热反应 的焓变
的焓变 (忽略温度对焓变的影响,忽略溶液体积、质量变化和金属吸收的热量。近似的认为溶液的密度、比热容与水的相同,已知水的比热容为4.18
(忽略温度对焓变的影响,忽略溶液体积、质量变化和金属吸收的热量。近似的认为溶液的密度、比热容与水的相同,已知水的比热容为4.18 )。实验结果见下表。
)。实验结果见下表。
则温度:b___________ c(填“>”“<”或“=”);
___________  (用含a、c的代数式表示)。
(用含a、c的代数式表示)。
(3)已知298 K,101 kPa时,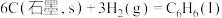
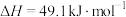 ,相关物质的摩尔燃烧焓数据如表:
,相关物质的摩尔燃烧焓数据如表:
则表示C(石墨,s)摩尔燃烧焓的热化学方程式为___________ ,a=___________ 。
(1)一种即热饭盒的结构如图所示,这种饭盒使用起来非常方便,撤去底部的隔板几分钟后,饭菜就变热了。

①下层物质可以是由镁粉、铁粉和食盐组成的混合物,则镁粉和铁粉的作用依次为
②化学能转化为热能在生产或生活中的应用还有
③某种冷敷袋盛装的物质是硝酸铵,加少量水即可达到冷却效果,该冷敷袋的主要工作原理为
(2)借鉴中和反应反应热的测定方法,某同学测定放热反应
 的焓变
的焓变 (忽略温度对焓变的影响,忽略溶液体积、质量变化和金属吸收的热量。近似的认为溶液的密度、比热容与水的相同,已知水的比热容为4.18
(忽略温度对焓变的影响,忽略溶液体积、质量变化和金属吸收的热量。近似的认为溶液的密度、比热容与水的相同,已知水的比热容为4.18 )。实验结果见下表。
)。实验结果见下表。| 序号 | 反应试剂 | 体系温度/℃ | ||
| 反应前 | 反应后 | |||
| ⅰ | 100mL 0.20  溶液 溶液 | 1.36g Zn粉 | a | b |
| ⅱ | 0.62g Zn粉 | a | c | |

 (用含a、c的代数式表示)。
(用含a、c的代数式表示)。(3)已知298 K,101 kPa时,
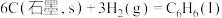
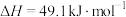 ,相关物质的摩尔燃烧焓数据如表:
,相关物质的摩尔燃烧焓数据如表:| 物质 |  | 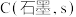 |  |
摩尔燃烧焓 | -285.8 | -393.5 | a |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用___ (填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热饭盒”给人们生活带来方便,它可利用下面___ (填字母)反应释放的热量加热食物。
A.生石灰和水 B.浓硫酸和水
(3)表中是部分共价键的键能。
根据表中的数据写出工业合成氨的热化学反应方程式:_______
(4)写出下列反应的热化学方程式
①1molC与1mol水蒸气反应生成1molCO和1molH2,吸热131. 5kJ:____
②1molNO2气体溶于水生成HNO3和NO气体放出46kJ的热量:____
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用
(2)“即热饭盒”给人们生活带来方便,它可利用下面
A.生石灰和水 B.浓硫酸和水
(3)表中是部分共价键的键能。
| 共价键 |  |  |  |
键能( ) ) | 436 | 946 | 391 |
(4)写出下列反应的热化学方程式
①1molC与1mol水蒸气反应生成1molCO和1molH2,吸热131. 5kJ:
②1molNO2气体溶于水生成HNO3和NO气体放出46kJ的热量:
您最近一年使用:0次
【推荐2】已知某些化学键的键能数据如下:
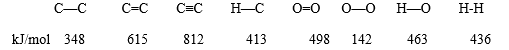
(1)通过比较C—C 和 C=C 的键能大小,简要说明为什么烯烃易发生加成反应而烷烃不能?______ 。
(2)利用键能数据可判断反应 2H2 + O2 → 2 H2O 为 放热反应, 计算每生成 1 mol H2O 所放出的热量为_____________ kJ。
(3)若某有机物的结构简式如下: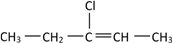 ,一定条件下与HCl发生加成反应后可能生成两种互为同分异构体的物质,写出其中属于手性分子的物质的结构简式:
,一定条件下与HCl发生加成反应后可能生成两种互为同分异构体的物质,写出其中属于手性分子的物质的结构简式:________________
(4)将硫酸铜白色固体溶于水得到蓝色的溶液,原因是生成了一种配合离子,其结构简式为:___________ (标明配位键),向该溶液中加入过量稀氨水得深蓝色溶液,其离子方程式为 _________ 。已知NF3与NH3的结构类似,但NF3不易与Cu2+形成配离子,其主要原因是_________________________________ 。
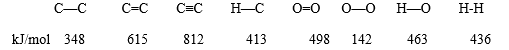
(1)通过比较C—C 和 C=C 的键能大小,简要说明为什么烯烃易发生加成反应而烷烃不能?
(2)利用键能数据可判断反应 2H2 + O2 → 2 H2O 为 放热反应, 计算每生成 1 mol H2O 所放出的热量为
(3)若某有机物的结构简式如下:
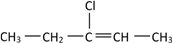 ,一定条件下与HCl发生加成反应后可能生成两种互为同分异构体的物质,写出其中属于手性分子的物质的结构简式:
,一定条件下与HCl发生加成反应后可能生成两种互为同分异构体的物质,写出其中属于手性分子的物质的结构简式:(4)将硫酸铜白色固体溶于水得到蓝色的溶液,原因是生成了一种配合离子,其结构简式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】汽车尾气中主要污染物是 和CO,它们是现代化城市中的重要大气污染物。
和CO,它们是现代化城市中的重要大气污染物。
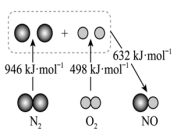
(1)汽车发动机工作时会引发 和
和 反应生成NO,其能量变化如图所示,则图中三种分子最稳定的是
反应生成NO,其能量变化如图所示,则图中三种分子最稳定的是___________ ,图中对应反应的热化学方程式为___________ 。
(2) 和CO均是有害气体,可在
和CO均是有害气体,可在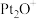 表面转化为无害气体,其反应原理如下:
表面转化为无害气体,其反应原理如下: 。有关化学反应的能量变化过程如图所示。
。有关化学反应的能量变化过程如图所示。
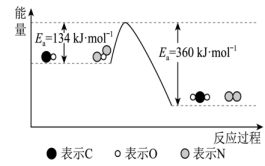
图中反应是___________ (填“放热”或“吸热”)反应,该反应的活化能为___________ ,该反应的 =
=___________ 。
(3)利用 还原法可将
还原法可将 ,还原为
,还原为 进行脱除。已知:
进行脱除。已知: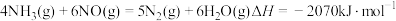 ,若有0.5molNO被还原,放出的热量为
,若有0.5molNO被还原,放出的热量为___________ 。
 和CO,它们是现代化城市中的重要大气污染物。
和CO,它们是现代化城市中的重要大气污染物。(1)汽车发动机工作时会引发
 和
和 反应生成NO,其能量变化如图所示,则图中三种分子最稳定的是
反应生成NO,其能量变化如图所示,则图中三种分子最稳定的是
(2)
 和CO均是有害气体,可在
和CO均是有害气体,可在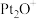 表面转化为无害气体,其反应原理如下:
表面转化为无害气体,其反应原理如下: 。有关化学反应的能量变化过程如图所示。
。有关化学反应的能量变化过程如图所示。
图中反应是
 =
=(3)利用
 还原法可将
还原法可将 ,还原为
,还原为 进行脱除。已知:
进行脱除。已知: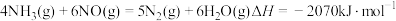 ,若有0.5molNO被还原,放出的热量为
,若有0.5molNO被还原,放出的热量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
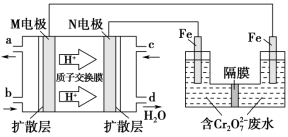
【推荐1】现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有 ),实验室利用如图装置模拟该方法:
),实验室利用如图装置模拟该方法:
(1)N电极为电池的___________ (填“正”或“负”)极,N电极的电极反应式为___________ 。
(2)下图电解法除去含铬废水中铁电极为___________ 电极(填“活性”或“惰性”)请写出该电解池的阳极电极反应式___________ 。
 ),实验室利用如图装置模拟该方法:
),实验室利用如图装置模拟该方法:(1)N电极为电池的
(2)下图电解法除去含铬废水中铁电极为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
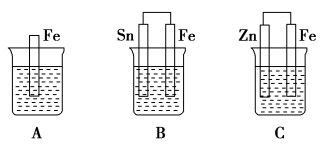
(1)A中反应的离子方程式为___________ 。
(2)B中锡极为________ 极,电极反应式为_________ ,锡极附近溶液的酸性_________ (填“增强”“减弱”或“不变”)。B中Fe极为________ 极,电极反应式为_________ 。
(3)C中被氧化的金属是___________ ,总反应的化学方程式为___________ 。
(4)A、B、C中铁被氧化由快到慢的顺序是___________ 。

(1)A中反应的离子方程式为
(2)B中锡极为
(3)C中被氧化的金属是
(4)A、B、C中铁被氧化由快到慢的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】铝和氢氧化钠都是重要的工业产品。请回答:
(1)工业冶炼铝的化学方程式是___________________________________________ 。
(2)可用阳离子交换膜法电解饱和食盐水制NaOH,其工作原理如左下图所示。
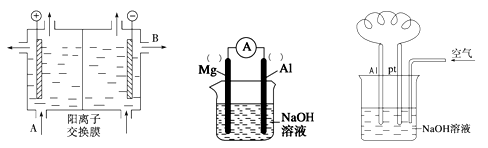
①请写出A、B两处物质的名称:A___________________ 、B____________________
②请写出电解食盐水的离子方程式__________________________________________
(3)以镁条、铝片为电极,以NaOH溶液为电解质溶液设计的原电池如上中图。
①负极材料为________ (填Mg或Al)。
②该原电池的总反应式为____________________________________________
(要求用单线桥标出电子转移的方向和数目)
(4)铝—空气燃料电池可用于电动汽车,通常以NaOH溶液为电解液,铝合金为负极,通入空气的极为正极(如右上图),则
负极的电极反应式为__________________________________ ;
正极的电极反应式为___________________________________ 。
(1)工业冶炼铝的化学方程式是
(2)可用阳离子交换膜法电解饱和食盐水制NaOH,其工作原理如左下图所示。

①请写出A、B两处物质的名称:A
②请写出电解食盐水的离子方程式
(3)以镁条、铝片为电极,以NaOH溶液为电解质溶液设计的原电池如上中图。
①负极材料为
②该原电池的总反应式为
(要求用单线桥标出电子转移的方向和数目)
(4)铝—空气燃料电池可用于电动汽车,通常以NaOH溶液为电解液,铝合金为负极,通入空气的极为正极(如右上图),则
负极的电极反应式为
正极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】肼(N2H4),又称联氨,主要用作火箭和喷气发动机的燃料部分。
(1)已知:N2H4(g)+H2(g) =2NH3(g) △H=-41.8 KJ•mol-1
N2(g)+3H2(g) 2NH3(g) △H=-92 KJ•mol-1
2NH3(g) △H=-92 KJ•mol-1
2H2(g)+O2(g) =2H2O(g) △H=-483.6 KJ•mol-1
请写出肼与氧气反应生成氮气和水蒸气的热化学方程式______________________________ ;
(2)同时,肼也可作为新型燃料电池的燃料。请利用肼、氧气与氢氧化钾溶液组成碱性燃料电池,写出该电池负极的电极反应式__________________________ ,当电路中转移0.6mol电子时,正极消耗的氧气体积为___________ L(标准状况下)。
(1)已知:N2H4(g)+H2(g) =2NH3(g) △H=-41.8 KJ•mol-1
N2(g)+3H2(g)
 2NH3(g) △H=-92 KJ•mol-1
2NH3(g) △H=-92 KJ•mol-12H2(g)+O2(g) =2H2O(g) △H=-483.6 KJ•mol-1
请写出肼与氧气反应生成氮气和水蒸气的热化学方程式
(2)同时,肼也可作为新型燃料电池的燃料。请利用肼、氧气与氢氧化钾溶液组成碱性燃料电池,写出该电池负极的电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】如图为原电池装置示意图:
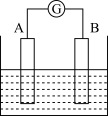
(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,做负极的分别是__________ 。
a.铝片 铜片 b.铜片 铝片 c.铝片 铝片 d.铜片 铜片
(2)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。写出B电极反应式:______________________________ ;该电池工作时,A电极的质量将__________ (填“增加”、“减小”或“不变”)。若该电池反应消耗了0.1 mol H2SO4,则转移电子的数目为__________ 。
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入CH4和O2,该电池为甲烷燃料电池,写出A电极反应式:______________________________ 。该电池工作一段时间后,溶液的碱性将__________ (填“增强”、“减弱”或“不变”)。

(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,做负极的分别是
a.铝片 铜片 b.铜片 铝片 c.铝片 铝片 d.铜片 铜片
(2)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。写出B电极反应式:
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入CH4和O2,该电池为甲烷燃料电池,写出A电极反应式:
您最近一年使用:0次




