亚硝酸钠(NaNO2)是一种用途广泛的工业盐,其外观和食盐相似容易误食中毒。
(1)人体正常的血红蛋白中含有 ,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的
,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的 转化为
转化为 而使人体中毒,服用维生素C可解毒。
而使人体中毒,服用维生素C可解毒。 转化为
转化为 时,
时, 在反应中被
在反应中被_______ (填“氧化”或“还原”);服用维生素C可使血红蛋白中的 转变成
转变成 ,说明维生素C作
,说明维生素C作_______ (填“氧化”或“还原”)剂。
(2)已知 能发生反应:
能发生反应: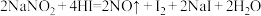 ,淀粉遇碘会变蓝色。则鉴别
,淀粉遇碘会变蓝色。则鉴别 固体和NaCl固体,无须选用的物质为
固体和NaCl固体,无须选用的物质为_______ (填标号)。
①水 ②碘化钾淀粉试纸 ③食醋 ④白酒
(3)某厂废液中含有2%~5%的 ,直接排放会造成污染,下列试剂能使
,直接排放会造成污染,下列试剂能使 转化为不引起二次污染的
转化为不引起二次污染的 的是
的是_______ (填标号)。
A.NaCl B. C.
C.
(4) 也可作为食品防腐剂,但由于亚硝酸钠具有一定的毒性,因此食品中用量和残留量均有严格规定。可用酸性
也可作为食品防腐剂,但由于亚硝酸钠具有一定的毒性,因此食品中用量和残留量均有严格规定。可用酸性 测定
测定 样品纯度,配平下列反应并用单线桥法标出该反应中电子转移的方向和数目:
样品纯度,配平下列反应并用单线桥法标出该反应中电子转移的方向和数目:_________ 。
_______ _______
_______ _______
_______ _______
_______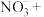 _______
_______ _______
_______
(5)可用Cl2将溶液中的NO 氧化为NO
氧化为NO ,同时生成Cl-,则该反应的离子方程式为
,同时生成Cl-,则该反应的离子方程式为_______ 。
(1)人体正常的血红蛋白中含有
 ,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的
,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的 转化为
转化为 而使人体中毒,服用维生素C可解毒。
而使人体中毒,服用维生素C可解毒。 转化为
转化为 时,
时, 在反应中被
在反应中被 转变成
转变成 ,说明维生素C作
,说明维生素C作(2)已知
 能发生反应:
能发生反应: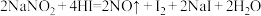 ,淀粉遇碘会变蓝色。则鉴别
,淀粉遇碘会变蓝色。则鉴别 固体和NaCl固体,无须选用的物质为
固体和NaCl固体,无须选用的物质为①水 ②碘化钾淀粉试纸 ③食醋 ④白酒
(3)某厂废液中含有2%~5%的
 ,直接排放会造成污染,下列试剂能使
,直接排放会造成污染,下列试剂能使 转化为不引起二次污染的
转化为不引起二次污染的 的是
的是A.NaCl B.
 C.
C.
(4)
 也可作为食品防腐剂,但由于亚硝酸钠具有一定的毒性,因此食品中用量和残留量均有严格规定。可用酸性
也可作为食品防腐剂,但由于亚硝酸钠具有一定的毒性,因此食品中用量和残留量均有严格规定。可用酸性 测定
测定 样品纯度,配平下列反应并用单线桥法标出该反应中电子转移的方向和数目:
样品纯度,配平下列反应并用单线桥法标出该反应中电子转移的方向和数目:_______
 _______
_______ _______
_______ _______
_______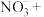 _______
_______ _______
_______
(5)可用Cl2将溶液中的NO
 氧化为NO
氧化为NO ,同时生成Cl-,则该反应的离子方程式为
,同时生成Cl-,则该反应的离子方程式为
更新时间:2022-10-28 15:19:46
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】反应方程式如下,完成相应问题
___ Fe3++___ SO2+___ H2O→___ Fe2++___ SO42-+___ H+
(1)配平上述反应方程式并标出电子转移的方向和数目__________ 。
(2)反应中氧化剂为________ ,还原剂为________ 。
(3)反应中,所得氧化产物和还原产物的物质的量之比为_____________ 。
(4)反应过程中,溶液颜色由_______ 变为_________ 。
(1)配平上述反应方程式并标出电子转移的方向和数目
(2)反应中氧化剂为
(3)反应中,所得氧化产物和还原产物的物质的量之比为
(4)反应过程中,溶液颜色由
您最近一年使用:0次
【推荐2】1.亚硝酸钠易溶于水,水溶液显碱性,有氧化性,也有还原性。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:
___________ ___________
___________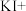 ___________=___________
___________=___________ ___________
___________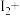 ___________
___________ ___________
___________
___ 
(1)请完成该化学方程式并配平。___________
(2)将上述反应方程式改写为离子反应方程式:___________ 。
(3)用上述反应来处理 并不是最佳方法,其原因是
并不是最佳方法,其原因是___________ 。从环保角度来讲,要将 转化为氮气,所用物质的
转化为氮气,所用物质的___________ (填“氧化性”或“还原性”)应该比KI更___________ (填“强”或“弱”)。
(4)简便鉴别亚硝酸钠和氯化钠的方法是___________ 。
(5)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目:___________ 。
 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:___________
 ___________
___________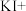 ___________=___________
___________=___________ ___________
___________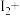 ___________
___________ ___________
___________

(1)请完成该化学方程式并配平。
(2)将上述反应方程式改写为离子反应方程式:
(3)用上述反应来处理
 并不是最佳方法,其原因是
并不是最佳方法,其原因是 转化为氮气,所用物质的
转化为氮气,所用物质的(4)简便鉴别亚硝酸钠和氯化钠的方法是
(5)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】为抗击新冠肺炎经常对环境进行消毒,常用药物如:高锰酸钾、漂白粉、氯气等。
(1)新制氯水中含有多种微粒,将紫色石蕊试液滴入氯水中,溶液显红色起作用的微粒是___________ (填化学符号,下同);过一会儿,溶液颜色逐渐褪去,起作用的微粒是___________ 。
(2)工业上利用氯气和石灰乳反应制取漂白粉,漂白粉的有效成分为___________ (填化学式)。向漂白粉清液中滴加碳酸钠溶液,有白色沉淀生成,写出发生反应的离子方程式___________ 。
(3)已知高锰酸钾与浓盐酸混合能产生氯气,化学反应方程式为: (浓)
(浓)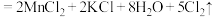 ,回答下列问题:
,回答下列问题:
①用双线桥标出电子转移的方向和数目___________
 (浓)
(浓)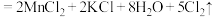
(在线桥上标出化合价升或降、得或失电子数以及被氧化或被还原)
②结合所学知识及本题信息比较氧化性强弱:
___________ 
___________  (填“>”,“<”或“=”)。
(填“>”,“<”或“=”)。
③反应中氯化氢表现出的性质是___________ 。(填写字母)
a.还原性 b.酸性 c.氧化性
④若生成标准状况下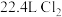 ,则转移电子总数是
,则转移电子总数是___________ 。
(1)新制氯水中含有多种微粒,将紫色石蕊试液滴入氯水中,溶液显红色起作用的微粒是
(2)工业上利用氯气和石灰乳反应制取漂白粉,漂白粉的有效成分为
(3)已知高锰酸钾与浓盐酸混合能产生氯气,化学反应方程式为:
 (浓)
(浓)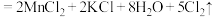 ,回答下列问题:
,回答下列问题:①用双线桥标出电子转移的方向和数目
 (浓)
(浓)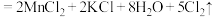
(在线桥上标出化合价升或降、得或失电子数以及被氧化或被还原)
②结合所学知识及本题信息比较氧化性强弱:


 (填“>”,“<”或“=”)。
(填“>”,“<”或“=”)。③反应中氯化氢表现出的性质是
a.还原性 b.酸性 c.氧化性
④若生成标准状况下
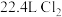 ,则转移电子总数是
,则转移电子总数是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO2+NO+2NaOH=2NaNO2+H2O ①
2NO2+2NaOH=NaNO2+NaNO3+H2O ②
①在反应①中,氧化剂是___________ ;在反应②中,氧化剂和还原剂的物质的量之比为___________ 。
②由反应②判断二氧化氮___________ (填“是”或“不是”)酸性氧化物。解释原因:___________ 。
(2)汽车尾气中含有CO和NO,消除这两种物质对大气的污染的方法是安装催化转化器,使它们发生反应消除污染,试写出该反应的化学方程式:___________ 。
(3)在一定条件下,用氨气可以将氮氧化物转化为无污染的物质。
①请写出NO2与氨气发生该反应的化学方程式:___________ 。生成1.4 mol N2时,转移电子的物质的量为___________ 。
②现有NO2和NO的混合气体3 L,通入3 L(同温同压下)NH3恰好使其完全转化为N2 则原混合气体中NO2和NO的物质的量之比为___________ 。
NO2+NO+2NaOH=2NaNO2+H2O ①
2NO2+2NaOH=NaNO2+NaNO3+H2O ②
①在反应①中,氧化剂是
②由反应②判断二氧化氮
(2)汽车尾气中含有CO和NO,消除这两种物质对大气的污染的方法是安装催化转化器,使它们发生反应消除污染,试写出该反应的化学方程式:
(3)在一定条件下,用氨气可以将氮氧化物转化为无污染的物质。
①请写出NO2与氨气发生该反应的化学方程式:
②现有NO2和NO的混合气体3 L,通入3 L(同温同压下)NH3恰好使其完全转化为N2 则原混合气体中NO2和NO的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化工产品中,含氯物质众多,其用途广泛。回答下列问题:
(1)如图为氯及其化合物的“价一类”二维图。缺失的类别A为___________ 、物质B为___________ (填化学式)。

(2)电石渣[主要成分为Ca(OH)2]是氯碱工业中的废料,某同学在实验室以电石渣为原料制取KClO3的工艺流程如图所示:

已知Ca(ClO3)2易溶于水。
①工业生产电石的反应为CaO+3C CaC2+CO↑,该反应中还原剂为
CaC2+CO↑,该反应中还原剂为___________ 。
②流程中“制Ca(ClO3)2”的化学方程式为___________ ;“转化”发生反应的离子方程式为___________ 。
③上述流程中所用Cl2是用MnO2与浓盐酸反应制得。该反应的离子方程式是___________ ,其中盐酸体现的性质为___________ 性和___________ 性。下列发生装置可用于制备Cl2的是___________ (填字母)。

(3)“84”消毒液可杀死新冠病毒,其主要成分为NaClO,但在使用过程中不能与含盐酸的除垢剂混用,原因是NaClO与盐酸反应生成Cl2,写出该反应的化学方程式并用双线桥法标出电子的得失:___________ 。
(1)如图为氯及其化合物的“价一类”二维图。缺失的类别A为

(2)电石渣[主要成分为Ca(OH)2]是氯碱工业中的废料,某同学在实验室以电石渣为原料制取KClO3的工艺流程如图所示:

已知Ca(ClO3)2易溶于水。
①工业生产电石的反应为CaO+3C
 CaC2+CO↑,该反应中还原剂为
CaC2+CO↑,该反应中还原剂为②流程中“制Ca(ClO3)2”的化学方程式为
③上述流程中所用Cl2是用MnO2与浓盐酸反应制得。该反应的离子方程式是

(3)“84”消毒液可杀死新冠病毒,其主要成分为NaClO,但在使用过程中不能与含盐酸的除垢剂混用,原因是NaClO与盐酸反应生成Cl2,写出该反应的化学方程式并用双线桥法标出电子的得失:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】配平下列化学方程式(其中(3)用双线桥标出转移的电子数
(1)_____ Cu +______ HNO3(稀) — _____ Cu(NO3)2 +______ NO↑ +______ H2O
(2)______ S+______ NaOH—______ Na2S+______ Na2SO3+______ H2O
(3)______ KClO3+______ HCl— ______ KCl+______ Cl2↑+______ H2O_____________
(4)_____  +
+_____ Fe2++______ —_____ Cr3++_____ Fe3++_______ ,_________________
(1)
(2)
(3)
(4)
 +
+
您最近一年使用:0次



