2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(CH2=CH2)与四氯乙烯(CF2=CF2)的共聚物(ETFE)制成。回答下列问题:
(1)F原子最外层轨道表示式为_______ 。
(2)图a、b、c分别表示C、N、O和F的气态原子逐级失去电子所需能量(纵坐标的标度不同)。失去最外层的一个电子所需能量的变化图是_______ (填标号),判断的根据是_______ ,失去三个电子的变化图是_______ (填标号)。

(3)上图四种元素中,原子核外s亚层电子数与p亚层电子数相同的元素在周期表中的位置是_______ ,其形成的氢化物的沸点_______ H2S的沸点(填>、<或=),理由是_______ 。
(4)聚四氯乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因_______ 。
(5)FTFE_______ (填“有”、“没有”)固定熔沸点,其结构简式为:_______ 。
(1)F原子最外层轨道表示式为
(2)图a、b、c分别表示C、N、O和F的气态原子逐级失去电子所需能量(纵坐标的标度不同)。失去最外层的一个电子所需能量的变化图是

(3)上图四种元素中,原子核外s亚层电子数与p亚层电子数相同的元素在周期表中的位置是
(4)聚四氯乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因
(5)FTFE
更新时间:2022-11-17 16:16:15
|
相似题推荐
解答题-有机推断题
|
较难
(0.4)
【推荐1】下图中A、B、C、D、E、F、G、H均为有机化合物,转化关系如图所示:

根据下面给出的信息回答问题:
(1)有机化合物A的相对分子质量小于60,A能发生银镜反应,1mol A在催化剂作用下能与3mol H2反应生成B,则A的结构简式是_________________ ,由A生成B的反应类型是__________________ ;
(2)B在浓硫酸中加热可生成C,C在催化剂作用下可聚合生成高分子化合物D,由C生成D的化学方程式是__________________________________________________________________ ;
(3)①芳香化合物E的分子式C8H8Cl2,E的苯环上的一溴取代物只有一种,则E可能结构简式是__________________________________________________________________ (写两种)
②E在NaOH水溶液中可转变为F,F用高锰酸钾酸性溶液氧化生成G(C8H6O4)。1molG与足量的NaHCO3溶液反应可放出44.8LCO2(标准状况),由此确定E的结构简式是__________________ ;
(4)G和足量的B在浓硫酸催化作用下加热反应可生成H,则由G和B生成H的化学方程式是______________________________________________________ ,该反应的反应类型是_____________ 。

根据下面给出的信息回答问题:
(1)有机化合物A的相对分子质量小于60,A能发生银镜反应,1mol A在催化剂作用下能与3mol H2反应生成B,则A的结构简式是
(2)B在浓硫酸中加热可生成C,C在催化剂作用下可聚合生成高分子化合物D,由C生成D的化学方程式是
(3)①芳香化合物E的分子式C8H8Cl2,E的苯环上的一溴取代物只有一种,则E可能结构简式是
②E在NaOH水溶液中可转变为F,F用高锰酸钾酸性溶液氧化生成G(C8H6O4)。1molG与足量的NaHCO3溶液反应可放出44.8LCO2(标准状况),由此确定E的结构简式是
(4)G和足量的B在浓硫酸催化作用下加热反应可生成H,则由G和B生成H的化学方程式是
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
【推荐2】已知A、B、C、D、E、F六种有机物存在如下转化关系, E在核磁共振氢谱中出现三组峰,其峰面积之比为6:1:1,F能使Br2的CCl4溶液褪色。回答下列问题:
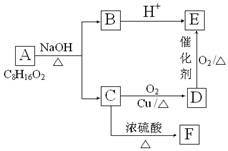
(1)C和E的官能团名称:C___________ ,E____________ 。
(2)由F生成高聚物的化学方程式_______________________________________ 。
(3)六种有机物中能跟Na反应的是______________________ (填字母)。
(4)由A生成B和C的化学反应方程式为____________________________________ 。
(5)D在一定条件下生成C的化学反应方程式为_______________________________ 。

(1)C和E的官能团名称:C
(2)由F生成高聚物的化学方程式
(3)六种有机物中能跟Na反应的是
(4)由A生成B和C的化学反应方程式为
(5)D在一定条件下生成C的化学反应方程式为
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
名校
【推荐3】优良的有机溶剂对孟烷、耐热型特种高分子功能材料PMnMA的合成路线如下:
①由B生成对孟烷的反应类型是___________ 。对孟烷的一氯代物有___________ 种。
②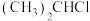 与A生成B的化学方程式是
与A生成B的化学方程式是___________ 。
③A的同系物中相对分子质量最小的物质是___________ 。
(2)1.08g的C与饱和溴水完全反应生成3.45g白色沉淀。E不能使 的
的 溶液褪色。
溶液褪色。
①F的官能团是___________ 。
②C的结构简式是___________ 。C的属于芳香化合物且具有官能团―OH的同分异构体有___________ 种。
③反应I的化学方程式是___________ 。
(3)下列说法正确的是___________。
(4)G的核磁共振氢谱有3种峰,其峰面积之比为3∶2∶1.G与 反应放出
反应放出 。
。
反应Ⅱ的化学方程式是___________ 。

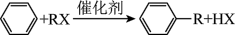 (R为烷基,X为卤原子)
(R为烷基,X为卤原子)
①由B生成对孟烷的反应类型是
②
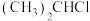 与A生成B的化学方程式是
与A生成B的化学方程式是③A的同系物中相对分子质量最小的物质是
(2)1.08g的C与饱和溴水完全反应生成3.45g白色沉淀。E不能使
 的
的 溶液褪色。
溶液褪色。①F的官能团是
②C的结构简式是
③反应I的化学方程式是
(3)下列说法正确的是___________。
| A.B可使酸性高锰酸钾溶液褪色 | B.C不存在醛类同分异构体 |
| C.D的酸性比E弱 | D.E的沸点高于对孟烷 |
(4)G的核磁共振氢谱有3种峰,其峰面积之比为3∶2∶1.G与
 反应放出
反应放出 。
。反应Ⅱ的化学方程式是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】含钴化合物在机械制造、磁性材料等领域具有广泛的应用,请回答下列问题:
(1)基态Co3+的价电子排布图为____ 。
(2)钴的配合物[Co(NH3)5Br](NO3)2
①第一电离能N_____ O(填“大于”、“小于”或“不能确定”);两种配位原子的杂化轨道类型均为____ ;
②钴离子周围配位键数目(配位数)是___ ;N03-的空间构型为____ ;
③已知Br的含氧酸酸性由强到弱的顺序为HBrO4>HBrO3>HBrO2>HBrO,其原因是____ 。
(3)某钴氧化物晶体具有CoO2的层状结构如下图所示(小球表示Co,大球表示O)。下列用粗线面出的结构单元不能描述CoO2)的化学组成的是_____

(4)Co的另一种氧化物的晶胞如图,已知钴原子的半径为apm,氧原子的半径为bpm,它们在晶体中是紧密接触的,钴原子填在氧原子的___ 填“正八面体”、“正四面体”或“立方体”)空隙;钴原子与跟它次近邻的氧原子之间的距离为____ ;在该钴的氧化物晶体中原子的空间利用率为____ (均用含a、b的计算表达式表示)。

(1)基态Co3+的价电子排布图为
(2)钴的配合物[Co(NH3)5Br](NO3)2
①第一电离能N
②钴离子周围配位键数目(配位数)是
③已知Br的含氧酸酸性由强到弱的顺序为HBrO4>HBrO3>HBrO2>HBrO,其原因是
(3)某钴氧化物晶体具有CoO2的层状结构如下图所示(小球表示Co,大球表示O)。下列用粗线面出的结构单元不能描述CoO2)的化学组成的是

(4)Co的另一种氧化物的晶胞如图,已知钴原子的半径为apm,氧原子的半径为bpm,它们在晶体中是紧密接触的,钴原子填在氧原子的

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】铁被称为“第一金属”,铁及其化合物在生产、生活中有广泛用途。
(1)铁原子核外电子发生跃迁时会吸收或释放不同的光,可以用___________ 摄取铁元素的原子光谱。
(2)FeCl3的熔点为306℃,沸点为315℃。由此可知FeCl3属于______ 晶体。FeSO4常作净水剂和补铁剂,SO42-的立体构型是____________ 。
(3) 铁氰化钾K3[Fe(CN)6]是检验Fe2+的重要试剂。
①基态N原子的轨道表示式为___________ 。
②写出一种与铁氰化钾中配体互为等电子体的极性分子的化学式_______ 。
③铁氰化钾中,所涉及的元素的第一电离能由大到小的顺序为____________ 。
④铁氰化钾中,不存在___________ (填字母标号)。
A.离子键 B. σ键 C. π键 D.氢键 E.金属键
(4)有机金属配位化合物二茂铁[(C5H5)2Fe]是汽油中的抗震剂。分子中的大 π键可用符号πmn表示,其中m代表参与形成大π键的原子数, n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π66),则 中的大π键应表示为
中的大π键应表示为________ ,其中碳原子的杂化方式为________ 。
(5)羰基铁[Fe(CO)5]可用作催化剂、汽油抗爆剂等。1mol [Fe(CO)5]分子中含_____ molσ键。
(6)某种磁性氮化铁的结构如图所示,N随机排列在Fe构成的正四 面体空隙中。其中铁原子周围最近的铁原子个数为_____ ;六棱柱底边长为acm,高为c cm,阿伏加 德罗常数的值为NA,则该磁性氮化铁的晶体密度为_________ g/cm3(列出计算式)。

(1)铁原子核外电子发生跃迁时会吸收或释放不同的光,可以用
(2)FeCl3的熔点为306℃,沸点为315℃。由此可知FeCl3属于
(3) 铁氰化钾K3[Fe(CN)6]是检验Fe2+的重要试剂。
①基态N原子的轨道表示式为
②写出一种与铁氰化钾中配体互为等电子体的极性分子的化学式
③铁氰化钾中,所涉及的元素的第一电离能由大到小的顺序为
④铁氰化钾中,不存在
A.离子键 B. σ键 C. π键 D.氢键 E.金属键
(4)有机金属配位化合物二茂铁[(C5H5)2Fe]是汽油中的抗震剂。分子中的大 π键可用符号πmn表示,其中m代表参与形成大π键的原子数, n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π66),则
 中的大π键应表示为
中的大π键应表示为(5)羰基铁[Fe(CO)5]可用作催化剂、汽油抗爆剂等。1mol [Fe(CO)5]分子中含
(6)某种磁性氮化铁的结构如图所示,N随机排列在Fe构成的正四 面体空隙中。其中铁原子周围最近的铁原子个数为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】由第ⅢA和第ⅤA元素所形成的化合物种类繁多,它们是探测器、激光器、微波器的重要材料,请根据材料回答以下问题:
(1)基态As原子的电子排布式为[Ar]___________ 。N、P、As的第一电离能从大到小的顺序是:___________ 。
(2)除了已知的氮气,科学家还先后研究出了 、
、 、
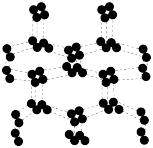
、 、高聚氮等物质。而高聚氮结构具有空间网状结构,如图所示,则
、高聚氮等物质。而高聚氮结构具有空间网状结构,如图所示,则 的沸点
的沸点___________ (填“>”、“<”或“=”)高聚氮的沸点,原因是___________ 。
(3)氧原子价电子层上的电子可以进行重排以便提供一个空轨道与氮原子形成配位键,该氧原子重排后的价电子排布图为___________ ,电子重排后的氧原子能量有所升高,原因是不符合___________ (填“泡利原理”或“洪特规则”)。
(4)自然界中不存在单质硼,硼的氢化物也很少,主要存在的是硼的化合物,根据下表数据分析原因是___________ 。
(5) 晶体的晶胞参数为
晶体的晶胞参数为 ,
, ,α=β=90°,
,α=β=90°, =120°,结构如下图:
=120°,结构如下图:
①已知 的分数坐标为(0,0,0)、(0,0,
的分数坐标为(0,0,0)、(0,0, ),(
),( ,
, ,
, ),(
),( ,
, ,
, ),(
),( ,
, ,
, )和 (
)和 ( ,
, ,
, ),晶胞中
),晶胞中 的个数为
的个数为___________ 。
②下图是上述 晶胞的某个截面,共含有10个
晶胞的某个截面,共含有10个 ,其中6个已经画出(图中的○)请在图中用○将剩余的
,其中6个已经画出(图中的○)请在图中用○将剩余的 画出。
画出。___________

③此晶体的密度为___________ g/cm3 (列出计算式即可)。
(1)基态As原子的电子排布式为[Ar]
(2)除了已知的氮气,科学家还先后研究出了
 、
、 、
、 、高聚氮等物质。而高聚氮结构具有空间网状结构,如图所示,则
、高聚氮等物质。而高聚氮结构具有空间网状结构,如图所示,则 的沸点
的沸点
(3)氧原子价电子层上的电子可以进行重排以便提供一个空轨道与氮原子形成配位键,该氧原子重排后的价电子排布图为
(4)自然界中不存在单质硼,硼的氢化物也很少,主要存在的是硼的化合物,根据下表数据分析原因是
| 化学键 |  |  |  |
| 键能 (kJ/mol) | 389 | 561 | 293 |
(5)
 晶体的晶胞参数为
晶体的晶胞参数为 ,
, ,α=β=90°,
,α=β=90°, =120°,结构如下图:
=120°,结构如下图:
①已知
 的分数坐标为(0,0,0)、(0,0,
的分数坐标为(0,0,0)、(0,0, ),(
),( ,
, ,
, ),(
),( ,
, ,
, ),(
),( ,
, ,
, )和 (
)和 ( ,
, ,
, ),晶胞中
),晶胞中 的个数为
的个数为②下图是上述
 晶胞的某个截面,共含有10个
晶胞的某个截面,共含有10个 ,其中6个已经画出(图中的○)请在图中用○将剩余的
,其中6个已经画出(图中的○)请在图中用○将剩余的 画出。
画出。
③此晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐1】VA族元素及其化合物在材料等方面有重要用途。根据所学知识回答下列问题:
(1)基态砷原子处于最高能级的电子云轮廓图为_______ 形。
(2)NH3、PH3、AsH3是同主族元素的氢化物,其中键角最小的是________ 。
(3)叠氮化钠(NaN3)用于汽车的安气囊中,当发生车祸时迅速分解放出氮气,使安全气囊充气。可与酸反应生成叠氮酸(HN3),叠氮酸中3个氮原子的杂化类型分别为___________ (不分先后)。
(4)N原子之间可以形成π键,而As原子之间较难形成π键。从原子结构角度分析,其原因为________ 。
(5)往硫酸铜溶液中加入过量氨水,可生成配离子[Cu(NH3)4]2+。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是______ 。
(6)磷的含氧酸有很多种,其中有磷酸(H3PO4)、亚磷酸(H3PO3)、次磷酸(H3PO2)等。
①已知NaH2PO2是次磷酸的正盐,则1molH3PO2中含有的σ键的物质的量为___ mol。
②磷酸通过分子间脱水缩合形成多磷酸,如:
如果有n个磷酸分子间脱水形成链状的多磷酸,则相应的酸根可写为_______ 。
(7)HgCl2和不同浓度NH3–NH4Cl反应得到某种含汞化合物的晶胞结构(有四个等同的小立方体)如图所示。(部分微粒不在晶胞内,每个Hg原子均处于小立方体的面心)

写出该含汞化合物的化学式:______ 。则该晶体的密度ρ=_____ g·cm-3(设阿伏加德罗常数的值为NA,用含a、NA的代数式表示)。
(1)基态砷原子处于最高能级的电子云轮廓图为
(2)NH3、PH3、AsH3是同主族元素的氢化物,其中键角最小的是
(3)叠氮化钠(NaN3)用于汽车的安气囊中,当发生车祸时迅速分解放出氮气,使安全气囊充气。可与酸反应生成叠氮酸(HN3),叠氮酸中3个氮原子的杂化类型分别为
(4)N原子之间可以形成π键,而As原子之间较难形成π键。从原子结构角度分析,其原因为
(5)往硫酸铜溶液中加入过量氨水,可生成配离子[Cu(NH3)4]2+。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是
(6)磷的含氧酸有很多种,其中有磷酸(H3PO4)、亚磷酸(H3PO3)、次磷酸(H3PO2)等。
①已知NaH2PO2是次磷酸的正盐,则1molH3PO2中含有的σ键的物质的量为
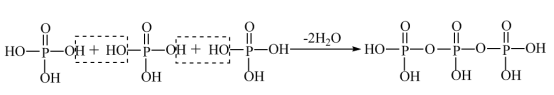
②磷酸通过分子间脱水缩合形成多磷酸,如:

如果有n个磷酸分子间脱水形成链状的多磷酸,则相应的酸根可写为
(7)HgCl2和不同浓度NH3–NH4Cl反应得到某种含汞化合物的晶胞结构(有四个等同的小立方体)如图所示。(部分微粒不在晶胞内,每个Hg原子均处于小立方体的面心)

写出该含汞化合物的化学式:
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
真题
解题方法
【推荐2】 失水后可转为
失水后可转为 ,与
,与 可联合制备铁粉精
可联合制备铁粉精 和
和 。
。
I. 结构如图所示。
结构如图所示。
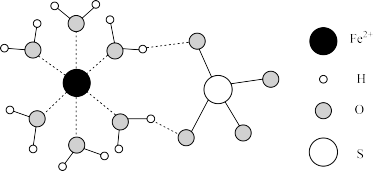
(1) 价层电子排布式为
价层电子排布式为___________ 。
(2)比较 和
和 分子中的键角大小并给出相应解释:
分子中的键角大小并给出相应解释:___________ 。
(3) 与
与 和
和 的作用分别为
的作用分别为___________ 。
II. 晶胞为立方体,边长为
晶胞为立方体,边长为 ,如图所示。
,如图所示。
(4)①与 紧邻的阴离子个数为
紧邻的阴离子个数为___________ 。
②晶胞的密度为
___________  。
。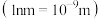
(5)以 为燃料,配合
为燃料,配合 可以制备铁粉精
可以制备铁粉精 和
和 。结合图示解释可充分实现能源和资源有效利用的原因为
。结合图示解释可充分实现能源和资源有效利用的原因为___________ 。
 失水后可转为
失水后可转为 ,与
,与 可联合制备铁粉精
可联合制备铁粉精 和
和 。
。I.
 结构如图所示。
结构如图所示。
(1)
 价层电子排布式为
价层电子排布式为(2)比较
 和
和 分子中的键角大小并给出相应解释:
分子中的键角大小并给出相应解释:(3)
 与
与 和
和 的作用分别为
的作用分别为II.
 晶胞为立方体,边长为
晶胞为立方体,边长为 ,如图所示。
,如图所示。(4)①与
 紧邻的阴离子个数为
紧邻的阴离子个数为②晶胞的密度为

 。
。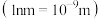

(5)以
 为燃料,配合
为燃料,配合 可以制备铁粉精
可以制备铁粉精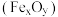 和
和 。结合图示解释可充分实现能源和资源有效利用的原因为
。结合图示解释可充分实现能源和资源有效利用的原因为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】氢能是一种极具发展潜力的清洁能源,下列物质都是具有广阔应用前景的储氢材料。按要求回答下列问题:
(1)氢化钠( )是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原剂的电子式为
)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原剂的电子式为___________ 。
(2)钛系贮氢合金中的钛锰合金具成本低,吸氢量大,室温下易活化等优点,基态钛的价层电子排布式为___________ 。
(3) (氨硼烷)具有很高的储氢容量及相对低的放氢温度(
(氨硼烷)具有很高的储氢容量及相对低的放氢温度(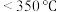 )而成为颇具潜力的化学储氢材料之一,它可通过环硼氮烷、
)而成为颇具潜力的化学储氢材料之一,它可通过环硼氮烷、 与
与 进行合成,则涉及的元素H、B、C、N、O电负性最大的是
进行合成,则涉及的元素H、B、C、N、O电负性最大的是___________ ,键角:
___________  (填“
(填“ ”或“
”或“ ”)。
”)。
(4)咔唑(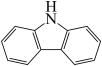 )是一种新型有机液体储氢材料,它的沸点比(
)是一种新型有机液体储氢材料,它的沸点比(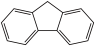 )的高,其主要原因是
)的高,其主要原因是___________ 。
(5)氢气的安全贮存和运输是氢能应用的关键,铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。
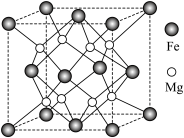
①距离 原子最近的
原子最近的 原子个数是
原子个数是___________ 。
②铁镁合金的化学式为___________ 。
③若该晶胞的晶胞边长为dnm,阿伏加德罗常数为NA,则该合金的密度为___________  。
。
④若该晶体储氢时, 分子在晶胞的体心和棱心位置,则含Mg 48g的该储氢合金可储存标准状况下
分子在晶胞的体心和棱心位置,则含Mg 48g的该储氢合金可储存标准状况下 的体积约为
的体积约为___________ L。
(1)氢化钠(
 )是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原剂的电子式为
)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原剂的电子式为(2)钛系贮氢合金中的钛锰合金具成本低,吸氢量大,室温下易活化等优点,基态钛的价层电子排布式为
(3)
 (氨硼烷)具有很高的储氢容量及相对低的放氢温度(
(氨硼烷)具有很高的储氢容量及相对低的放氢温度(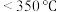 )而成为颇具潜力的化学储氢材料之一,它可通过环硼氮烷、
)而成为颇具潜力的化学储氢材料之一,它可通过环硼氮烷、 与
与 进行合成,则涉及的元素H、B、C、N、O电负性最大的是
进行合成,则涉及的元素H、B、C、N、O电负性最大的是
 (填“
(填“ ”或“
”或“ ”)。
”)。(4)咔唑(
 )是一种新型有机液体储氢材料,它的沸点比(
)是一种新型有机液体储氢材料,它的沸点比( )的高,其主要原因是
)的高,其主要原因是(5)氢气的安全贮存和运输是氢能应用的关键,铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。

①距离
 原子最近的
原子最近的 原子个数是
原子个数是②铁镁合金的化学式为
③若该晶胞的晶胞边长为dnm,阿伏加德罗常数为NA,则该合金的密度为
 。
。④若该晶体储氢时,
 分子在晶胞的体心和棱心位置,则含Mg 48g的该储氢合金可储存标准状况下
分子在晶胞的体心和棱心位置,则含Mg 48g的该储氢合金可储存标准状况下 的体积约为
的体积约为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】生物质能是一种洁净、可再生的能源。.生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
⑴上述反应的催化剂含有Cu、Zn、AI等元素。写出基态Cu原子的核外电子排布式:___________ 。
⑵根据等电子原理.写出CO分子的电子式:______________ 。
(3)甲醇催化氧化可得到甲醛,甲醇的沸点比甲醛的高,其主要原因是___________________ 。
(4)胆矾结构示意图可简单表示如下,回答下列问题。
①胆矾晶体中存在的作用力有:__________________
②胆钒晶体溶于水呈蓝色,滴加少量氨水之后得到蓝色沉淀。再滴加氨水,沉淀又逐渐溶解。请写出蓝色沉淀溶解的离子方程式:_________________ 。
⑴上述反应的催化剂含有Cu、Zn、AI等元素。写出基态Cu原子的核外电子排布式:
⑵根据等电子原理.写出CO分子的电子式:
(3)甲醇催化氧化可得到甲醛,甲醇的沸点比甲醛的高,其主要原因是
(4)胆矾结构示意图可简单表示如下,回答下列问题。
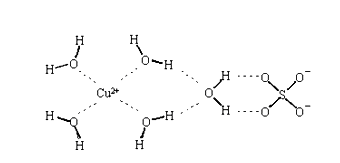
①胆矾晶体中存在的作用力有:
②胆钒晶体溶于水呈蓝色,滴加少量氨水之后得到蓝色沉淀。再滴加氨水,沉淀又逐渐溶解。请写出蓝色沉淀溶解的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐2】锂离子电池是近年来的研究热点,常见的锂离子聚合物电池材料有石墨、LiAsF6、LiPF6、LiMn2O4等。回答下列问题:
(1)As的最高能级组的电子排布式为_______ ,Li、O、P、As四种元素电负性由大到小的顺序为_______ (填元素符号)。
(2)LiPF6的阴离子的空间构型为_______ 。
(3)一种类石墨的聚合物g—C3N4可由三聚氰胺( )制得。三聚氰胺分子中氮原子杂化类型是
)制得。三聚氰胺分子中氮原子杂化类型是_______ ;三聚氰胺分子不溶于冷水,溶于热水,主要原因是_______ 。
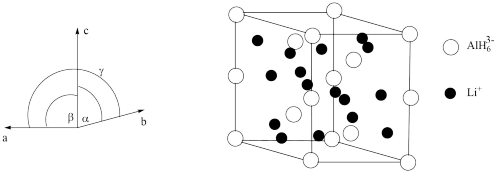
(4)尖晶石结构的LiMn2O4是一种常用的正极材料。已知一种LiMn2O4晶胞可看成由A、B单元按Ⅲ方式交替排布构成,“○”表示O2−。
 ①“●”表示的微粒是
①“●”表示的微粒是_______ (填元素符号)
②若该晶胞的晶胞参数为apm,设NA为阿伏加德罗常数的值,该晶体的密度为_______ g·cm-3(列出计算表达式,不必化简)
(1)As的最高能级组的电子排布式为
(2)LiPF6的阴离子的空间构型为
(3)一种类石墨的聚合物g—C3N4可由三聚氰胺(
 )制得。三聚氰胺分子中氮原子杂化类型是
)制得。三聚氰胺分子中氮原子杂化类型是(4)尖晶石结构的LiMn2O4是一种常用的正极材料。已知一种LiMn2O4晶胞可看成由A、B单元按Ⅲ方式交替排布构成,“○”表示O2−。
 ①“●”表示的微粒是
①“●”表示的微粒是②若该晶胞的晶胞参数为apm,设NA为阿伏加德罗常数的值,该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】 是一种高迁移率的新型热电材料,回答下列问题:
是一种高迁移率的新型热电材料,回答下列问题:
(1) 为
为 族元素,单质
族元素,单质 与干燥
与干燥 反应生成
反应生成 。常温常压下
。常温常压下 为无色液体,
为无色液体, 空间构型为
空间构型为___________ ,其固体的晶体类型为___________ 。
(2) 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为___________ ,试写出一种与它们互为等电子体的阳离子的化学式___________ 。
(3) 原子的价层电子排布式为
原子的价层电子排布式为___________ , 与
与 两元素中第一电离能较大的是
两元素中第一电离能较大的是___________ 。
(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系 的晶胞结构如下图所示,晶胞棱边夹角均为
的晶胞结构如下图所示,晶胞棱边夹角均为 ,晶胞中部分原子的分数坐标如下表所示。
,晶胞中部分原子的分数坐标如下表所示。

 晶体的密度为
晶体的密度为___________  。(可不化简,已知相对原子质量:
。(可不化简,已知相对原子质量: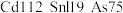 )
)
 是一种高迁移率的新型热电材料,回答下列问题:
是一种高迁移率的新型热电材料,回答下列问题:(1)
 为
为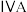 族元素,单质
族元素,单质 与干燥
与干燥 反应生成
反应生成 。常温常压下
。常温常压下 为无色液体,
为无色液体, 空间构型为
空间构型为(2)
 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为(3)
 原子的价层电子排布式为
原子的价层电子排布式为 与
与 两元素中第一电离能较大的是
两元素中第一电离能较大的是(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系
 的晶胞结构如下图所示,晶胞棱边夹角均为
的晶胞结构如下图所示,晶胞棱边夹角均为 ,晶胞中部分原子的分数坐标如下表所示。
,晶胞中部分原子的分数坐标如下表所示。| 坐标 原子 | x | y | z |
 | 0 | 0 | 0 |
 | 0 | 0 | 0.5 |
 | 0.25 | 0.25 | 0.125 |

 晶体的密度为
晶体的密度为 。(可不化简,已知相对原子质量:
。(可不化简,已知相对原子质量: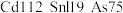 )
)
您最近一年使用:0次



