回答下列问题:
(1)已知:①5.6L (标准状况下)②
(标准状况下)② 个
个 分子③4.8g
分子③4.8g ④4℃时,5.4mL水,其中含有的氢原子数由大到小的顺序为
④4℃时,5.4mL水,其中含有的氢原子数由大到小的顺序为_______ 。
(2)在标准状况下,将VLHCl溶于0.1L水中,所得溶液的密度为 ,则形成溶液的物质的量浓度为
,则形成溶液的物质的量浓度为_______  。
。
(3)某工厂废液中含有 ,排放废液前要将废液中的
,排放废液前要将废液中的 还原成
还原成 ,取100mL此工厂的废液样品进行实验时,恰好消耗纯净NaHSO3固体3.12g。则此废液中含有
,取100mL此工厂的废液样品进行实验时,恰好消耗纯净NaHSO3固体3.12g。则此废液中含有 的浓度为
的浓度为_______  。
。
(4)联氨(又称联肼, ,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。实验室中可用次氯酸钠溶液与氨气反应制备联氨(
,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。实验室中可用次氯酸钠溶液与氨气反应制备联氨( ),反应的化学方程式为
),反应的化学方程式为_______ 。
(1)已知:①5.6L
 (标准状况下)②
(标准状况下)② 个
个 分子③4.8g
分子③4.8g ④4℃时,5.4mL水,其中含有的氢原子数由大到小的顺序为
④4℃时,5.4mL水,其中含有的氢原子数由大到小的顺序为(2)在标准状况下,将VLHCl溶于0.1L水中,所得溶液的密度为
 ,则形成溶液的物质的量浓度为
,则形成溶液的物质的量浓度为 。
。(3)某工厂废液中含有
 ,排放废液前要将废液中的
,排放废液前要将废液中的 还原成
还原成 ,取100mL此工厂的废液样品进行实验时,恰好消耗纯净NaHSO3固体3.12g。则此废液中含有
,取100mL此工厂的废液样品进行实验时,恰好消耗纯净NaHSO3固体3.12g。则此废液中含有 的浓度为
的浓度为 。
。(4)联氨(又称联肼,
 ,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。实验室中可用次氯酸钠溶液与氨气反应制备联氨(
,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。实验室中可用次氯酸钠溶液与氨气反应制备联氨( ),反应的化学方程式为
),反应的化学方程式为
更新时间:2022-10-30 21:39:35
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】I.有下列物质:①Fe ②NH4Cl溶液③Na2O ④Cu(OH)2 ⑤熔融的MgCl2 ⑥H2SO4 ⑦CO2 ⑧C2H5OH(酒精)(用序号作答 )。其中属于电解质的有_____________ ,属于非电解质的有________________ 。
Ⅱ、某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是________ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子所发生的离子方程式为______________________________________ 。
(3)取(2)中的滤液,加入过量的NaOH出现白色沉淀,说明原溶液中肯定有的该离子所发生的离子方程式为___________________________ 。
(4)通过以上实验确定原溶液中一定含有的阳离子是_________ ,不能确定的阳离子是_________ 。
(5)原溶液可能大量存在的阴离子是下列的________ 。
A.Cl- B.NO C.CO
C.CO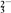 D.OH-
D.OH-
Ⅲ.现有M、N两种气态化合物,其摩尔质量之比为2:1,试回答下列问题:
(1)同温同压下,M、N气体的密度之比为____________ 。
(2)相同温度下,在两个相同体积的密闭容器中分别充入M、N,若两个容器中气体的密度相等,则两个容器中的压强之比为____________ 。
Ⅱ、某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子所发生的离子方程式为
(3)取(2)中的滤液,加入过量的NaOH出现白色沉淀,说明原溶液中肯定有的该离子所发生的离子方程式为
(4)通过以上实验确定原溶液中一定含有的阳离子是
(5)原溶液可能大量存在的阴离子是下列的
A.Cl- B.NO
 C.CO
C.CO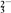 D.OH-
D.OH-Ⅲ.现有M、N两种气态化合物,其摩尔质量之比为2:1,试回答下列问题:
(1)同温同压下,M、N气体的密度之比为
(2)相同温度下,在两个相同体积的密闭容器中分别充入M、N,若两个容器中气体的密度相等,则两个容器中的压强之比为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】硝酸工业尾气中氮氧化物(NO 和NO2)是主要的大气污染物之一,可用氨氧混合气体进行选择性还原处理。其主要反应原理如下:4NO+4NH3+O2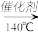 4N2+6H2O 6NO2+8NH3
4N2+6H2O 6NO2+8NH3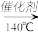 7N2+12H2O,某硝酸厂排放的尾气中氮氧化合物的含量为2490mg/m3(体积已换算成标准状况),其中NO NO2的物质的量比为4:1。设尾气中氮氧化物与氨氧混合气恰好完全反应。
7N2+12H2O,某硝酸厂排放的尾气中氮氧化合物的含量为2490mg/m3(体积已换算成标准状况),其中NO NO2的物质的量比为4:1。设尾气中氮氧化物与氨氧混合气恰好完全反应。
(1)尾气中氮氧化物的平均相对原子量为_____________ ;尾气中NO的含量为_____ mg/m3。
(2)要处理5m3的尾气,需要氨氧混合气的体积为_______ L。
另一种处理氮氧化物的方法是用烧碱进行吸收,产物为NaNO2、NaNO3和H2O。现有含0.5mol氮氧化物的尾气,恰好被一定体积25%NaOH溶液(密度1.28g/cm3)完全吸收。
(3)NaOH溶液的物质的量浓度为_____________ mol/L,体积为_____ mL。
(4)已知反应后溶液含有0.35molNaNO2。若将尾气NO 和NO2的平均组成用NOx表示,则x=______
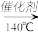 4N2+6H2O 6NO2+8NH3
4N2+6H2O 6NO2+8NH3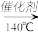 7N2+12H2O,某硝酸厂排放的尾气中氮氧化合物的含量为2490mg/m3(体积已换算成标准状况),其中NO NO2的物质的量比为4:1。设尾气中氮氧化物与氨氧混合气恰好完全反应。
7N2+12H2O,某硝酸厂排放的尾气中氮氧化合物的含量为2490mg/m3(体积已换算成标准状况),其中NO NO2的物质的量比为4:1。设尾气中氮氧化物与氨氧混合气恰好完全反应。(1)尾气中氮氧化物的平均相对原子量为
(2)要处理5m3的尾气,需要氨氧混合气的体积为
另一种处理氮氧化物的方法是用烧碱进行吸收,产物为NaNO2、NaNO3和H2O。现有含0.5mol氮氧化物的尾气,恰好被一定体积25%NaOH溶液(密度1.28g/cm3)完全吸收。
(3)NaOH溶液的物质的量浓度为
(4)已知反应后溶液含有0.35molNaNO2。若将尾气NO 和NO2的平均组成用NOx表示,则x=
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】钠、镁、铝是重要的金属。请根据钠、镁、铝的性质回答下列问题:
(1)将共0.4molMg、Al的混合物用盐酸完全溶解,放出标准状况下11.2L气体,该混合物中Mg、Al的物质的量之比为_______ 。
(2)相同质量的钠在下列哪种情况下产生的氢气最多_______ 。
A.放在水中 B.放在足量盐酸中
C.放在足量CuSO4溶液中 D.用刺有小孔的铝箔包好放入足量水中
(3)铝分别与足量的NaOH溶液和盐酸反应,若两个反应在相同状况下放出等量的气体,则反应中消耗的NaOH和HCl物质的量之比为_______ 。
(4)常温下镁、铝都具有较强的抗腐蚀性,主要原因是_______ 。
(5)将铝片投入到下列溶液中,铝片不溶解的是_______ 。
A.NaOH溶液 B.NaCl溶液 C.CuSO4溶液 D.HCl溶液
(1)将共0.4molMg、Al的混合物用盐酸完全溶解,放出标准状况下11.2L气体,该混合物中Mg、Al的物质的量之比为
(2)相同质量的钠在下列哪种情况下产生的氢气最多
A.放在水中 B.放在足量盐酸中
C.放在足量CuSO4溶液中 D.用刺有小孔的铝箔包好放入足量水中
(3)铝分别与足量的NaOH溶液和盐酸反应,若两个反应在相同状况下放出等量的气体,则反应中消耗的NaOH和HCl物质的量之比为
(4)常温下镁、铝都具有较强的抗腐蚀性,主要原因是
(5)将铝片投入到下列溶液中,铝片不溶解的是
A.NaOH溶液 B.NaCl溶液 C.CuSO4溶液 D.HCl溶液
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】将xgFe、FeO和Fe2O3混合物分成两等份,向其中一份中滴加500mL稀硝酸,固体恰好完全溶解并产生标准状况下NO气体aL,溶液中Fe元素均以+3价形式存在,另一份固体与足量H2反应质量减少yg。根据以上数据计算稀硝酸的浓度为___ mol·L-1(写出计算过程)。
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】为探究一种矿石(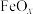 )的组成,已知矿石不含其他杂质,铁元素呈+2、+3价,氧元素为-2价。称取1.504g样品用足量的稀硫酸溶解,所得溶液用
)的组成,已知矿石不含其他杂质,铁元素呈+2、+3价,氧元素为-2价。称取1.504g样品用足量的稀硫酸溶解,所得溶液用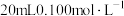 的
的 溶液恰好使+2价铁元素氧化为+3价,同时Cr元素被还原为+3价。另取1.504g样品用足量的
溶液恰好使+2价铁元素氧化为+3价,同时Cr元素被还原为+3价。另取1.504g样品用足量的 还原,得固体1.120g。请回答:
还原,得固体1.120g。请回答:
(1)实验用稀硫酸溶解矿石而不用盐酸,原因是___________ (用文字或用方程式表述均可)。
(2)矿石的化学组成为___________ 。
(3)若无“另取1.504g样品用足量的 还原,得固体1.120g”的数据,能否求得该矿石的组成:
还原,得固体1.120g”的数据,能否求得该矿石的组成:___________ (填“能”或“否”)。
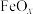 )的组成,已知矿石不含其他杂质,铁元素呈+2、+3价,氧元素为-2价。称取1.504g样品用足量的稀硫酸溶解,所得溶液用
)的组成,已知矿石不含其他杂质,铁元素呈+2、+3价,氧元素为-2价。称取1.504g样品用足量的稀硫酸溶解,所得溶液用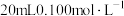 的
的 溶液恰好使+2价铁元素氧化为+3价,同时Cr元素被还原为+3价。另取1.504g样品用足量的
溶液恰好使+2价铁元素氧化为+3价,同时Cr元素被还原为+3价。另取1.504g样品用足量的 还原,得固体1.120g。请回答:
还原,得固体1.120g。请回答:(1)实验用稀硫酸溶解矿石而不用盐酸,原因是
(2)矿石的化学组成为
(3)若无“另取1.504g样品用足量的
 还原,得固体1.120g”的数据,能否求得该矿石的组成:
还原,得固体1.120g”的数据,能否求得该矿石的组成:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)硫酸在下列用途或反应中各表现的性质是(用字母填在横线上)
A.难挥发性 B.酸性 C.吸水性 D.脱水性 E.强氧化性 F.催化作用
①敞口放置浓硫酸时,质量增加_______ ,
②浓硫酸使润湿蓝色石蕊试纸先变红后又变黑___________ ,
③浓硫酸与铜反应_____________ ;
(2)氮氧化物也是造成酸雨的成分之一,治理汽车尾气中NO和CO的一种方法是:在汽车的排气管上装一个催化转换装置,使NO和CO反应,生成无毒气体,反应的化学方程式是_________________________________________ ;
(3)喷泉是一种常见的自然现象,其产生的原因是存在压强差;提供如图的装置,请说明引发喷泉的方法____________________________________ ;

(4)为了测定某铜银合金的成分,将17.2 g合金溶于40 mL 12.25 mol/L的浓硝酸中,待合金完全溶解后,收集到3.36 L(标准状况下)气体(气体为NO和NO2混合气体),并测得溶液中c(H+)=1mol/L,假设反应后溶液的体积仍为40 mL,则合金中铜的质量分数为_______________ ( 保留两位有效数字),收集到的混合气体中NO与NO2的体积之比为___________ 。
A.难挥发性 B.酸性 C.吸水性 D.脱水性 E.强氧化性 F.催化作用
①敞口放置浓硫酸时,质量增加
②浓硫酸使润湿蓝色石蕊试纸先变红后又变黑
③浓硫酸与铜反应
(2)氮氧化物也是造成酸雨的成分之一,治理汽车尾气中NO和CO的一种方法是:在汽车的排气管上装一个催化转换装置,使NO和CO反应,生成无毒气体,反应的化学方程式是
(3)喷泉是一种常见的自然现象,其产生的原因是存在压强差;提供如图的装置,请说明引发喷泉的方法

(4)为了测定某铜银合金的成分,将17.2 g合金溶于40 mL 12.25 mol/L的浓硝酸中,待合金完全溶解后,收集到3.36 L(标准状况下)气体(气体为NO和NO2混合气体),并测得溶液中c(H+)=1mol/L,假设反应后溶液的体积仍为40 mL,则合金中铜的质量分数为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】将 固体溶于水配成
固体溶于水配成 溶液,其密度为
溶液,其密度为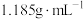 。
。
(1)该溶液中 的物质的量浓度为
的物质的量浓度为___________ 。
(2)该溶液中 的质量分数为
的质量分数为___________ 。
(3)从该溶液中取出 ,其中
,其中 的物质的量浓度为
的物质的量浓度为___________ ,含 的物质的量为
的物质的量为___________ 。
(4)将取出的 溶液加水稀释,稀释后溶液中
溶液加水稀释,稀释后溶液中 的物质的量浓度为
的物质的量浓度为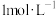 ,稀释后溶液体积为
,稀释后溶液体积为___________  。
。
 固体溶于水配成
固体溶于水配成 溶液,其密度为
溶液,其密度为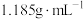 。
。(1)该溶液中
 的物质的量浓度为
的物质的量浓度为(2)该溶液中
 的质量分数为
的质量分数为(3)从该溶液中取出
 ,其中
,其中 的物质的量浓度为
的物质的量浓度为 的物质的量为
的物质的量为(4)将取出的
 溶液加水稀释,稀释后溶液中
溶液加水稀释,稀释后溶液中 的物质的量浓度为
的物质的量浓度为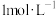 ,稀释后溶液体积为
,稀释后溶液体积为 。
。
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】将一定量的Cl2通入体积为40mL的氢氧化钾溶液中,两者恰好完全反应,测得反应后溶液中有三种含氯元素的离子,其中ClO-物质的量为0.06mol和ClO3-物质的量0.03mol,请按要求完成下列问题
(1)该反应的离子方程式为___________________________________________ 。
(2)该反应中,氧化剂与还原剂物质的量之比为____________________ 。
(3)上述反应中,通入Cl2的物质的量为________ mol,氢氧化钾溶液的物质的量浓度为________ mol/L。
(1)该反应的离子方程式为
(2)该反应中,氧化剂与还原剂物质的量之比为
(3)上述反应中,通入Cl2的物质的量为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)在标准状况下,测得 某气体的体积为
某气体的体积为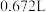 ,该气体的摩尔质量为
,该气体的摩尔质量为_______ 。
(2)将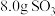 溶于水配成
溶于水配成 溶液,则所得溶液的物质的量浓度为
溶液,则所得溶液的物质的量浓度为_______ 。
(3) 溶液和
溶液和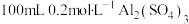 溶液混合后(混合体积变化忽略不计),溶液中
溶液混合后(混合体积变化忽略不计),溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
(4)设 为阿伏加德罗常数的数值,如果
为阿伏加德罗常数的数值,如果 氧气中含有的分子数为b,则
氧气中含有的分子数为b,则 氧气在标准状况下的体积约是
氧气在标准状况下的体积约是_______ (用含 的式子表示)
的式子表示)
(5)标准状况下,将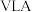 气体(摩尔质量为
气体(摩尔质量为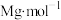 )全部溶于
)全部溶于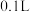 水(水的密度为
水(水的密度为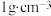 )中(假设气体与水不反应),所得溶液的密度为
)中(假设气体与水不反应),所得溶液的密度为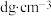 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为_______ 。
(6)某盐混合溶液中含有离子: ,测得
,测得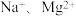 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: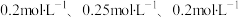 ,则
,则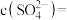
_______ 。
(1)在标准状况下,测得
 某气体的体积为
某气体的体积为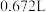 ,该气体的摩尔质量为
,该气体的摩尔质量为(2)将
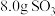 溶于水配成
溶于水配成 溶液,则所得溶液的物质的量浓度为
溶液,则所得溶液的物质的量浓度为(3)
 溶液和
溶液和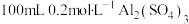 溶液混合后(混合体积变化忽略不计),溶液中
溶液混合后(混合体积变化忽略不计),溶液中 的物质的量浓度为
的物质的量浓度为(4)设
 为阿伏加德罗常数的数值,如果
为阿伏加德罗常数的数值,如果 氧气中含有的分子数为b,则
氧气中含有的分子数为b,则 氧气在标准状况下的体积约是
氧气在标准状况下的体积约是 的式子表示)
的式子表示)(5)标准状况下,将
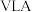 气体(摩尔质量为
气体(摩尔质量为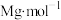 )全部溶于
)全部溶于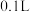 水(水的密度为
水(水的密度为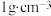 )中(假设气体与水不反应),所得溶液的密度为
)中(假设气体与水不反应),所得溶液的密度为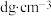 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为(6)某盐混合溶液中含有离子:
 ,测得
,测得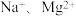 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: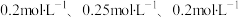 ,则
,则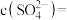
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程:H2O2→O2,
(1)该反应的氧化剂是:___ 。
(2)该反应中还原产物和氧化产物的物质的量之比为___ 。
(3)H2O2在反应过程中不仅可以转化为0价的O2,在一定条件下也可转化为-2价化合物,当H2O2和H2S在水溶液中反应时,若H2O2的氧只转化为-2价,且参加反应的H2O2和H2S物质的量只比为4:1,其中的氧只生成-2价,反应的化学方程式___ 。
(4)在MnO2作催化剂的条件下,会发生自身的歧化反应,即-1价的氧即升高也降低,则该反应过程中,若参加反应的H2O2为17g时,转移电子的数目为____ ,生成标准状况下O2的体积为_____ 。
(1)该反应的氧化剂是:
(2)该反应中还原产物和氧化产物的物质的量之比为
(3)H2O2在反应过程中不仅可以转化为0价的O2,在一定条件下也可转化为-2价化合物,当H2O2和H2S在水溶液中反应时,若H2O2的氧只转化为-2价,且参加反应的H2O2和H2S物质的量只比为4:1,其中的氧只生成-2价,反应的化学方程式
(4)在MnO2作催化剂的条件下,会发生自身的歧化反应,即-1价的氧即升高也降低,则该反应过程中,若参加反应的H2O2为17g时,转移电子的数目为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氯气和一些含氯化合物常用作消毒剂。 制备流程可表述如下:
制备流程可表述如下:
① 与
与 作用生成
作用生成 ;
;
②在75℃左右, 进一步完全转化为
进一步完全转化为 ,
,
此步方程式为 (未配平)
(未配平)
(1)写出①生成 的化学方程式
的化学方程式_______ 。漂粉精久置空气中会变质,在变质过程中不会涉及的性质是_______
A. 的酸性 B.HClO的不稳定性 C.HClO的弱酸性 D.HClO的漂白性
的酸性 B.HClO的不稳定性 C.HClO的弱酸性 D.HClO的漂白性
(2)若某学生在上述流程中发现某含钙离子盐的化学式为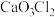 ,试根据盐的定义写出构成这种盐的酸根离子的符号
,试根据盐的定义写出构成这种盐的酸根离子的符号_______ 。
(3)若每一步反应均完全进行,且没有其他副产物,最终 与
与 的物质的量之比为
的物质的量之比为_______ 。
 制备流程可表述如下:
制备流程可表述如下:①
 与
与 作用生成
作用生成 ;
;②在75℃左右,
 进一步完全转化为
进一步完全转化为 ,
,此步方程式为
 (未配平)
(未配平)(1)写出①生成
 的化学方程式
的化学方程式A.
 的酸性 B.HClO的不稳定性 C.HClO的弱酸性 D.HClO的漂白性
的酸性 B.HClO的不稳定性 C.HClO的弱酸性 D.HClO的漂白性(2)若某学生在上述流程中发现某含钙离子盐的化学式为
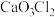 ,试根据盐的定义写出构成这种盐的酸根离子的符号
,试根据盐的定义写出构成这种盐的酸根离子的符号(3)若每一步反应均完全进行,且没有其他副产物,最终
 与
与 的物质的量之比为
的物质的量之比为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氨在人类的生产和生活中有着广泛的应用
(1)氨气溶解于水,得到的溶液称为氨水。氨溶解于水时与水发生反应生成一水合氨(NH3·H2O),它是一种弱碱。写出一水合氨的电离方程式___________ 。从上述电离方程式可知,往氨水中加入稀硫酸生成的盐是___________ (填化学式)
(2)标准状况下,将 2.24L的氨气溶于水配成 0.5L溶液,所得溶液的物质的量浓度为____ mol/L。
(3)氨可与Cl2反应,反应方程式如下:8NH3+3Cl2=6NH4Cl+N2,利用该反应的原理,在工业上可用于检验输送氯气的管道是否漏气。该反应中,___________ 是还原剂;若反应中有1.5mol氧化剂参与反应,则发生转移的电子的物质的量为___________ mol,被氧化的物质有___________ mol
(4)工业上利用水煤气产生H2以制取氨气,若在生产过程中H2O中的氢原子都全部转化为NH3,则3molH2O可制得___________ molNH3
(1)氨气溶解于水,得到的溶液称为氨水。氨溶解于水时与水发生反应生成一水合氨(NH3·H2O),它是一种弱碱。写出一水合氨的电离方程式
(2)标准状况下,将 2.24L的氨气溶于水配成 0.5L溶液,所得溶液的物质的量浓度为
(3)氨可与Cl2反应,反应方程式如下:8NH3+3Cl2=6NH4Cl+N2,利用该反应的原理,在工业上可用于检验输送氯气的管道是否漏气。该反应中,
(4)工业上利用水煤气产生H2以制取氨气,若在生产过程中H2O中的氢原子都全部转化为NH3,则3molH2O可制得
您最近半年使用:0次



