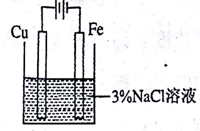
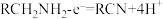利用如图装置探究铁在海水中的电化学防护,下列说法错误的是
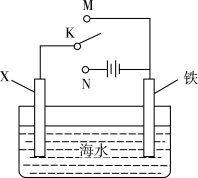

| A.若X为锌棒,开关K置于M处,可减缓铁的腐蚀 |
B.若X为锌棒,开关K置于M处,海水 降低 降低 |
| C.若X为碳棒,开关K置于N处,可减缓铁的腐蚀 |
| D.若X为碳棒,开关K置于N处,碳棒上发生氧化反应 |
更新时间:2022-12-10 20:38:40
|
相似题推荐
单选题
|
较难
(0.4)
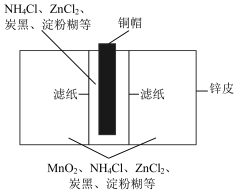
【推荐1】某同学为探究酸性干电池的工作原理,设计电池的结构如图所示。该电池工作一段时间后,实验测得 转化为
转化为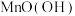 ,
, 转化为
转化为 。下列对该电池的叙述中错误的是
。下列对该电池的叙述中错误的是
 转化为
转化为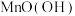 ,
, 转化为
转化为 。下列对该电池的叙述中错误的是
。下列对该电池的叙述中错误的是
| A.石墨做正极,锌皮做负极 |
B.正极反应为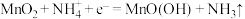 |
| C.淀粉糊有效吸水保湿,使电解质具有良好的导电性 |
D.当生成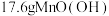 时,理论上生成 时,理论上生成 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】某小组研究 分别与
分别与 和
和 的反应:
的反应:
下列说法不正确的是
 分别与
分别与 和
和 的反应:
的反应:| 编号 | 1 | 2 | 3 |
| 实验 | 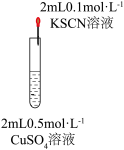 |  | 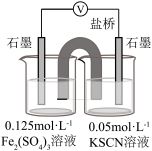 |
| 现象 | 溶液变为黄绿色,产生白色沉淀(白色沉淀为CuSCN) | 溶液变红,向反应后的溶液中滴加 溶液,产生蓝色沉淀,且沉淀量逐渐增多 溶液,产生蓝色沉淀,且沉淀量逐渐增多 | 接通电路后,电压表指针不偏转。一段时间后,取出左侧烧杯中少量溶液,滴加 溶液,没有观察到蓝色沉淀 溶液,没有观察到蓝色沉淀 |
A.实验1中产生白色沉淀说明 被还原 被还原 |
| B.实验2中的现象说明KSCN在溶液中发生了不止一个反应 |
| C.综合实验1~3,说明微粒的氧化性与浓度有关 |
D.若将实验3中 溶液替换为0.25 mol/L 溶液替换为0.25 mol/L  溶液,接通电路后,可推测出电压表指针会发生偏转 溶液,接通电路后,可推测出电压表指针会发生偏转 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】近期,科学家研发了“全氧电池”,其工作原理示意图如下。

下列说法不正确 的是

下列说法
| A.电极a是负极 |
B.电极b的反应式: |
| C.该装置可将酸和碱的化学能转化为电能 |
D.酸性条件下 的氧化性强于碱性条件下 的氧化性强于碱性条件下 的氧化性 的氧化性 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是
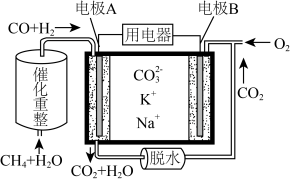

A.反应CH4+H2O 3H2+CO,每消耗1molCH4转移12mol 电子 3H2+CO,每消耗1molCH4转移12mol 电子 |
B.电池工作时,CO 向电极B移动 向电极B移动 |
C.电极B上发生的电极反应为O2+2CO2+4e-=2CO |
| D.电极A上H2参与的电极反应为:H2+2OH-_2e-=2H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】化学镀铜废液中含有一定量的CuSO4,任意排放会污染环境,利用电化学原理可对废液进行回收处理,装置如图,其中质子交换膜只允许H+通过。已知:①Cu2++ HCHO + 3OH-=Cu + HCOO-+ 2H2O;②还原性:HCHO > M(—种金属)> Cu。
下列说法正确的是

下列说法正确的是

| A.反应之前,应将含OH-的HCHO溶液加入到装置的左侧 |
| B.右侧发生的电极反应式:HCHO-2e-+H2O=HCOO-+3H+ |
| C.若将质子交换膜换成阴离子交换膜,放电过程中,大量的OH-将向左侧迁移 |
| D.放电一段时间后打开开关,移去质子交换膜,装置中可能会有红色固体、蓝色絮状物出现 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】用石墨电极完成下列电解实验。下列对实验现象的解释或推测不合理的是
| 实验一 | 实验二 | |
| 装置 | 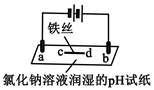 | 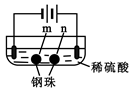 |
| 现象 | a、d处试纸变蓝;b处变红,局部褪色;c处无明显变化 | 两个石墨电极附近有气泡产生;n处有气泡产生;…… |
| A.a、d处:2H2O+2e-=H2↑+2OH- |
| B.b处:2Cl--2e-=Cl2↑,Cl2溶于水生成HClO,使溶液褪色 |
| C.c处发生了反应:Fe-2e-=Fe2+ |
| D.根据实验一的原理,实验二中n处能析出O2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】工业上电解法处理含镍酸性废水并得到单质镍的原理如图所示,已知:①Ni2+在弱酸性溶液中发生水解②氧化性:Ni2+(高浓度)>H+ >Ni2+(低浓度)。下列说法正确的是
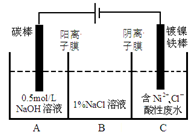

| A.碳棒上发生的电极反应:2C1--2e-=Cl2 ↑ |
| B.电解过程中,B中NaCl 溶液的浓度将不断减小 |
| C.为了提高Ni的产率,电解过程中需要控制废水的pH |
| D.若将图中阳离子交换膜去掉,则电解反应总方程式不发生改变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列说法正确的是
| A.用盐酸标准溶液测定NaOH溶液浓度滴定实验中,滴定前无气泡而滴定后有气泡,会使测定值偏高 |
| B.将地下钢管与直流电源的正极相连,用来保护钢管 |
| C.已知在101KPa下,1gH2燃烧生成水蒸气放出121kJ热量,其热化学方程式为:2H2(g)+O2(g)=2H2O(g) △H=-484 kJ·mol-1 |
| D.25℃,101kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3kJ·mol-1,表示稀H2SO4与KOH 溶液反应的中和热的热化学方程式为:H2SO4(aq)+2KOH(aq)=K2SO4(aq)+2H2O(l)△H=-114.6kJ·mol-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】在实验室中进行下列实验,下列操作能实现实验目的的是
| 选项 | 实验目的 | 操作 |
| A | 检验甲酸中是否含有羧基 | 取其水溶液于试管中,向其中加入少量金属钠,观察溶液中有无气泡产生 |
| B | 检验某溶液中是否含有 | 取少量待测液于试管中,向其中滴加浓氨水,生成白色沉淀,继续滴加浓氨水,观察沉淀是否溶解 |
| C | 检验牺牲阳极法对钢铁防腐的效果 | 将镀层有破损的镀锌铁片放入酸化的3%NaCl溶液中,一段时间后,取少量溶液向其中加入 溶液,观察有无蓝色沉淀生成 溶液,观察有无蓝色沉淀生成 |
| D | 探究氢离子浓度对 、 、 互相转化影响 互相转化影响 | 向 溶液中缓慢滴加浓盐酸,观察溶液颜色的变化 溶液中缓慢滴加浓盐酸,观察溶液颜色的变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

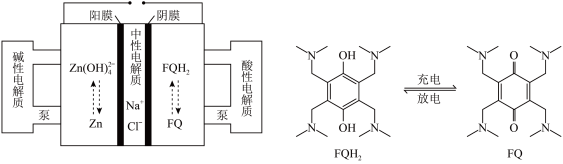

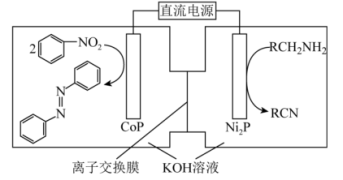
 )的装置如图所示(R代表烃基)。下列说法正确的是
)的装置如图所示(R代表烃基)。下列说法正确的是