下图是实验室用乙醇、硫酸、溴化钠混合反应来制备溴乙烷的装置(省去了加热装置),回答下列问题:
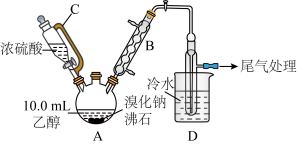
已知:浓硫酸与溴化钠共热时发生反应:
(1)仪器A、C的名称分别为_______ 、_______ ;B的作用为_______ 。
(2)装置A中生成溴乙烷的化学方程式为_______ 。
(3)若选用的硫酸浓度过大,D中得到的产品则会因混入少量溴而呈棕黄色,生成这一副产物的原因为_______ (用化学方程式表示);为纯化产物,最好选择下列的_______ 溶液来洗涤产品。
A.四氯化碳 B.硫酸钠 C.碘化钠 D.亚硫酸钠
(4)若实验中使用了10g乙醇、20.6g溴化钠,且浓硫酸足量,经过分离、提纯、干燥后,最终得到10.9g溴乙烷,则本实验中溴乙烷的产率为_______ (保留3位有效数字)。
(5)检验溴乙烷中溴元素的方法为:取样,_______ ,若产生淡黄色沉淀,则该物质中存在溴元素。

已知:浓硫酸与溴化钠共热时发生反应:

(1)仪器A、C的名称分别为
(2)装置A中生成溴乙烷的化学方程式为
(3)若选用的硫酸浓度过大,D中得到的产品则会因混入少量溴而呈棕黄色,生成这一副产物的原因为
A.四氯化碳 B.硫酸钠 C.碘化钠 D.亚硫酸钠
(4)若实验中使用了10g乙醇、20.6g溴化钠,且浓硫酸足量,经过分离、提纯、干燥后,最终得到10.9g溴乙烷,则本实验中溴乙烷的产率为
(5)检验溴乙烷中溴元素的方法为:取样,
更新时间:2022-10-25 07:54:31
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室用乙醇和浓硫酸反应制备乙烯,乙烯再与溴反应制备1,2—二溴乙烷。装置如图所示(加热及夹持装置省略):
已知:①乙醇在浓硫酸、140℃的条件下脱水生成乙醚。
②制备乙烯时部分乙醇可能与浓硫酸反应产生CO2、SO2。
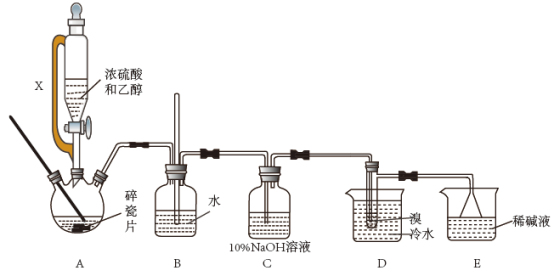
有关数据列表如下:
回答下列问题:
(1)该装置中盛放浓硫酸和乙醇的仪器名称___ ;装置B的作用__ 。
(2)装置C中10%NaOH溶液的作用___ 。
(3)在A中发生的化学反应方程式为___ 。
(4)在制备乙烯时,要尽快地把反应温度提高到170℃左右,其最主要的目的是___ 。
a.引发反应 b.加快反应速率 c.防止乙醇挥发 d.减少副产物乙醚生成
(5)将1,2—二溴乙烷粗产品置于分液漏斗中,加水,振荡后静置,产物应在__ (填“上”或“下”)层。
(6)下列操作除掉1,2—二溴乙烷中的溴单质可行的是__ 。
a.加入碳酸钠溶液振荡、静置后分液
b.加入氢氧化钠溶液振荡、静置后分液
c.蒸馏
已知:①乙醇在浓硫酸、140℃的条件下脱水生成乙醚。
②制备乙烯时部分乙醇可能与浓硫酸反应产生CO2、SO2。

有关数据列表如下:
| 物质 | 乙醇 | 1,2—二溴乙烷 | 溴 |
| 密度g·cm-3 | 0.79 | 2.2 | 3.12 |
| 沸点/℃ | 78.5 | 132 | 59 |
(1)该装置中盛放浓硫酸和乙醇的仪器名称
(2)装置C中10%NaOH溶液的作用
(3)在A中发生的化学反应方程式为
(4)在制备乙烯时,要尽快地把反应温度提高到170℃左右,其最主要的目的是
a.引发反应 b.加快反应速率 c.防止乙醇挥发 d.减少副产物乙醚生成
(5)将1,2—二溴乙烷粗产品置于分液漏斗中,加水,振荡后静置,产物应在
(6)下列操作除掉1,2—二溴乙烷中的溴单质可行的是
a.加入碳酸钠溶液振荡、静置后分液
b.加入氢氧化钠溶液振荡、静置后分液
c.蒸馏
您最近一年使用:0次
【推荐2】氯苯是有机生产中重要的生产原料,利用氯苯可合成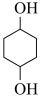 ,其工艺流程如下(部分试剂和反应条件已略去):
,其工艺流程如下(部分试剂和反应条件已略去):
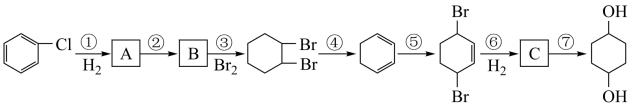
回答下列问题:
(1)B分子中含有的官能团名称为___________ 。
(2)反应①~⑦中属于消去反应的是___________ (填序号)。
(3)反应①的化学方程式:___________ 。
(4)反应④的化学方程式:___________ 。
(5)反应⑦的化学方程式:___________ 。
 ,其工艺流程如下(部分试剂和反应条件已略去):
,其工艺流程如下(部分试剂和反应条件已略去):
回答下列问题:
(1)B分子中含有的官能团名称为
(2)反应①~⑦中属于消去反应的是
(3)反应①的化学方程式:
(4)反应④的化学方程式:
(5)反应⑦的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】溴乙烷是卤代烃的代表,通过对溴乙烷的探究来掌握卤代烃的性质,可以达到举一反三、触类旁通的效果。
I.已知:NaBr+H2SO4(浓) NaHSO4+ HBr
NaHSO4+ HBr
CH3CH2OH+HBr CH3CH2Br+H2O
CH3CH2Br+H2O
溴乙烷的沸点38.4℃,实验室制备溴乙烷(CH3CH2Br)的装置和步骤如下:
①检查装置的气密性,向装置图所示的U形管和大烧杯中加入冰水;
②在圆底烧瓶中加入10mL95%乙醇、28mL78%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;
③小心加热,使其充分反应。

回答下列问题:
(1)为了更好的控制反应温度,除用图示的小火加热,更好的加热方式是_______________ 。
(2)浓硫酸具有强氧化性,能氧化还原性气体HBr为Br2,导致U形管中粗制的溴乙烷呈棕黄色。为了除去粗产品中的杂质Br2,可选择下列试剂中的:______ (填序号)
A.NaOH溶液B.H2O
C.Na2SO3溶液D.CCl4
分离时所需的主要玻璃仪器是______________ (填仪器名称)。要进一步制得纯净的溴乙烷,可用水洗,然后加入无水CaCl2,再进行_________ (填操作名称)。
II.溴乙烷在不同溶剂中与NaOH可发生不同类型的反应,生成不同的反应产物。某同学依据溴乙烷的性质,用图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究。

(1)在试管中加入5 mL 1 mol/L NaOH水溶液和5 mL溴乙烷,将试管如图固定后,加热。试管口安装一长导管的作用是_________ 。
(2)在试管中加入5 mL NaOH乙醇溶液和5 mL溴乙烷,将试管如图固定后,加热。
①请写出该反应的化学方程式_____________________________________________ 。
②为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在设计的实验方案中,需要检验的是___________ ,检验的装置如图所示,在气体通入酸性高锰酸钾溶液前加一个盛水的试管,其作用是_____________ 。

I.已知:NaBr+H2SO4(浓)
 NaHSO4+ HBr
NaHSO4+ HBrCH3CH2OH+HBr
 CH3CH2Br+H2O
CH3CH2Br+H2O溴乙烷的沸点38.4℃,实验室制备溴乙烷(CH3CH2Br)的装置和步骤如下:
①检查装置的气密性,向装置图所示的U形管和大烧杯中加入冰水;
②在圆底烧瓶中加入10mL95%乙醇、28mL78%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;
③小心加热,使其充分反应。

回答下列问题:
(1)为了更好的控制反应温度,除用图示的小火加热,更好的加热方式是
(2)浓硫酸具有强氧化性,能氧化还原性气体HBr为Br2,导致U形管中粗制的溴乙烷呈棕黄色。为了除去粗产品中的杂质Br2,可选择下列试剂中的:
A.NaOH溶液B.H2O
C.Na2SO3溶液D.CCl4
分离时所需的主要玻璃仪器是
II.溴乙烷在不同溶剂中与NaOH可发生不同类型的反应,生成不同的反应产物。某同学依据溴乙烷的性质,用图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究。

(1)在试管中加入5 mL 1 mol/L NaOH水溶液和5 mL溴乙烷,将试管如图固定后,加热。试管口安装一长导管的作用是
(2)在试管中加入5 mL NaOH乙醇溶液和5 mL溴乙烷,将试管如图固定后,加热。
①请写出该反应的化学方程式
②为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在设计的实验方案中,需要检验的是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
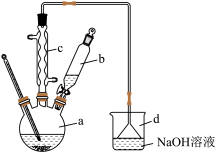
【推荐1】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
按以下合成步骤回答问题:
(1)在a中加入15 mL苯和少量铁屑。在b中小心加入4.0 mL 液溴。再将b中液溴慢慢加入到a中,充分反应。装置a中发生的主要反应是___ ;装置d的作用是___ 。
(2)反应过程中,a外壁温度升高,为提高原料利用率,采取以下措施:
①采用装置c的目的是___ 。
②利用温度计控制温度,适宜的温度范围为(填序号)___ 。
A.>156℃ B. 59℃-80℃ C.<59℃
(3)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用10 mL水、8 mL10%的NaOH溶液、10 mL水洗涤。操作②所需要的玻璃仪器除烧杯外,还需___ ,滤液用NaOH溶液洗涤的作用是___ 。
③向分离出的粗溴苯中加入少量的无水氯化钙,静置、过滤。
(4)经过上述分离操作后,粗溴苯中溶解的主要杂质为苯,要进一步提纯,下列操作中必须的是___ (填入正确选项前的字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
| 苯 | 溴 | 溴苯 | |
| 密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
按以下合成步骤回答问题:
(1)在a中加入15 mL苯和少量铁屑。在b中小心加入4.0 mL 液溴。再将b中液溴慢慢加入到a中,充分反应。装置a中发生的主要反应是
(2)反应过程中,a外壁温度升高,为提高原料利用率,采取以下措施:
①采用装置c的目的是
②利用温度计控制温度,适宜的温度范围为(填序号)
A.>156℃ B. 59℃-80℃ C.<59℃
(3)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用10 mL水、8 mL10%的NaOH溶液、10 mL水洗涤。操作②所需要的玻璃仪器除烧杯外,还需
③向分离出的粗溴苯中加入少量的无水氯化钙,静置、过滤。
(4)经过上述分离操作后,粗溴苯中溶解的主要杂质为苯,要进一步提纯,下列操作中必须的是
A.重结晶 B.过滤 C.蒸馏 D.萃取
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
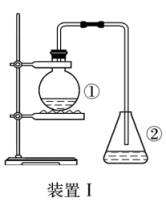
【推荐2】为探究苯与溴的取代反应,甲用如图装置Ⅰ进行如下实验:
(1)装置Ⅰ中①的化学方程式为(写两个)_______ 。②中离子方程式为_______ 。
(2)①中长导管的作用是_______ 。
(3)烧瓶中生成的红褐色油状液滴的成分是(答两种)_______ ,要想得到纯净的产物,可用_______ 试剂洗涤。洗涤后分离粗产品应使用的仪器是_______ 。
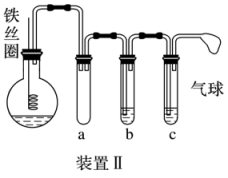
(4)乙同学设计如图所示装置Ⅱ,并用下列某些试剂完成该实验,可选用的试剂是苯、液溴、浓硫酸、氢氧化钠溶液、硝酸银溶液、四氯化碳。_______ ;b中的试剂是_______ 。比较两套装置,装置Ⅱ的主要优点是(答两条)_______ 。
(1)装置Ⅰ中①的化学方程式为(写两个)
(2)①中长导管的作用是
(3)烧瓶中生成的红褐色油状液滴的成分是(答两种)
(4)乙同学设计如图所示装置Ⅱ,并用下列某些试剂完成该实验,可选用的试剂是苯、液溴、浓硫酸、氢氧化钠溶液、硝酸银溶液、四氯化碳。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
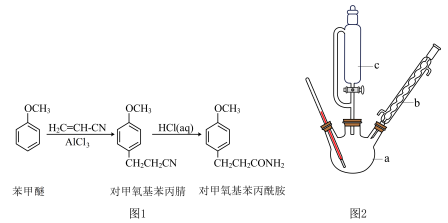
【推荐3】对甲氧基苯丙酰胺(相对分子质量为179)为难溶于冷水的白色晶体,且是一种医药中间体,可以由苯甲醚通过两步反应合成,合成路线如图1所示。
②丙烯腈蒸汽与空气可形成爆炸性混合物。
步骤一:用图2所示装置合成对甲氧基苯丙腈
在a中加入108g苯甲醚,室温下缓慢加入70g粉末状三氯化铝,加入过程中温度不超过25℃,加完后降温至5℃,然后逐滴加入130g丙烯腈(沸点77℃),滴加结束后再升温至90~95℃,反应2h。将反应液倒入500g冰水中,搅匀,静置分层,分出油相。减压蒸馏,收集2.67kPa下150~160℃的馏分,得到对甲氧基苯丙腈。
步骤二:合成对甲氧基苯丙酰胺
将步骤一中合成的对甲氧基苯丙腈加到a中,再加入300mL浓盐酸,经过一系列操作后得到对甲氧基苯丙酰胺134.25g。
(1)a的名称是______ ,对甲氧基苯丙腈的合成过程中宜采用的加热方式为______ 。
(2)图2中合成对甲氧基苯丙腈的装置有一缺陷,请提出改进方法并说明理由:______ 。
(3)用c加丙烯腈的优点有______ 。(写出两条)
(4)合成对甲氧基苯丙酰胺的过程中加浓盐酸后的一系列操作为:升温至40~50℃。搅拌1h→加入活性炭回流0.5h→______ →将滤液慢慢倒入1000g冷水中,析出晶体→抽滤→洗涤、烘干。
(5)下列关于实验操作的说法正确的是______ 。
(6)本实验中对甲氧基苯丙酰胺的产率为_______ 。
②丙烯腈蒸汽与空气可形成爆炸性混合物。
步骤一:用图2所示装置合成对甲氧基苯丙腈
在a中加入108g苯甲醚,室温下缓慢加入70g粉末状三氯化铝,加入过程中温度不超过25℃,加完后降温至5℃,然后逐滴加入130g丙烯腈(沸点77℃),滴加结束后再升温至90~95℃,反应2h。将反应液倒入500g冰水中,搅匀,静置分层,分出油相。减压蒸馏,收集2.67kPa下150~160℃的馏分,得到对甲氧基苯丙腈。
步骤二:合成对甲氧基苯丙酰胺
将步骤一中合成的对甲氧基苯丙腈加到a中,再加入300mL浓盐酸,经过一系列操作后得到对甲氧基苯丙酰胺134.25g。
(1)a的名称是
(2)图2中合成对甲氧基苯丙腈的装置有一缺陷,请提出改进方法并说明理由:
(3)用c加丙烯腈的优点有
(4)合成对甲氧基苯丙酰胺的过程中加浓盐酸后的一系列操作为:升温至40~50℃。搅拌1h→加入活性炭回流0.5h→
(5)下列关于实验操作的说法正确的是
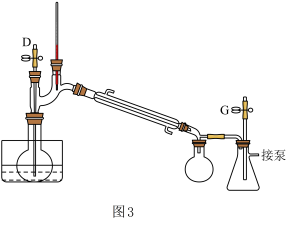
| A.减压蒸馏采用如图3所示装置,装置中的D为毛细管,也可以用沸石代替 |
| B.减压蒸馏过程中,可以通过控制G处的旋塞停止减压 |
| C.在对甲氧基苯丙酰胺的合成过程中,析出的晶体可以用冷水洗涤 |
| D.减压过滤不宜用于过滤颗粒太小的沉淀,因为颗粒太小的沉淀在快速过滤时易透过滤纸 |
(6)本实验中对甲氧基苯丙酰胺的产率为
您最近一年使用:0次



