对于反应: ,若有0.1molKClO3参加反应,下列说法正确的是
,若有0.1molKClO3参加反应,下列说法正确的是
 ,若有0.1molKClO3参加反应,下列说法正确的是
,若有0.1molKClO3参加反应,下列说法正确的是| A.被氧化的HCl为0.6mol |
| B.转移电子1.806×1023个 |
| C.还原性:KClO3大于Cl2 |
D.还原剂占参加反应HCl的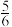 |
更新时间:2022-11-01 18:22:17
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】氮的化合物在催化剂作用下可转化为N2和水,催化机理如图所示。下列说法正确的是


| A.Fe2+为该反应的催化剂 |
| B.该反应可在碱性条件下发生 |
C.该过程总反应方程式为4NH3+4NO+O2 4N2+6H2O 4N2+6H2O |
| D.若有22.4LNO参与反应,则转移的电子数为4NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】2018年11月16日,国际计量大会通过最新决议,将1摩尔定义为“精确包含6.02214076×1023个原子或分子等基本单元,这一常数称作阿伏加 德罗常数(NA),单位为mol−1。”下列叙述正确的是
| A.标准状况下,22.4L SO3含有NA个分子 |
| B.4.6g乙醇中含有的C−H键为0.6NA |
| C.0.1mol Na2O2与水完全反应转移的电子数为0.1NA |
| D.0.1 mol·L─1的醋酸溶液中含有的H+数目小于0.1NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
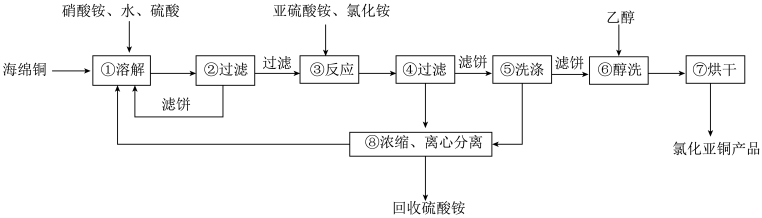
【推荐1】氯化亚铜(CuCl)难溶于水和稀酸,可溶于 浓度较大的体系,在潮湿空气中易水解氧化。在工业上可利用海绵铜(主要成分是Cu和少量CuO)制备,流程如下。下列说法错误的是
浓度较大的体系,在潮湿空气中易水解氧化。在工业上可利用海绵铜(主要成分是Cu和少量CuO)制备,流程如下。下列说法错误的是
 浓度较大的体系,在潮湿空气中易水解氧化。在工业上可利用海绵铜(主要成分是Cu和少量CuO)制备,流程如下。下列说法错误的是
浓度较大的体系,在潮湿空气中易水解氧化。在工业上可利用海绵铜(主要成分是Cu和少量CuO)制备,流程如下。下列说法错误的是
| A.①步溶解过程中,硝酸铵是氧化剂,铜是还原剂 |
B.③步反应的离子方程式是: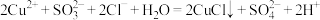 |
| C.⑤步包含了酸洗和水洗,酸洗时可采用稀硫酸或浓盐酸 |
| D.⑦步“烘干”过程中需要保持真空条件 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】高铁酸钠(Na2FeO4)具有优异的氧化漂白、杀菌作用。工业上可以用下列四种方法制备高铁酸钠:
①Fe2O3+Na2O2→Na2FeO4+Na2O
②FeSO4+Na2O2→Na2FeO4+Na2O+Na2SO4+O2↑
③Fe(NO3)3+NaOH+Cl2→Na2FeO4+NaNO3+NaCl+H2O
④Fe(OH)3+NaClO+NaOH→Na2FeO4+NaCl+H2O
下列说法正确的是
①Fe2O3+Na2O2→Na2FeO4+Na2O
②FeSO4+Na2O2→Na2FeO4+Na2O+Na2SO4+O2↑
③Fe(NO3)3+NaOH+Cl2→Na2FeO4+NaNO3+NaCl+H2O
④Fe(OH)3+NaClO+NaOH→Na2FeO4+NaCl+H2O
下列说法正确的是
| A.反应①和②中Na2O2均只作氧化剂 |
| B.Na2FeO4的氧化性强于NaClO、Na2O2 |
| C.反应③中氧化产物和还原产物的物质的量比为2:3 |
| D.反应④中转移3mol电子时,消耗2mol NaOH |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】在Fe+催化作用下CO可将N2O转化为N2,反应的能量变化及反应历程如图所示:
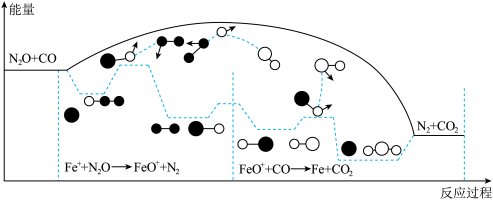
①N2O+Fe+=N2+FeO+(慢)②FeO++CO=CO2+Fe+(快)
下列叙述不 正确的是

①N2O+Fe+=N2+FeO+(慢)②FeO++CO=CO2+Fe+(快)
下列叙述
| A.反应①为放热反应 |
| B.FeO+为反应①的氧化产物,也是总反应的中间产物 |
| C.反应②的活化能Ea2比反应①的活化能Ea2要大 |
| D.每生成1molN2,转移电子数目为2×6.02×1023 |
您最近一年使用:0次
【推荐2】氯化硫(S2C12)的结构式为Cl- S- S- Cl, 常温下为浅黄色油状液体,遇与水即分解:2S2Cl2+2H2O→4HCl+SO2↑+3S↓。下列有关此反应的说法正确的是
| A.S2C12做氧化剂,H2O做还原剂。 |
| B.每生成1molSO2转移4mol电子 |
| C.氧化产物与还原产物的物质的量之比为3:1 |
| D.每生成48g硫会断裂2mol氢氧键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】氢化钙 与水反应可生成氢气,常作为登山运动员能源提供剂,利用干燥纯净的氢气与钙在加热条件下制备氢化钙的装置如下图所示:
与水反应可生成氢气,常作为登山运动员能源提供剂,利用干燥纯净的氢气与钙在加热条件下制备氢化钙的装置如下图所示:
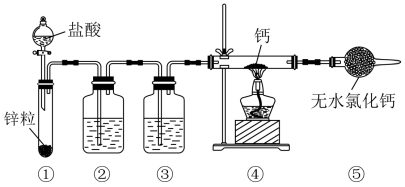
则下列说法中正确的是
 与水反应可生成氢气,常作为登山运动员能源提供剂,利用干燥纯净的氢气与钙在加热条件下制备氢化钙的装置如下图所示:
与水反应可生成氢气,常作为登山运动员能源提供剂,利用干燥纯净的氢气与钙在加热条件下制备氢化钙的装置如下图所示:
则下列说法中正确的是
| A.氢化钙与水反应时,氢化钙中的氢元素被还原 |
| B.装置②、③中盛放的试剂依次是浓硫酸、NaOH溶液 |
| C.点燃装置④中的酒精灯与打开分液漏斗旋塞可同时进行 |
| D.装置⑤中的无水氯化钙也可以用碱石灰来代替 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知:还原性 > I-,氧化性
> I-,氧化性 > I2.在含3 mol NaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和析出的I2的物质的量的关系曲线如图(不考虑I2+I-
> I2.在含3 mol NaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和析出的I2的物质的量的关系曲线如图(不考虑I2+I-
 )下列说法不正确的是
)下列说法不正确的是

 > I-,氧化性
> I-,氧化性 > I2.在含3 mol NaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和析出的I2的物质的量的关系曲线如图(不考虑I2+I-
> I2.在含3 mol NaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和析出的I2的物质的量的关系曲线如图(不考虑I2+I-
 )下列说法不正确的是
)下列说法不正确的是
A.a点时消耗NaHSO3的物质的量为1.2 mol,得到的氧化产物为 |
B.b~c段的反应可用如下离子方程式表示: + 5I- +3 H2O = 3I2 + 6OH- + 5I- +3 H2O = 3I2 + 6OH- |
| C.滴加过程中溶液的pH值先降低后升高 |
| D.从c点后所得混合液中分离出碘的操作为:加四氯化碳萃取分液,然后蒸馏 |
您最近一年使用:0次

 的数目为0. 02 NA
的数目为0. 02 NA 的数目为NA
的数目为NA 可以支持镁燃烧发生以下反应:
可以支持镁燃烧发生以下反应: ,下列关于该反应的判断正确的是
,下列关于该反应的判断正确的是 是氧化产物
是氧化产物
 原子失去的电子数目等于
原子失去的电子数目等于 原子得到的电子数目
原子得到的电子数目

