在Fe+催化作用下CO可将N2O转化为N2,反应的能量变化及反应历程如图所示:
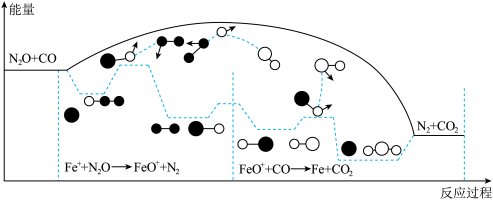
①N2O+Fe+=N2+FeO+(慢)②FeO++CO=CO2+Fe+(快)
下列叙述不 正确的是

①N2O+Fe+=N2+FeO+(慢)②FeO++CO=CO2+Fe+(快)
下列叙述
| A.反应①为放热反应 |
| B.FeO+为反应①的氧化产物,也是总反应的中间产物 |
| C.反应②的活化能Ea2比反应①的活化能Ea2要大 |
| D.每生成1molN2,转移电子数目为2×6.02×1023 |
更新时间:2023-09-21 15:47:30
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】我国科技工作者运用DFT计算研究HCOOH在不同催化剂(Pd和Rh)表面分解产生H2的部分反应历程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法错误的是( )
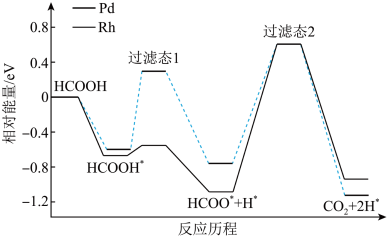

| A.HCOOH吸附在催化剂表面是一个放热过程 |
| B.Pd、Rh作催化剂时HCOOH分解产生H2的反应热不同 |
| C.该反应过程中有C-H键的断裂,还有C=O键的生成 |
| D.HCOO*+H*=CO2+2H*是该历程的决速步骤 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】合成氨反应过程中的能量变化如图所示,下列说法正确的是


| A.反应体系中加入催化剂,会改变反应的热效应 |
| B.反应物的总能量低于生产物的总量 |
C.该反应的热化学方程式为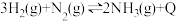 (Q>0) (Q>0) |
| D.该反应是吸热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】以太阳能为热源分解 ,经热化学铁氧化合物循环分解水制
,经热化学铁氧化合物循环分解水制 的过程如图所示,已知:
的过程如图所示,已知:
过程Ⅰ: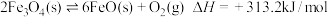
过程Ⅱ: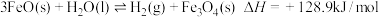
下列说法不正确 的是
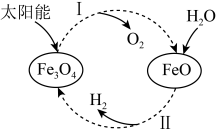
 ,经热化学铁氧化合物循环分解水制
,经热化学铁氧化合物循环分解水制 的过程如图所示,已知:
的过程如图所示,已知:过程Ⅰ:
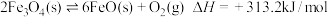
过程Ⅱ:
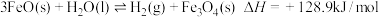
下列说法

| A.过程Ⅰ中实现了太阳能向化学能的转化 |
B.由信息可知 |
| C.增加铁氧化合物的质量可以加快反应速率 |
| D.过程Ⅰ中正反应的活化能高于逆反应的活化能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】CH3CH2CH3的氯化、溴化反应势能图及产物选择性如图,下列叙述错误的是


| A.丙烷中仲氢(—CH2—)比伯氢(—CH3)活性强 |
B.升高温度CH3CH2CH3与Cl 反应速率比与Br 反应速率比与Br 反应速率慢 反应速率慢 |
| C.以CH3CH2CH3为原料合成2-丙醇时,溴化反应比氯化反应产率更高 |
| D.HCl和HBr的键能差=ΔH1-ΔH3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某实验小组学习化学反应速率后,联想到 分解制备氧气,设计如下实验方案探究外界条件对反应速率的影响。下列说法错误的是
分解制备氧气,设计如下实验方案探究外界条件对反应速率的影响。下列说法错误的是
 分解制备氧气,设计如下实验方案探究外界条件对反应速率的影响。下列说法错误的是
分解制备氧气,设计如下实验方案探究外界条件对反应速率的影响。下列说法错误的是| 编号 | 温度 | 反应物 | 催化剂 |
| 甲 | 25℃ | 试管中加入 溶液 溶液 |  蒸馏水 蒸馏水 |
| 乙 | 25℃ | 试管中加入 溶液 溶液 |  溶液 溶液 |
| 丙 | 40℃ | 试管中加入 溶液 溶液 |  蒸馏水 蒸馏水 |
A.实验甲中发生的反应 |
| B.实验甲和乙的实验目的是探究催化剂对反应速率的影响 |
| C.实验甲和丙的实验目的是温度越高,反应速率越快 |
D.实验乙中 的反应速率大于 的反应速率大于 的反应速率,不考虑实验测量误差,二者速率存在差异的主要原因是随着反应的进行 的反应速率,不考虑实验测量误差,二者速率存在差异的主要原因是随着反应的进行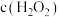 减少 减少 |
您最近一年使用:0次
【推荐2】根据以下实验操作及现象,能推出相应结论的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向丙烯醛(CH2=CHCHO)中加入橙色的溴水,振荡 | 溴水褪色 | 丙烯醛与Br2发生加成反应 |
| B | 向Na2S溶液中滴加浓盐酸 | 产生臭鸡蛋气味的气体 | 非金属性:Cl>S |
| C | 向苯酚浊液中滴加少量Na2CO3溶液 | 浊液变澄清 | 酸性:苯酚> |
| D | 向盛有等体积、等浓度的H2O2溶液的两支试管中分别加入0.2mL等浓度的CuSO4溶液和KMnO4溶液 | 加KMnO4溶液的试管中产生气泡的速率更快 |  比Cu2+的催化效果好 比Cu2+的催化效果好 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】 常用作食盐中的补碘剂,可用“氯酸钾四化法”制备,该方法的第一步反应为
常用作食盐中的补碘剂,可用“氯酸钾四化法”制备,该方法的第一步反应为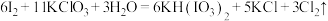 。下列说法正确的是
。下列说法正确的是
 常用作食盐中的补碘剂,可用“氯酸钾四化法”制备,该方法的第一步反应为
常用作食盐中的补碘剂,可用“氯酸钾四化法”制备,该方法的第一步反应为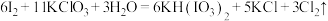 。下列说法正确的是
。下列说法正确的是A.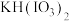 为还原产物 为还原产物 |
B.产生11.2L(标准状况) 时,转移10mol 时,转移10mol |
C.可用澄清石灰水吸收反应产生的 尾气,防止污染空气 尾气,防止污染空气 |
| D.反应中氧化剂和还原剂的物质的量之比为6∶11 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】用还原法可以将硝酸厂烟气中的大量氮氧化物(NOx)转化为无害物质。常温下,将NO与H2的混合气体通入Ce(SO4)2与Ce2(SO4)3的混合溶液中,其物质的转化过程如图所示。下列说法不正确的是
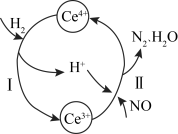

| A.反应I的离子方程式为2Ce4+ + H2 = 2Ce3+ + 2H+ |
| B.反应II中氧化剂与还原剂的物质的量之比为1:2 |
| C.反应过程中,混合溶液中Ce3+和Ce4+的总数一定保持不变 |
| D.理论上,每消耗2.24 L氢气,转移的电子的物质的量为0.2 mol |
您最近一年使用:0次

 ,发生的反应为:
,发生的反应为:
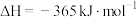 。上述反应分两步进行:
。上述反应分两步进行: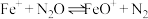
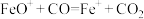
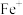 与
与
 ,
,

 )是一种新型绿色消毒剂,主要用于饮用水处理,制备的一种方法其原理:
)是一种新型绿色消毒剂,主要用于饮用水处理,制备的一种方法其原理: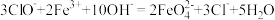 ,下列说法
,下列说法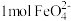 ,转移
,转移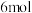 电子
电子


