填空。
(1)用软锰矿(主要成分为MnO2,含少量Fe3O4、Al2O3)和BaS制备高纯MnCO3的工艺流程如下:
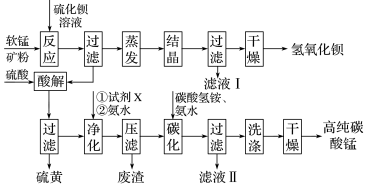
软锰矿预先粉碎的目的是_______ ,MnO2与BaS溶液反应转化为MnO的化学方程式为_______ 。
(2)高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂作剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为Fe2+离子。配平制取铁酸钠的化学方程式:_______ 。
______Fe(NO3)3+______NaOH+______Cl2═______Na2FeO4+______NaCl+6NaNO3+8H2O
反应中,_______ 元素被氧化,每生成8mol H2O转移电子总数为_______ 。
(1)用软锰矿(主要成分为MnO2,含少量Fe3O4、Al2O3)和BaS制备高纯MnCO3的工艺流程如下:

软锰矿预先粉碎的目的是
(2)高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂作剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为Fe2+离子。配平制取铁酸钠的化学方程式:
______Fe(NO3)3+______NaOH+______Cl2═______Na2FeO4+______NaCl+6NaNO3+8H2O
反应中,
更新时间:2022-12-07 19:27:27
|
相似题推荐
【推荐1】氧氯化铜[Cu2(OH)3Cl]可用作农药,氧化亚铜(Cu2O)可作杀虫剂。
(1)利用工业铜渣(主要成分为Cu、CuS、FeS等)制得氧氯化铜的流程如下:___________ 。
②“转化”过程的化学方程式为___________ 。
③“氧化”产生的SO2可以用石灰石浆(石灰石加水)吸收,同时鼓入空气可以制得石膏(CaSO4)。该反应的化学方程式为___________ 。
(2)用铜作阳极,电解一定浓度的NaCl和NaOH溶液可得到氧化亚铜,相关转化如下图所示。___________ 。
②转化Ⅱ的离子方程式为___________ 。
(1)利用工业铜渣(主要成分为Cu、CuS、FeS等)制得氧氯化铜的流程如下:

②“转化”过程的化学方程式为
③“氧化”产生的SO2可以用石灰石浆(石灰石加水)吸收,同时鼓入空气可以制得石膏(CaSO4)。该反应的化学方程式为
(2)用铜作阳极,电解一定浓度的NaCl和NaOH溶液可得到氧化亚铜,相关转化如下图所示。

②转化Ⅱ的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】钪是一种稀土金属元素,在国防、航天、核能等领域具有重要应用。氯化钪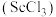 是制备钪的重要原料。工业上利用固体废料“赤泥”(含
是制备钪的重要原料。工业上利用固体废料“赤泥”(含 、
、 、
、 、
、 、
、 等)制取
等)制取 的流程如图。
的流程如图。 难溶于盐酸;②草酸可与多种金属离子形成可溶性络合物。
难溶于盐酸;②草酸可与多种金属离子形成可溶性络合物。
回答下列问题:
(1)酸浸中,滤渣的主要成分是_______ (填化学式), 溶解的离子反应方程式为
溶解的离子反应方程式为_______ 。
(2)“步骤Ⅰ”中加入 后选择合适试剂调pH,再将溶液加热煮沸一段时间,加热煮沸的目的是
后选择合适试剂调pH,再将溶液加热煮沸一段时间,加热煮沸的目的是_______ 。
(3)草酸用量过多时,钪的沉淀率反而下降,原因是_______ 。
(4)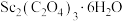 在空气中加热分解时,
在空气中加热分解时, %随温度变化如图所示。
%随温度变化如图所示。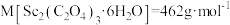 。
。
250℃时固体的主要成分是:_______ (填化学式)。
(5)传统制备 的方法是先得到
的方法是先得到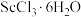 沉淀,再高温脱水得
沉淀,再高温脱水得 ,但通常含有
,但通常含有 杂质,原因是
杂质,原因是_______ 。
(6)“加热氯化”过程主要发生反应的化学方程式为:_______ 。
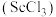 是制备钪的重要原料。工业上利用固体废料“赤泥”(含
是制备钪的重要原料。工业上利用固体废料“赤泥”(含 、
、 、
、 、
、 、
、 等)制取
等)制取 的流程如图。
的流程如图。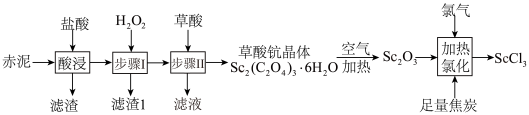
 难溶于盐酸;②草酸可与多种金属离子形成可溶性络合物。
难溶于盐酸;②草酸可与多种金属离子形成可溶性络合物。回答下列问题:
(1)酸浸中,滤渣的主要成分是
 溶解的离子反应方程式为
溶解的离子反应方程式为(2)“步骤Ⅰ”中加入
 后选择合适试剂调pH,再将溶液加热煮沸一段时间,加热煮沸的目的是
后选择合适试剂调pH,再将溶液加热煮沸一段时间,加热煮沸的目的是(3)草酸用量过多时,钪的沉淀率反而下降,原因是
(4)
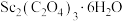 在空气中加热分解时,
在空气中加热分解时, %随温度变化如图所示。
%随温度变化如图所示。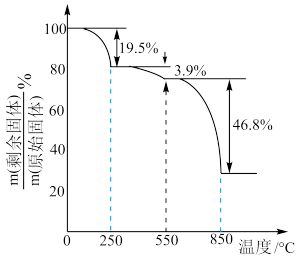
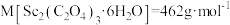 。
。250℃时固体的主要成分是:
(5)传统制备
 的方法是先得到
的方法是先得到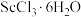 沉淀,再高温脱水得
沉淀,再高温脱水得 ,但通常含有
,但通常含有 杂质,原因是
杂质,原因是(6)“加热氯化”过程主要发生反应的化学方程式为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某品牌糖衣片补血剂,除去糖衣后显淡蓝绿色,主要成分是硫酸亚铁,不含其他铁的化合物。某研究性学习小组为测定该补血剂中硫酸亚铁的含量进行了以下探究:
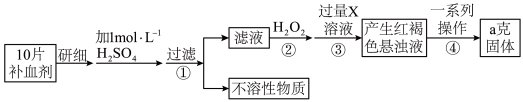
请回答下列问题:
(1)用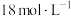 的浓硫酸配制100 mL
的浓硫酸配制100 mL  的硫酸溶液.所需浓硫酸的体积为
的硫酸溶液.所需浓硫酸的体积为________ mL(计算结果保留一位小数)。
(2)下列操作中,容量瓶所具备的功能有________(填字母)。
(3)在下列配制过程示意图中,有错误的是(填字母)________ 。

(4)下列说法正确的________。
(5)验证步骤②反应后的溶液中是否含有 的实验操作为
的实验操作为_____________________ (可选择的试剂有氯水、KSCN溶液、NaOH溶液、酸性 溶液)。
溶液)。
(6)步骤②加入适量 发生反应的离子方程式为
发生反应的离子方程式为____________________ 。
(7)经一系列操作后,所获得固体的质量为 ,则每片补血剂中含硫酸亚铁的质量为
,则每片补血剂中含硫酸亚铁的质量为________ g。

请回答下列问题:
(1)用
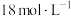 的浓硫酸配制100 mL
的浓硫酸配制100 mL  的硫酸溶液.所需浓硫酸的体积为
的硫酸溶液.所需浓硫酸的体积为(2)下列操作中,容量瓶所具备的功能有________(填字母)。
| A.配制一定体积准确浓度的标准溶液 |
| B.长期贮存溶液 |
| C.用来溶解固体溶质 |
| D.常用来代替量筒量取一定体积的液体 |
(3)在下列配制过程示意图中,有错误的是(填字母)

(4)下列说法正确的________。
| A.洗涤烧杯2~3次,并将洗涤液移入容量瓶以减少误差 |
| B.某同学将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低 |
| C.定容时仰视观察,所配溶液浓度会偏低 |
| D.容量瓶使用前先要检查是否漏液,具体操作是向容量瓶中加蒸馏水,倒置不漏液即可 |
(5)验证步骤②反应后的溶液中是否含有
 的实验操作为
的实验操作为 溶液)。
溶液)。(6)步骤②加入适量
 发生反应的离子方程式为
发生反应的离子方程式为(7)经一系列操作后,所获得固体的质量为
 ,则每片补血剂中含硫酸亚铁的质量为
,则每片补血剂中含硫酸亚铁的质量为
您最近一年使用:0次
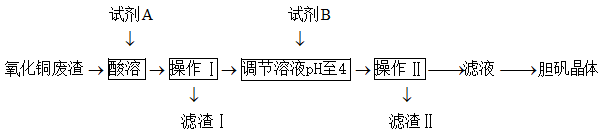
【推荐1】实验室利用氧化铜废渣(含少量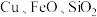 )制取胆矾晶体(
)制取胆矾晶体(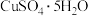 )的操作流程如下:
)的操作流程如下:
已知:生成氢氧化物沉淀的
(1)操作Ⅰ是___________ ,此步骤使用到的玻璃仪器有烧杯、___________ 和___________ 。
(2)滤渣Ⅰ的化学式是___________ ,滤渣Ⅱ的化学式是___________ 。
(3)试剂A为稀硫酸和 的混合物。
的混合物。
①写出 和试剂A反应的化学方程式
和试剂A反应的化学方程式___________ 。
②试制A中的 不能换成
不能换成 说明理由
说明理由___________ 。
(4)试剂B最好选用下列物质中的___________(填序号)。
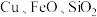 )制取胆矾晶体(
)制取胆矾晶体(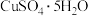 )的操作流程如下:
)的操作流程如下:
已知:生成氢氧化物沉淀的

| 沉淀物 | 开始沉淀的 | 沉淀完全的 |
 | 2.7 | 3.7 |
 | 4.7 | 6.7 |
(1)操作Ⅰ是
(2)滤渣Ⅰ的化学式是
(3)试剂A为稀硫酸和
 的混合物。
的混合物。①写出
 和试剂A反应的化学方程式
和试剂A反应的化学方程式②试制A中的
 不能换成
不能换成 说明理由
说明理由(4)试剂B最好选用下列物质中的___________(填序号)。
A. | B. | C. | D. |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】以黄铁矿(主要成分 )为原料生产硫酸,并将产出的炉渣和尾气进行资源综合利用,减轻对环境的污染,其中一种流程如下图所示。
)为原料生产硫酸,并将产出的炉渣和尾气进行资源综合利用,减轻对环境的污染,其中一种流程如下图所示。

资料:已知
(1) 中硫元素的化合价为
中硫元素的化合价为_______ 。
(2)“氧化”时,反应的化学方程式为_______ 。
(3)工业上,吸收 时宜选用的试剂X为
时宜选用的试剂X为_______ ,不能直接用水吸收的原因是_______ 。
(4)因为 在保存过程中易被氧化,导致商品
在保存过程中易被氧化,导致商品 中存在
中存在 。欲检验
。欲检验 已变质的实验方法为
已变质的实验方法为_______ 。
(5) 可用于葡萄酒的抗氧化剂。用碘标准液可测定葡萄酒中
可用于葡萄酒的抗氧化剂。用碘标准液可测定葡萄酒中 的残留量,请配平该反应的离子方程式:
的残留量,请配平该反应的离子方程式:_______ 。
_______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______
(6)查阅资料知:“尾气”可用双碱脱硫法处理,其过程如图所示。

①写出过程I的离子反应方程式_______ 。
②过程II反应中氧化剂与还原剂的物质的量之比为_______ 。
 )为原料生产硫酸,并将产出的炉渣和尾气进行资源综合利用,减轻对环境的污染,其中一种流程如下图所示。
)为原料生产硫酸,并将产出的炉渣和尾气进行资源综合利用,减轻对环境的污染,其中一种流程如下图所示。
资料:已知

(1)
 中硫元素的化合价为
中硫元素的化合价为(2)“氧化”时,反应的化学方程式为
(3)工业上,吸收
 时宜选用的试剂X为
时宜选用的试剂X为(4)因为
 在保存过程中易被氧化,导致商品
在保存过程中易被氧化,导致商品 中存在
中存在 。欲检验
。欲检验 已变质的实验方法为
已变质的实验方法为(5)
 可用于葡萄酒的抗氧化剂。用碘标准液可测定葡萄酒中
可用于葡萄酒的抗氧化剂。用碘标准液可测定葡萄酒中 的残留量,请配平该反应的离子方程式:
的残留量,请配平该反应的离子方程式:_______
 _______
_______ _______
_______ _______
_______ _______
_______ _______
_______(6)查阅资料知:“尾气”可用双碱脱硫法处理,其过程如图所示。

①写出过程I的离子反应方程式
②过程II反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】冬奥会国家速滑馆又称为“冰丝带”,所用的碲化镉(CdTe)发电玻璃被誉为“挂在墙上的油田”。镉(Cd)可用于制作发光电子组件,以铜镉废渣(含Cu、Cd、Zn、Fe等单质)为原料制备镉的工艺流程如下:

浸出后的溶液中含有 、
、 、
、 等金属离子,相关金属离子形成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol·L
等金属离子,相关金属离子形成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol·L 计算)如下表:
计算)如下表:
(1)可加快“浸出”速率的措施有:___________ (任写一条);“浸出”时通入氮气而不是通入空气的原因是:___________ 。
(2)“氧化”时发生反应的离子方程式为:___________ ;使用 为氧化剂的优点是:
为氧化剂的优点是:___________ 。
(3)“调pH”时控制溶液pH在3.3~5.9之间,“滤渣”的主要成分是___________ (填化学式)。
(4)“置换”时发生反应的离子方程式为:___________ 。

浸出后的溶液中含有
 、
、 、
、 等金属离子,相关金属离子形成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol·L
等金属离子,相关金属离子形成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol·L 计算)如下表:
计算)如下表:| 氢氧化物 |  |  |  |
| 开始沉淀的pH | 1.5 | 5.9 | 7.2 |
| 沉淀完全的pH | 3.3 | 8.9 | 9.9 |
(2)“氧化”时发生反应的离子方程式为:
 为氧化剂的优点是:
为氧化剂的优点是:(3)“调pH”时控制溶液pH在3.3~5.9之间,“滤渣”的主要成分是
(4)“置换”时发生反应的离子方程式为:
您最近一年使用:0次



