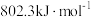下列说法正确的是
| A.1gH2完全燃烧生成H2O(g)放出的热量叫H2的热值 |
| B.25℃、101kPa时,1molS和2molS的燃烧热相等 |
C.已知S(s)+ O2(g)=SO3(g) ∆H=-269.8kJ/mol,则该反应的反应热为269.8kJ/mol O2(g)=SO3(g) ∆H=-269.8kJ/mol,则该反应的反应热为269.8kJ/mol |
| D.25℃、101kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3kJ·mol-1,硫酸溶液与氢氧化钾溶液反应的热化学方程式为H2SO4(aq)+2KOH(aq)=K2SO4(aq)+2H2O(l) ΔH=-57.3kJ·mol-1 |
更新时间:2022-12-16 09:38:04
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】下列说法正确的是



A.已知甲烷的燃烧热为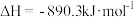 ,则甲烷燃烧的热化学方程式可表示为 ,则甲烷燃烧的热化学方程式可表示为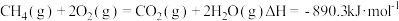 |
| B.当反应物的总能量低于生成物的总能量时,该反应必须加热才能发生 |
C.上图是 、 、 时, 时, 和 和 合成 合成 的反应过程中的能量变化曲线图,则该反应的热化学方程式为 的反应过程中的能量变化曲线图,则该反应的热化学方程式为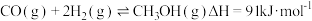 |
D.已知: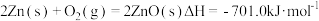 ,则 ,则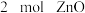 分解成 分解成 固体和 固体和 气体,需吸收 气体,需吸收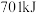 的热量 的热量 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】 在适量的
在适量的 中完全燃烧生成液态
中完全燃烧生成液态 ,放出
,放出 热量。能正确表示
热量。能正确表示 燃烧热的热化学方程式是
燃烧热的热化学方程式是
 在适量的
在适量的 中完全燃烧生成液态
中完全燃烧生成液态 ,放出
,放出 热量。能正确表示
热量。能正确表示 燃烧热的热化学方程式是
燃烧热的热化学方程式是A. 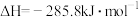 |
B.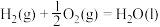 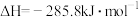 |
C. 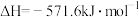 |
D.  |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】根据如图所示示意图,下列说法不正确的是( )
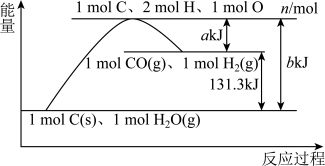

| A.反应的热化学方程式可表示为C(s)+H2O(g)=CO(g)+H2(g) ΔH=(b-a) kJ·mol-1 |
| B.该反应过程反应物断键吸收的能量大于生成物成键放出的能量 |
| C.amol C和amol H2O(l)反应生成amol CO和a mol H2吸收的热量一定为131.3a kJ |
| D.1mol C、2mol H、1mol O转变成1mol CO(g)和1mol H2(g)放出的热量为a kJ |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列叙述不正确的是
| A.测定中和热实验中常用稍过量的NaOH溶液的原因是为保证盐酸完全被中和 |
| B.酸与碱发生反应放出的热量即为中和热 |
| C.碳酸钙的分解是吸热反应 |
| D.测定反应初始温度和终止温度重复三次的原因是减少实验误差,增加实验的准确度 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列关于反应能量的说法正确的是
| A.若反应A(s)=B(s),ΔH <0,则说明A物质比B物质稳定,分子内共价键键能A比B大 |
| B.Zn(s)+ CuSO4(aq) = ZnSO4(aq) + Cu(s) ΔH =- 216 kJ·mol-1, 则反应物总能量>生成物总能量 |
C.101kPa时,2C(s) + O2(g)= 2CO(g) ΔH =- Q kJ·mol-1,则C的燃烧热为 Q kJ·mol-1 Q kJ·mol-1 |
| D.H+(aq) + OH-(aq)= H2O(l) ΔH =- 57.3 kJ·mol-1,含1mol NaOH的氢氧化钠溶液与含0.5molH2SO4的浓硫酸混合后放出57.3kJ的热量 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列关于燃烧热的说法中正确的是( )
| A.燃烧热是指1mol物质燃烧所放出的热量 |
| B.燃烧热是指常温下,可燃物燃烧放出的热量 |
| C.燃烧热是指1.01×105Pa时,1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量 |
| D.燃烧热随化学计量数的改变而改变 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列说法正确的是
A.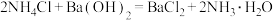  ,该反应为吸热反应,必须加热才能发生 ,该反应为吸热反应,必须加热才能发生 |
B.已知反应: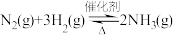 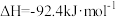 ,则取 ,则取  和 和  充分反应,放出的热量小于 充分反应,放出的热量小于 |
C.已知:  ; ;  ,则 ,则 |
D.在 时, 时, 物质燃烧时放出的热量叫该物质的燃烧热 物质燃烧时放出的热量叫该物质的燃烧热 |
您最近半年使用:0次
【推荐3】下列说法或表示方法错误 的是
| A.盖斯定律实质上是能量守恒定律的体现 |
| B.一定条件下,0.5molN2和1.5molH2充分反应后放出35.5 kJ热量,则N2(g)+3H2(g)⇌2NH3(g) ΔH=-71kJ/mol |
| C.由于反应情况不同,反应热可分为燃烧热,中和热等 |
| D.在稀溶液中:H+(aq)+OH-(aq)=H2O(l);∆H =-57.3kJ/mol,若将含0.5mol H2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3kJ |
您最近半年使用:0次

 在光照和点燃条件下的
在光照和点燃条件下的 不同
不同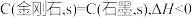 ,则石墨比金刚石稳定
,则石墨比金刚石稳定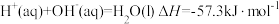 可知,稀醋酸与
可知,稀醋酸与 溶液反应生成
溶液反应生成 液态水时释放
液态水时释放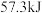 的热量
的热量 ,表示甲烷的燃烧热为
,表示甲烷的燃烧热为