下列说法或表示方法错误 的是
| A.盖斯定律实质上是能量守恒定律的体现 |
| B.一定条件下,0.5molN2和1.5molH2充分反应后放出35.5 kJ热量,则N2(g)+3H2(g)⇌2NH3(g) ΔH=-71kJ/mol |
| C.由于反应情况不同,反应热可分为燃烧热,中和热等 |
| D.在稀溶液中:H+(aq)+OH-(aq)=H2O(l);∆H =-57.3kJ/mol,若将含0.5mol H2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3kJ |
更新时间:2021-10-22 22:31:46
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】在下列各说法中,正确的是
| A.热化学方程式中的化学计量数可以是分数 | B. 表示放热反应, 表示放热反应, 表示吸热反应 表示吸热反应 |
C. 的大小与热化学方程式中的计量数无关 的大小与热化学方程式中的计量数无关 | D.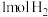 与 与 反应放出的热就是 反应放出的热就是 的燃烧热 的燃烧热 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】现有如下3个热化学方程式:
①H2(g)+ O2(g) = H2O(g) ΔH1= - akJ⋅mol-1;
O2(g) = H2O(g) ΔH1= - akJ⋅mol-1;
②H2(g)+ O2(g) = H2O(l) ΔH2= - bkJ⋅mol-1;
O2(g) = H2O(l) ΔH2= - bkJ⋅mol-1;
③2H2(g)+ O2(g) = 2H2O(l) ΔH3= - ckJ⋅mol-1;
关于它们的下列表述中,原因和结论都正确的是( )
①H2(g)+
 O2(g) = H2O(g) ΔH1= - akJ⋅mol-1;
O2(g) = H2O(g) ΔH1= - akJ⋅mol-1;②H2(g)+
 O2(g) = H2O(l) ΔH2= - bkJ⋅mol-1;
O2(g) = H2O(l) ΔH2= - bkJ⋅mol-1;③2H2(g)+ O2(g) = 2H2O(l) ΔH3= - ckJ⋅mol-1;
关于它们的下列表述中,原因和结论都正确的是( )
| A.H2的燃烧是放热反应,则a、b、c均大于0 |
| B.方程式①和②中物质的种类和化学计量数均相同,则a=b |
| C.方程式①和③中H2O的状态和化学计量数不同,则c<2a |
| D.方程式③的化学计量数是②的2倍,则ΔH2<ΔH3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的一种反应原理如下:CH3OH(g)+H2O(g)→CO2(g)+3H2(g)–49.0kJ。下列说法正确的是( )
| A.1LCH3OH蒸汽与1L水蒸气反应生成1LCO2气体与3L氢气吸收热量49.0kJ |
| B.1个CH3OH分子与1个水分子反应生成1个CO2分子与3个H2分子吸收49.0kJ热量 |
| C.相同条件下1molCH3OH(g)与1molH2O(g)的能量总和小于1molCO2(g)与3molH2(g)的能量总和 |
| D.1molCH3OH蒸汽与1mol液态水反应生成1molCO2气体与3mol氢气吸收的热量小于49.0kJ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列有关中和热实验的说法正确的是( )
| A.用铜丝替代环形玻璃搅拌棒,测得△H偏高 |
| B.强酸与强碱反应生成的水越多,该反应的中和热越大 |
| C.强酸与强碱反应生成1mol水的△H都约为-57.3kJ·mol-1 |
| D.测定中和热实验中,读取混合溶液不再变化的温度为终止温度 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】在下列说法中正确的是
| A.化学反应过程中一定有热量释放出来 |
B.已知C(s)+ O2(g)==CO(g) △H=-110.5kJ/mol,说明碳的燃烧热为110.5kJ/mol O2(g)==CO(g) △H=-110.5kJ/mol,说明碳的燃烧热为110.5kJ/mol |
| C.1molH2SO4与1molBa(OH)2反应生成BaSO4沉淀时放出的热叫做中和热 |
| D.同温同压下,已知两个放热反应:2A(l)+ B(l) == 2C(g) ΔH1;2A(g)+B(g)== 2C(l) △H2,则ΔH1>ΔH2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】如表所列的“依据”能推导出后面的“结论”的是
| 依据 | 结论 | |
| A | CH4(g)+2O2(g)= CO2(g)+2H2O(g)ΔH=-801.3kJ·mol-1 | CH4的燃烧热ΔH=-801.3kJ·mol-1 |
| B | Sn(灰,s)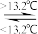 Sn(白,s)ΔH=+2.1kJ·mol-1 Sn(白,s)ΔH=+2.1kJ·mol-1 | 白锡制品在寒冷的冬天因易转化为灰状锡而损坏 |
| C | 稀溶液中:H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3kJ·mol-1 | 盐酸与氨水反应的中和热为57.3kJ·mol-1 |
| D | C(墨,s)+O2(g)=CO2(g)ΔH=-393.5kJ·mol-1 C(金刚石,s)+O2(g)=CO2(g)ΔH=-395kJ·mol-1 | 石墨转化为金刚石会放出热量 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列说法错误 的是
A.同温同压下, 在光照和点燃条件下的ΔH相同 在光照和点燃条件下的ΔH相同 |
| B.化学键断裂和形成时的能量变化是化学反应中能量变化的主要原因 |
C.甲烷的燃烧热为890.3kJ·mol-1,则1molCH4发生反应 放出的热量小于890.3kJ 放出的热量小于890.3kJ |
D.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放出热量19.3kJ,其热化学方程式可表示为: 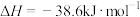 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】单质碳、 均是重要的燃料,下列有关比较中(
均是重要的燃料,下列有关比较中( :表示燃烧热)一定正确的是
:表示燃烧热)一定正确的是
 均是重要的燃料,下列有关比较中(
均是重要的燃料,下列有关比较中( :表示燃烧热)一定正确的是
:表示燃烧热)一定正确的是A.能量: | B. |
C.燃烧时放出的热量: | D.通常情况下易燃性: |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】下列有关热化学方程式的叙述中,正确的是( )
A.对于反应CO(g)+H2O(g)  CO2(g)+H2(g) ΔH<0,升温ΔH不变 CO2(g)+H2(g) ΔH<0,升温ΔH不变 |
| B.已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 |
| C.已知2H2(g)十O2(g)=2H2O(g) △H = -483.6 kJ/mol,则H2的燃烧热为 241.8 kJ/mol |
| D.已知2C(s)+2O2(g)=2CO2(g) △H1,2C(s)+O2(g)=2CO(g) △H2 ,则△H1>△H2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】Zewail创立的飞秒(1fs=10-15s)化学研究了极短时间内的反应历程,巧妙地解决了如何确定反应起点问题。例如HI与CO2 的反应过程片段为:H+OCO→HOCO→1000fs→HO+CO。下列有关说法不正确的是
| A.加入合适的催化剂可以加快该反应的速率 |
| B.该反应的起点是HI离解为H和I自由基,HOCO为中间产物 |
| C.HOCO经1000fs离解为HO自由基和CO,说明HI与CO2的反应速率极快 |
| D.飞秒化学展现的反应历程可以体现化学反应的实质是旧键断裂和新键形成 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】等质量的固体硫和硫蒸气分别在相同条件下完全燃烧,放出的热量
| A.前者多 | B.后者多 | C.两者相等 | D.无法比较 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】化学反应中,能量的测定和利用是关乎可持续发展的重要课题。下列相关叙述正确的是( )
| A.应用盖斯定律,可计算某些难以直接测量的反应热 |
| B.将锌片直接放入足量稀硫酸中,另取同样的锌片与铜片用导线连接后再放入足量的稀硫酸中,充分反应后,两者放出的热量相同 |
| C.已知H2和Cl2在混合光照时发生爆炸,而H2在Cl2中点燃能安静燃烧,说明在同温同压下H2(g)+Cl2(g)═2HCl(g),反应条件不同,△H也不同 |
| D.为了充分利用热能,可在燃烧时通入大量的空气以确保燃料完全燃烧 |
您最近一年使用:0次



