I.某天然油脂的分子式为C57H106O6 ,1 mol该油脂完全水解可得到1 mol甘油、1 mol脂肪酸X、2 mol脂肪酸Y。经测定X的相对分子质量为284,原子个数比C∶H∶O=9∶18∶1。
(1)下列物质在一定条件下能与X发生反应的有_______ 。
A.氢气 B.乙醇 C.溴水 D.烧碱溶液 E.高锰酸钾酸性溶液
(2)Y的分子式为_______ 。
II.某同学在实验室利用橄榄油与甲醇制备生物柴油(高级脂肪酸甲酯),其原理及实验步骤如下:
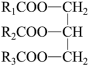 +3CH3OH
+3CH3OH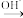
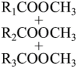 (高级脂肪酸甲酯) +
(高级脂肪酸甲酯) + 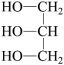
①称取9.2g CH3OH和0.56g KOH依次放入锥形瓶,充分振荡得KOH甲醇溶液
②将40g橄榄油(平均相对分子质量279~286)、40g 正己烷(作溶剂)、配好的KOH甲醇溶液一次加入到三颈烧瓶中;
③连接好装置(如图,固定装置省略),保持反应温度在60~64℃左右,搅拌速度350r/min,回流1.5h~2h;
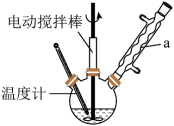
④冷却、分液、水洗、回收溶剂并得到生物柴油。
回答下列问题:
(3)油脂在碱性条件下发生的水解反应称为___ 反应。
(4)装置中仪器a的名称是___ ,保持反应温度在60~64℃左右最好采用的加热方式为___
(5)实验中甲醇过量的主要目的是:___ ; KOH 的用量不宜过多,其原因是:___
(6)步骤④的液体分为两层,上层为生物柴油、正己烷和甲醇。分离出的上层液体需用温水洗涤,能说明已洗涤干净的操作依据是:__
(1)下列物质在一定条件下能与X发生反应的有
A.氢气 B.乙醇 C.溴水 D.烧碱溶液 E.高锰酸钾酸性溶液
(2)Y的分子式为
II.某同学在实验室利用橄榄油与甲醇制备生物柴油(高级脂肪酸甲酯),其原理及实验步骤如下:
 +3CH3OH
+3CH3OH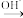
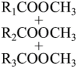 (高级脂肪酸甲酯) +
(高级脂肪酸甲酯) + 
①称取9.2g CH3OH和0.56g KOH依次放入锥形瓶,充分振荡得KOH甲醇溶液
②将40g橄榄油(平均相对分子质量279~286)、40g 正己烷(作溶剂)、配好的KOH甲醇溶液一次加入到三颈烧瓶中;
③连接好装置(如图,固定装置省略),保持反应温度在60~64℃左右,搅拌速度350r/min,回流1.5h~2h;

④冷却、分液、水洗、回收溶剂并得到生物柴油。
回答下列问题:
(3)油脂在碱性条件下发生的水解反应称为
(4)装置中仪器a的名称是
(5)实验中甲醇过量的主要目的是:
(6)步骤④的液体分为两层,上层为生物柴油、正己烷和甲醇。分离出的上层液体需用温水洗涤,能说明已洗涤干净的操作依据是:
更新时间:2022-12-17 18:51:45
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A是汽油裂化得到的一种气态烷经,B可用作水果的催熟剂,H是一种高分子化合物。以A为原料合成G和H的流程如图所示:
(1)将一定量A在足量的纯氧中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现二者分别增重4.5g和8.8g,则A的分子式为___________ ,其结构简式为___________ 。
(2)B的电子式为___________ ,E中含有的官能团名称为___________ ,⑤的反应类型为___________ 。
(3)反应③的化学方程式为___________ 。
(4)G与NaOH溶液反应的化学方程式为___________ 。
(5)下列说法正确的是___________。
(6)苯甲酸乙酯难溶于冷水,微溶于热水,与乙醇、乙醚等互溶。天然存在于桃、菠萝、红茶中,常用于配制香水、香精和人造精油。已知氯乙烷和NaOH水溶液在加热条件发生反应: ,完成以甲苯和乙醇为主要原料合成苯甲酸乙酯的合成路线图,在横线上写出主要产物的结构简式(反应条件略)
,完成以甲苯和乙醇为主要原料合成苯甲酸乙酯的合成路线图,在横线上写出主要产物的结构简式(反应条件略)_______ 、_______ 、_______ 。
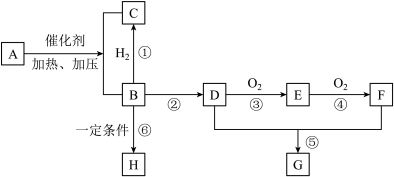
(1)将一定量A在足量的纯氧中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现二者分别增重4.5g和8.8g,则A的分子式为
(2)B的电子式为
(3)反应③的化学方程式为
(4)G与NaOH溶液反应的化学方程式为
(5)下列说法正确的是___________。
| A.H是纯净物 |
| B.A、C属于同系物 |
| C.D和F都能与金属钠反应,且F更剧烈 |
| D.G在碱性条件下的水解反应可称为皂化反应 |
 ,完成以甲苯和乙醇为主要原料合成苯甲酸乙酯的合成路线图,在横线上写出主要产物的结构简式(反应条件略)
,完成以甲苯和乙醇为主要原料合成苯甲酸乙酯的合成路线图,在横线上写出主要产物的结构简式(反应条件略)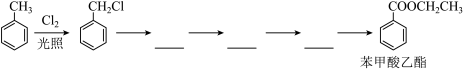
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】锰在冶金工业、电子工业等方面有广泛应用。某软锰矿的主要成分为MnO2、SiO2、CaO和少量的MgO、CuO,一种利用废铁屑还原浸出该软锰矿并制取金属锰的工艺流程如下:
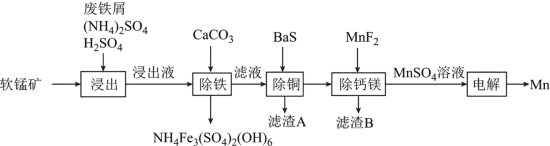
(1)废铁屑表面含有油脂,除去表面油脂的方法是___________ 。
(2)写出“浸出”时Fe与MnO2反应的离子方程式:___________ 。
(3)“除铁”时加入CaCO3的主要作用是___________ ;滤渣A的主要成分为___________ 、___________ (填化学式)。
(4)除铁后的滤液若酸性过强,加入BaS溶液后可能造成污染,原因是___________ 。(用离子反应方程式表示)
(5)电解硫酸锰溶液的装置示意图如下:
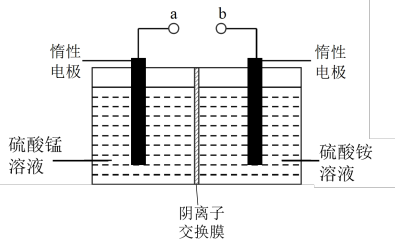
电解时Mn在___________ (填“阴”或“阳”)极析出,阳极产生O2的电极反应式为___________ ,阳极室的溶液可返回上述“___________ ”工序循环使用。

(1)废铁屑表面含有油脂,除去表面油脂的方法是
(2)写出“浸出”时Fe与MnO2反应的离子方程式:
(3)“除铁”时加入CaCO3的主要作用是
(4)除铁后的滤液若酸性过强,加入BaS溶液后可能造成污染,原因是
(5)电解硫酸锰溶液的装置示意图如下:

电解时Mn在
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】参考下列(a)~(c)项的叙述并回答有关问题。
(a) 皂化值是使1g油脂皂化所需要的氢氧化钾的毫克数。
(b)碘值是100g油脂加成碘的克数。
(c)各种油脂皂化值、碘值列表如下:
(假设下述油脂皆为(RCOO)3C3H5的单甘油酯)
(l)主要成分皆为(C17H33COO)3C3H5(相对分子质量884)形成的油,其皂化值是_________ 。
(2)硬化大豆油的碘值小的原因是______________________________ 。
(3) 使碘值为180的鱼油100g硬化所需要吸收的氢气在标准状况下的体积至少是_____ L。
(a) 皂化值是使1g油脂皂化所需要的氢氧化钾的毫克数。
(b)碘值是100g油脂加成碘的克数。
(c)各种油脂皂化值、碘值列表如下:
花生油 | 亚麻仁油 | 牛油 | 黄油 | 硬化大豆油 | 大豆油 | |
皂化值 | 190 | 180 | 195 | 226 | 193 | 193 |
碘值 | 90 | 182 | 38 | 38 | 5 | 126 |
(l)主要成分皆为(C17H33COO)3C3H5(相对分子质量884)形成的油,其皂化值是
(2)硬化大豆油的碘值小的原因是
(3) 使碘值为180的鱼油100g硬化所需要吸收的氢气在标准状况下的体积至少是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐1】已知:A、B、F是家庭中常见的有机物,F常用于食品包装,E是石油化工发展水平的标志。根据下面转化关系回答问题。
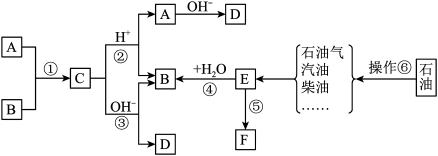
(1)分别写出A和E中官能团的名称:A中_________ ;E中_________ ;
(2)操作⑥的名称为________________ 。
(3)写出反应类型:④_________ ;
(4)请写出下列反应的化学方程式:
①写出A和B在浓硫酸中加热反应的方程式_________________ ;
②B在金属铜存在下在空气中加热反应________________ ;
(5)F是一种常见的高分子材料,它给我们带来了巨大的方便。然而,这种材料造成的当今的某一环境问题是__________________ .

(1)分别写出A和E中官能团的名称:A中
(2)操作⑥的名称为
(3)写出反应类型:④
(4)请写出下列反应的化学方程式:
①写出A和B在浓硫酸中加热反应的方程式
②B在金属铜存在下在空气中加热反应
(5)F是一种常见的高分子材料,它给我们带来了巨大的方便。然而,这种材料造成的当今的某一环境问题是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐2】【化学一选修5: 有机化学基础】有机物H是一种中枢神经兴奋剂,其合成路线如下图所示。
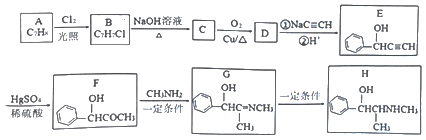
请回答下列问题:
(1)A的化学名称为______ ,C的结构简式为________ 。
(2)E中官能团的名称为______ 。B→C、G→H的反应类型分别为____ 、______ 。
(3)D分子中最多有___ 个原子共平面。
(4)F→G历经两步反应,第一步反应的化学方程式为_______ 。
(5)同时满足下列条件的F的同分异构体有___ 种(不考虑立体异构)。
①能发生银镜反应; ②能与氯化铁溶液反应; ③分子中只有1个甲基。
其中核磁共振氢谱有6组峰的结构简式为___________ 。
(6)最近网上流传,某明星的天价童颜针,其主要成分为聚乳酸,结构简式为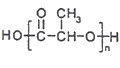 ,它是具有填充、紧致、提拉多重效果的微整形新武器,且具有生理兼容性与可降解性,比传统的硅胶填充整容要先进。参照上述合成路线,以丙烯为原料制备
,它是具有填充、紧致、提拉多重效果的微整形新武器,且具有生理兼容性与可降解性,比传统的硅胶填充整容要先进。参照上述合成路线,以丙烯为原料制备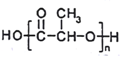 的合成路线流程图(无机试剂任选)
的合成路线流程图(无机试剂任选)____________________ 。

请回答下列问题:
(1)A的化学名称为
(2)E中官能团的名称为
(3)D分子中最多有
(4)F→G历经两步反应,第一步反应的化学方程式为
(5)同时满足下列条件的F的同分异构体有
①能发生银镜反应; ②能与氯化铁溶液反应; ③分子中只有1个甲基。
其中核磁共振氢谱有6组峰的结构简式为
(6)最近网上流传,某明星的天价童颜针,其主要成分为聚乳酸,结构简式为
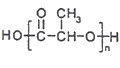 ,它是具有填充、紧致、提拉多重效果的微整形新武器,且具有生理兼容性与可降解性,比传统的硅胶填充整容要先进。参照上述合成路线,以丙烯为原料制备
,它是具有填充、紧致、提拉多重效果的微整形新武器,且具有生理兼容性与可降解性,比传统的硅胶填充整容要先进。参照上述合成路线,以丙烯为原料制备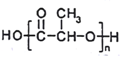 的合成路线流程图(无机试剂任选)
的合成路线流程图(无机试剂任选)
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐3】氧化白藜芦醇W具有抗病毒等作用。下面是利用Heck反应合成W的一种方法:
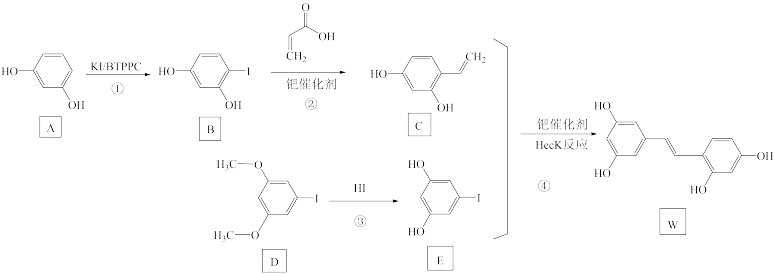
回答下列问题:
(1)A的化学名称为_______ 。
(2)1molA与浓溴水反应最多能消耗_______ molBr2。
(3)B中的官能团名称是_______ 、_______ 。
(4)反应③的类型为_______ ,W的分子式为_______ 。
(5)上述表格中是探究不同条件对反应④产率的影响:
上述实验探究了_______ 和_______ 对反应产率的影响,此外还可以进一步探究_______ 等对反应产率的影响。
(6)X为D的同分异构体,写出满足如下条件的X的结构简式_______ 、_______
①含有苯环
②有三种不同化学环境的氢,个数比为6∶2∶1
③1mol的X与足量金属Na反应可生成2gH2

| 实验 | 碱 | 溶剂 | 催化剂 | 产率/% |
| 1 | KOH | DMF | 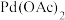 | 22.3 |
| 2 |  | DMF | 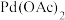 | 10.5 |
| 3 | 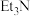 | DMF | 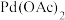 | 12.4 |
| 4 | 六氢吡啶 | DMF | 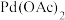 | 31.2 |
| 5 | 六氢吡啶 | DMA | 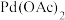 | 38.6 |
| 6 | 六氢吡啶 | NMP | 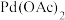 | 24.5 |
(1)A的化学名称为
(2)1molA与浓溴水反应最多能消耗
(3)B中的官能团名称是
(4)反应③的类型为
(5)上述表格中是探究不同条件对反应④产率的影响:
上述实验探究了
(6)X为D的同分异构体,写出满足如下条件的X的结构简式
①含有苯环
②有三种不同化学环境的氢,个数比为6∶2∶1
③1mol的X与足量金属Na反应可生成2gH2
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】叠氮化钠(NaN3)可用于汽车安全气囊的添加剂,与酸反应生成N2和H2。某学习小组在实验室用亚硝酸钠和氨在无氧环境中制备NaN3,设计如下实验(夹持装置略去) :
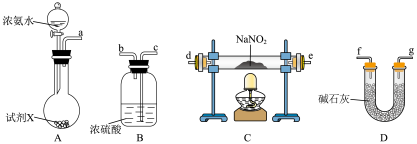
(1)按气流从左到右的方向,上述装置合理的连接顺序为_________________ (填仪器接口字母)。
(2)试剂X 可选用________________ (填试剂名称)。
(3)装置C中发生反应的化学方程式为_________________________________________ ,该反应需要在无氧环境中进行的原因为_______________________________________________ 。
(4)装置B的作用为___________________________________________ 。
(5)加热条件下,NaNH2和N2O反应也可制备NaN3,同时生成能使湿响的红色石蕊试纸变蓝的气体,该反应的化学方程式为_____________________________________________ 。
(6)HNO2是一元弱酸,不稳定,容易分解为两种氮的氧化物。现用如下试剂:NaNO2、pH试纸、水、稀硫酸、NaOH溶液、碱石灰、CuSO4、CuO,计实验证明((可加热);
①HNO2为弱酸____________________________________________________ 。
②装置C中反应进行一段时间后,有NaN3生成______________________________________ 。

(1)按气流从左到右的方向,上述装置合理的连接顺序为
(2)试剂X 可选用
(3)装置C中发生反应的化学方程式为
(4)装置B的作用为
(5)加热条件下,NaNH2和N2O反应也可制备NaN3,同时生成能使湿响的红色石蕊试纸变蓝的气体,该反应的化学方程式为
(6)HNO2是一元弱酸,不稳定,容易分解为两种氮的氧化物。现用如下试剂:NaNO2、pH试纸、水、稀硫酸、NaOH溶液、碱石灰、CuSO4、CuO,计实验证明((可加热);
①HNO2为弱酸
②装置C中反应进行一段时间后,有NaN3生成
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】乙二醛(OHC-CHO)是一种重要的精细化工产品。某小组利用乙醛液相硝酸氧化法制备乙二醛并测定乙二醛纯度,装置如图所示:
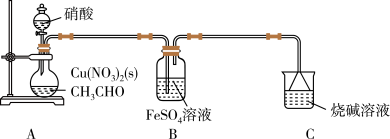
已知:①NO+FeSO4=FeSO4·NO(棕色)。
②几种有机物的部分性质如表所示:
实验步骤:
①取20 mL乙醛装于烧瓶,加入2 g Cu(NO3)2粉末作催化剂,向烧瓶中缓慢滴加2 mol·L-1硝酸至乙醛完全反应为止;
②提纯产品,最终得到10.0 mL产品。
请回答下列问题:
(1)盛装硝酸的仪器名称是___________ 。
(2)实验中,观察到装置B中溶液变为棕色,制备乙二醛的化学方程式为________________ 。
(3)向烧瓶中滴加硝酸要“缓慢”,其目的是___________ ;判断烧瓶中制备乙二醛的反应已完成的标志是___________ 。
(4)分离提纯产品,宜选择下列装置___________ (填字母)。
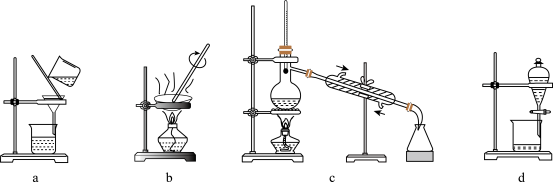
(5)根据上述实验数据,该实验中乙二醛的产率约为___________ (填字母)。
a.56.5% b.61.8% c.67.9% d.72.6%
(6)实验室可用酸性KMnO4溶液测定乙二醛的纯度,发生反应的离子方程式为:18H++6MnO4-+5C2H2O2→10CO2↑+6Mn2++14H2O。实验步骤如下:取V mL产品,加蒸馏水稀释至250 mL,量取25.00 mL稀释后的溶液于锥形瓶,滴加5.00 mL稀硫酸,用c mol·L-1 KMnO4溶液,三次平行实验消耗KMnO4溶液体积如下:
滴定终点的标志是___________ ;该产品纯度为___________ g·mL-1(用含V和c的代数式表示)。

已知:①NO+FeSO4=FeSO4·NO(棕色)。
②几种有机物的部分性质如表所示:
| 乙醛 | 乙二醛 | 乙二酸 | 乙酸 | |
| 沸点/℃ | 20.8 | 50.5 | 109 | 117.9 |
| 溶解性 | 与水、有机溶剂互溶 | 溶于水、乙醇等 | 溶于水和有机溶剂 | 与水、乙醇互溶 |
| 密度/g∙cm-3 | 0.78 | 1.27 | 1.90 | 1.05 |
| 相对分子质量 | 44 | 58 | 90 | 60 |
①取20 mL乙醛装于烧瓶,加入2 g Cu(NO3)2粉末作催化剂,向烧瓶中缓慢滴加2 mol·L-1硝酸至乙醛完全反应为止;
②提纯产品,最终得到10.0 mL产品。
请回答下列问题:
(1)盛装硝酸的仪器名称是
(2)实验中,观察到装置B中溶液变为棕色,制备乙二醛的化学方程式为
(3)向烧瓶中滴加硝酸要“缓慢”,其目的是
(4)分离提纯产品,宜选择下列装置

(5)根据上述实验数据,该实验中乙二醛的产率约为
a.56.5% b.61.8% c.67.9% d.72.6%
(6)实验室可用酸性KMnO4溶液测定乙二醛的纯度,发生反应的离子方程式为:18H++6MnO4-+5C2H2O2→10CO2↑+6Mn2++14H2O。实验步骤如下:取V mL产品,加蒸馏水稀释至250 mL,量取25.00 mL稀释后的溶液于锥形瓶,滴加5.00 mL稀硫酸,用c mol·L-1 KMnO4溶液,三次平行实验消耗KMnO4溶液体积如下:
| 实验 | Ⅰ | Ⅱ | Ⅲ |
| V[KmnO4(aq)]/mL | 20.05 | 22.40 | 19.95 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,该厂用上述废金属屑制取新型高效水处理剂Na2FeO4(高铁酸钠)等产品,过程如下:
I. 向废金属屑中加入过量的NaOH溶液,充分反应后过滤;
II. 向I所得固体中加入过量稀H2SO4,充分反应后过滤;
III. 向II所得固体中继续加入热的稀H2SO4,同时不断鼓入空气,固体溶解得CuSO4溶液;
IV. ……
(1)步骤I中发生反应的化学方程式为_________ 、_________ 。
(2)步骤II所得的滤液中加入KSCN溶液无明显现象,表明滤液中不存在Fe3+,用离子方程式解释其可能的原因_________ 。
(3)步骤III获得CuSO4溶液的离子方程式为_________ 。
(4)步骤II所得滤液经进一步处理可制得Na2FeO4,流程如下:

写出由Fe(OH)3制取Na2FeO4的化学方程式__________________________ 。
I. 向废金属屑中加入过量的NaOH溶液,充分反应后过滤;
II. 向I所得固体中加入过量稀H2SO4,充分反应后过滤;
III. 向II所得固体中继续加入热的稀H2SO4,同时不断鼓入空气,固体溶解得CuSO4溶液;
IV. ……
(1)步骤I中发生反应的化学方程式为
(2)步骤II所得的滤液中加入KSCN溶液无明显现象,表明滤液中不存在Fe3+,用离子方程式解释其可能的原因
(3)步骤III获得CuSO4溶液的离子方程式为
(4)步骤II所得滤液经进一步处理可制得Na2FeO4,流程如下:

写出由Fe(OH)3制取Na2FeO4的化学方程式
您最近一年使用:0次



