回答下列问题
(1)已知反应Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
①反应中氧化剂和还原剂的个数比为___________ 。
②浓硝酸在反应中表现的性质是___________ (填序号)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
③写出该反应的离子方程式:___________ 。
(2)某一反应体系有反应物和生成物共五种物质; 2、H2
2、H2 O4、
O4、 (OH)3、H2O、H2
(OH)3、H2O、H2 2。
2。
已知该反应中H2O2只发生如下过程:H2 2→
2→ 2
2
①该反应中的还原剂是___________ 。
②该反应中,发生还原反应的过程是___________ →___________ 。
③写出该反应的化学方程式,并用双线桥标出电子转移的方向和数目:___________ 。
(1)已知反应Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
①反应中氧化剂和还原剂的个数比为
②浓硝酸在反应中表现的性质是
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
③写出该反应的离子方程式:
(2)某一反应体系有反应物和生成物共五种物质;
 2、H2
2、H2 O4、
O4、 (OH)3、H2O、H2
(OH)3、H2O、H2 2。
2。已知该反应中H2O2只发生如下过程:H2
 2→
2→ 2
2①该反应中的还原剂是
②该反应中,发生还原反应的过程是
③写出该反应的化学方程式,并用双线桥标出电子转移的方向和数目:
更新时间:2022-12-21 23:45:54
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】按要求填空
(1) 的电离方程式
的电离方程式___________ 。
(2)汽车尾气的主要成分是 和
和 ,在催化剂的作用下,可将其转变成两种无毒的气体,写出对应的化学方程式
,在催化剂的作用下,可将其转变成两种无毒的气体,写出对应的化学方程式___________ 。
(3)现有以下物质:①液态 ②熔融的
②熔融的 ③
③ 固体④
固体④ 溶液⑤
溶液⑤ ⑥
⑥
能导电的是___________ (填序号,下同),属于电解质的是___________ ,属于非电解质的是___________ 。③的水溶液与④反应的离子反应方程式___________ 。
(1)
 的电离方程式
的电离方程式(2)汽车尾气的主要成分是
 和
和 ,在催化剂的作用下,可将其转变成两种无毒的气体,写出对应的化学方程式
,在催化剂的作用下,可将其转变成两种无毒的气体,写出对应的化学方程式(3)现有以下物质:①液态
 ②熔融的
②熔融的 ③
③ 固体④
固体④ 溶液⑤
溶液⑤ ⑥
⑥
能导电的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】现有下列10种物质:①铝,②纯醋酸,③CO2,④H2SO4,⑤NaOH,⑥硫酸铜溶液,⑦熔融的NaCl,⑧NaHSO4,⑨硝酸钾晶体,⑩乙醇。
(1)上述物质中属于非电解质的有_______ (填序号)。
(2)向⑥中加入⑤的离子方程式是_______ 。该反应属于_______ (填“氧化还原反应”或“非氧化还原反应”)。
(3)②与⑤反应的离子方程式为_______ 。
(4)上述物质中有两种物质在水溶液中发生的反应可用离子反应H++OH-=H2O表示,请写出该离子反应对应的其中一个化学方程式:_______ 。
(1)上述物质中属于非电解质的有
(2)向⑥中加入⑤的离子方程式是
(3)②与⑤反应的离子方程式为
(4)上述物质中有两种物质在水溶液中发生的反应可用离子反应H++OH-=H2O表示,请写出该离子反应对应的其中一个化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】写出下列个反应的方程式。
(1)钠和水的反应____________________________________ (写出离子方程式)。
(2)过氧化钠和二氧化碳的反应_____________________ (写出化学方程式)。
(3)铜与稀硝酸反应___________________________________ (写出化学方程式)。
(4)向FeBr2通入等物质的量的Cl2______________________ (写出离子方程式)。
(5)Cl2通入NaOH溶液中___________________ (写出化学方程式)。
(1)钠和水的反应
(2)过氧化钠和二氧化碳的反应
(3)铜与稀硝酸反应
(4)向FeBr2通入等物质的量的Cl2
(5)Cl2通入NaOH溶液中
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】已知:浓硝酸和铜在常温下反应的化学方程式为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O。回答下列问题:
(1)在这个反应中,浓硝酸表现的化学性质是____ 性(填“酸”或“碱”)和____ 性(填“氧化”或“还原”)。
(2)Cu(NO3)2的电离方程式为____ 。
(3)在离子方程式中,单质、氧化物、水、气体、难溶物等不写成离子形式,该反应的离子方程式为____ 。
(4)随着反应的进行,硝酸的浓度减小,发生3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O反应。在该反应中,有3个Cu原子反应,有____ 个NO 转化为气体。
转化为气体。
(5)氮的氧化物有毒。用等量的铜制备Cu(NO3)2,有三种方法:
方法一:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
方法二:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
方法三:2Cu+O2+4HNO3 2Cu(NO3)2+2H2O
2Cu(NO3)2+2H2O
请从经济效益(硝酸根都进入硝酸铜)和社会效益(无有毒气体排放)考虑,最优方法是____ 。
(1)在这个反应中,浓硝酸表现的化学性质是
(2)Cu(NO3)2的电离方程式为
(3)在离子方程式中,单质、氧化物、水、气体、难溶物等不写成离子形式,该反应的离子方程式为
(4)随着反应的进行,硝酸的浓度减小,发生3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O反应。在该反应中,有3个Cu原子反应,有
 转化为气体。
转化为气体。(5)氮的氧化物有毒。用等量的铜制备Cu(NO3)2,有三种方法:
方法一:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
方法二:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
方法三:2Cu+O2+4HNO3
 2Cu(NO3)2+2H2O
2Cu(NO3)2+2H2O请从经济效益(硝酸根都进入硝酸铜)和社会效益(无有毒气体排放)考虑,最优方法是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
I.氯气常用于自来水的杀菌消毒,但用氯气对自来水消毒易产生致癌物质,二氧化氯是一种更为高效安全的消毒剂。
工业上制备 的反应为:
的反应为: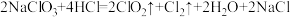 。
。
(1)该反应中的还原产物是___________ (写化学式),反应中每生成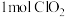 分子,转移电子的数目为
分子,转移电子的数目为___________ 。
(2) 在杀菌消毒后转化为
在杀菌消毒后转化为 ,可能会生成副产物亚氯酸盐(
,可能会生成副产物亚氯酸盐( ),需要将其转化为
),需要将其转化为 除去,下列试剂能实现其转化过程的是
除去,下列试剂能实现其转化过程的是________ (填序号)。
A. B.
B. C.
C.
(3)含氰废水中的 有剧毒。在碱性环境下
有剧毒。在碱性环境下 能被
能被 氧化成
氧化成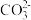 和
和 ,该反应氧化产物与还原产物物质的量之比为
,该反应氧化产物与还原产物物质的量之比为___________ 。
Ⅱ.高铁酸钾( )是一种新型绿色消毒剂,其在消毒后可形成胶体,可用于处理饮用水。
)是一种新型绿色消毒剂,其在消毒后可形成胶体,可用于处理饮用水。
(4) 胶体具有良好的净水效果,其分散质微粒大小范围为
胶体具有良好的净水效果,其分散质微粒大小范围为___________ ,其净水原理是胶体粒子具有___________ 性。
(5)工业上有干法与湿法两种制备高铁酸钾( )的方法。
)的方法。
①干法制备高铁酸钾时,一般先制备得到 ,当制
,当制 发生如下反应:
发生如下反应: ,该反应每生成
,该反应每生成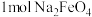 转移
转移___________  电子。
电子。
②湿法制备高铁酸钾的反应体系中主要有以下几种微粒: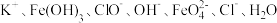 ,写出并配平湿法制高铁酸钾的离子反应方程式
,写出并配平湿法制高铁酸钾的离子反应方程式___________ 。
I.氯气常用于自来水的杀菌消毒,但用氯气对自来水消毒易产生致癌物质,二氧化氯是一种更为高效安全的消毒剂。
工业上制备
 的反应为:
的反应为: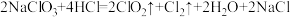 。
。(1)该反应中的还原产物是
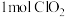 分子,转移电子的数目为
分子,转移电子的数目为(2)
 在杀菌消毒后转化为
在杀菌消毒后转化为 ,可能会生成副产物亚氯酸盐(
,可能会生成副产物亚氯酸盐( ),需要将其转化为
),需要将其转化为 除去,下列试剂能实现其转化过程的是
除去,下列试剂能实现其转化过程的是A.
 B.
B. C.
C.
(3)含氰废水中的
 有剧毒。在碱性环境下
有剧毒。在碱性环境下 能被
能被 氧化成
氧化成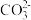 和
和 ,该反应氧化产物与还原产物物质的量之比为
,该反应氧化产物与还原产物物质的量之比为Ⅱ.高铁酸钾(
 )是一种新型绿色消毒剂,其在消毒后可形成胶体,可用于处理饮用水。
)是一种新型绿色消毒剂,其在消毒后可形成胶体,可用于处理饮用水。(4)
 胶体具有良好的净水效果,其分散质微粒大小范围为
胶体具有良好的净水效果,其分散质微粒大小范围为(5)工业上有干法与湿法两种制备高铁酸钾(
 )的方法。
)的方法。①干法制备高铁酸钾时,一般先制备得到
 ,当制
,当制 发生如下反应:
发生如下反应: ,该反应每生成
,该反应每生成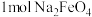 转移
转移 电子。
电子。②湿法制备高铁酸钾的反应体系中主要有以下几种微粒:
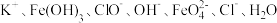 ,写出并配平湿法制高铁酸钾的离子反应方程式
,写出并配平湿法制高铁酸钾的离子反应方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】化学反应按照不同的分类方法,可以分为四大基本反应类型,离子反应和非离子反应,氧化还原反应和非氧化还原反应等。回答下列问题:
①2Na2O2+2CO2=2Na2CO3+O2 ②2Mg+CO2 2MgO+C
2MgO+C
③AlCl3+4NaOH=NaAlO2+3NaCl+2H2O ④Cl2+2KI=2KCl+I2
(1)上述反应中的单质被氧化的是___________ (填序号,下同)。
(2)上述反应中无电子转移的是___________ 。
(3)上述反应中,属于氧化还原反应且不属于四大基本反应类型的是___________ 。
(4)写出一个满足下列条件的化学方程式,并用单线桥标出电子转移的方向和数目___________ 。
①是分解反应 ②是氧化还原反应 ③产物中有单质
①2Na2O2+2CO2=2Na2CO3+O2 ②2Mg+CO2
 2MgO+C
2MgO+C③AlCl3+4NaOH=NaAlO2+3NaCl+2H2O ④Cl2+2KI=2KCl+I2
(1)上述反应中的单质被氧化的是
(2)上述反应中无电子转移的是
(3)上述反应中,属于氧化还原反应且不属于四大基本反应类型的是
(4)写出一个满足下列条件的化学方程式,并用单线桥标出电子转移的方向和数目
①是分解反应 ②是氧化还原反应 ③产物中有单质
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】回答下列问题:
Ⅰ.双氧水和84消毒液是生活中常用的两种消毒剂。
(1)某同学设计如下实验研究 的性质,请补全实验现象b.
的性质,请补全实验现象b._______ ,根据实验2现象写出该反应的离子方程式_______ 。
(2)某届奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是NaClO与 反应产生促进藻类快速生长。该反应说明氧化性:NaClO
反应产生促进藻类快速生长。该反应说明氧化性:NaClO_______  (填“>”或“<”);当有0.2mol
(填“>”或“<”);当有0.2mol 生成时,转移电子的物质的量为
生成时,转移电子的物质的量为_______ mol。
Ⅱ.亚硝酸钠( )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:
_______ _______
_______ _______=_______
_______=_______ _______
_______ _______
_______ _______
_______ _______
_______
(3)请完成该化学方程式并配平。_______
(4)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目_______ 。
Ⅰ.双氧水和84消毒液是生活中常用的两种消毒剂。
(1)某同学设计如下实验研究
 的性质,请补全实验现象b.
的性质,请补全实验现象b.| 序号 | 实验 | 实验现象 |
| 1 | 向5% 溶液中滴加酸性 溶液中滴加酸性 溶液 溶液 | a.溶液紫色褪去; b._______ |
| 2 | 向含5% 的酸性溶液中滴加淀粉碘化钾溶液 的酸性溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
(2)某届奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是NaClO与
 反应产生促进藻类快速生长。该反应说明氧化性:NaClO
反应产生促进藻类快速生长。该反应说明氧化性:NaClO (填“>”或“<”);当有0.2mol
(填“>”或“<”);当有0.2mol 生成时,转移电子的物质的量为
生成时,转移电子的物质的量为Ⅱ.亚硝酸钠(
 )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:_______
 _______
_______ _______=_______
_______=_______ _______
_______ _______
_______ _______
_______ _______
_______
(3)请完成该化学方程式并配平。
(4)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目
您最近一年使用:0次

 2FeCl3。
2FeCl3。 。
。 的质量之比为
的质量之比为 (标准状况)
(标准状况)

