根据所学知识回答问题:
(1)某无色澄清溶液的溶质可能由下列离子中的几种组成:Cl−、 、
、 、Cu2+、H+、Ca2+、Na+,某同学进行了如下实验:
、Cu2+、H+、Ca2+、Na+,某同学进行了如下实验:
Ⅰ.向溶液中加入过量的BaCl2溶液,有白色沉淀产生,过滤;
Ⅱ.向Ⅰ中滤液中加入AgNO3溶液,有白色沉淀产生;
Ⅲ.将Ⅰ中的沉淀加入稀盐酸中,沉淀部分消失,有气体产生。
依据以上实验可以推断,原溶液中一定含有___________ (用离子符号表示,下同);一定没有___________ 。
(2)下列微粒:①S ② ③Fe2+④Al3+⑤Na ⑥HCl ⑦Na2O2在化学反应中只能被氧化的是
③Fe2+④Al3+⑤Na ⑥HCl ⑦Na2O2在化学反应中只能被氧化的是___________ (填序号),只能表现出氧化性的是___________ (填序号)。
(元素常见的化合价: Fe:0,+2,+3 ;S:-2,0,+4,+6 H:0,+1;Al:0,+3;Cl:-1,0 +5,+7)
(3)某化学兴趣小组用食品脱氧剂(2g 铁粉、0.5g 活性炭、0.5g 氯化钠)进行如下两个实验。
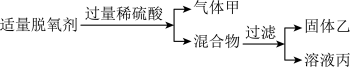
将乙烘干后进行如下实验,物质之间的转化关系如图(部分产物略去)
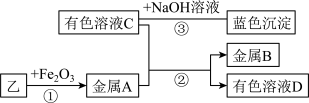
请回答:
①写出反应②的离子方程式为:___________ ;
②向溶液C 中加入BaCl2溶液,有白色沉淀产生,其化学反应方程式为:___________ 。
(1)某无色澄清溶液的溶质可能由下列离子中的几种组成:Cl−、
 、
、 、Cu2+、H+、Ca2+、Na+,某同学进行了如下实验:
、Cu2+、H+、Ca2+、Na+,某同学进行了如下实验:Ⅰ.向溶液中加入过量的BaCl2溶液,有白色沉淀产生,过滤;
Ⅱ.向Ⅰ中滤液中加入AgNO3溶液,有白色沉淀产生;
Ⅲ.将Ⅰ中的沉淀加入稀盐酸中,沉淀部分消失,有气体产生。
依据以上实验可以推断,原溶液中一定含有
(2)下列微粒:①S ②
 ③Fe2+④Al3+⑤Na ⑥HCl ⑦Na2O2在化学反应中只能被氧化的是
③Fe2+④Al3+⑤Na ⑥HCl ⑦Na2O2在化学反应中只能被氧化的是(元素常见的化合价: Fe:0,+2,+3 ;S:-2,0,+4,+6 H:0,+1;Al:0,+3;Cl:-1,0 +5,+7)
(3)某化学兴趣小组用食品脱氧剂(2g 铁粉、0.5g 活性炭、0.5g 氯化钠)进行如下两个实验。

将乙烘干后进行如下实验,物质之间的转化关系如图(部分产物略去)

请回答:
①写出反应②的离子方程式为:
②向溶液C 中加入BaCl2溶液,有白色沉淀产生,其化学反应方程式为:
更新时间:2022-12-05 16:34:04
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】I.已知:甲、乙、丙、丁为常见化合物,A、B为单质,相互转化关系如图。其中甲是天然气的主要成分。回答下列问题:
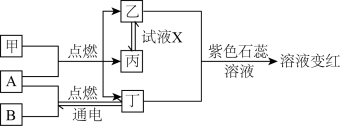
(1)丁物质的名称:_______ ;
(2)检验化合物乙的化学方程式_______ ;
(3)试剂X可能的化学式_______ 、_______ (要求:所选物质类别不同);
II.海水晒制粗盐的主要成分为 , 还含有少量的
, 还含有少量的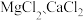 、
、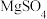 、泥沙等杂质。下面是由粗盐获取较纯净精盐的一种方法:
、泥沙等杂质。下面是由粗盐获取较纯净精盐的一种方法:
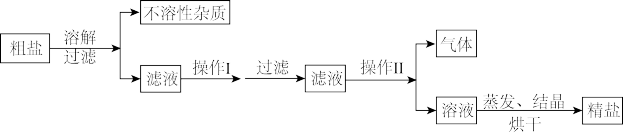
请分析上面流程图示,回答:
(4)为除去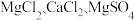 可溶性杂质, 操作 I 中依次加入的物质 (过量) 和顺序, 合理的是_______;
可溶性杂质, 操作 I 中依次加入的物质 (过量) 和顺序, 合理的是_______;
(5)操作I过量加入各物质的目的是_______ ;
(6)为获取较纯净精盐,操作II的具体方法是_______ 。

(1)丁物质的名称:
(2)检验化合物乙的化学方程式
(3)试剂X可能的化学式
II.海水晒制粗盐的主要成分为
 , 还含有少量的
, 还含有少量的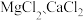 、
、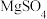 、泥沙等杂质。下面是由粗盐获取较纯净精盐的一种方法:
、泥沙等杂质。下面是由粗盐获取较纯净精盐的一种方法:
请分析上面流程图示,回答:
(4)为除去
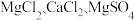 可溶性杂质, 操作 I 中依次加入的物质 (过量) 和顺序, 合理的是_______;
可溶性杂质, 操作 I 中依次加入的物质 (过量) 和顺序, 合理的是_______;A. |
B. |
C.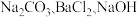 |
D.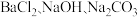 |
(6)为获取较纯净精盐,操作II的具体方法是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】构建知识网络是一种重要的学习方法。如图是初中化学常见的单质、氧化物、酸、碱、盐五种不同类别的物质与 的知识网络图,其中D为红棕色固体,C的溶液具有挥发性,盐为钠盐。图中“一”表示反应关系,“→”表示转化关系,请回答下列问题:
的知识网络图,其中D为红棕色固体,C的溶液具有挥发性,盐为钠盐。图中“一”表示反应关系,“→”表示转化关系,请回答下列问题:
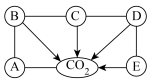
(1)A属于上述五种类别中的_______ 。
(2)D和E反应的化学方程式为_______ 。
(3)图中的反应没有涉及的基本反应类型是_______ 。
 的知识网络图,其中D为红棕色固体,C的溶液具有挥发性,盐为钠盐。图中“一”表示反应关系,“→”表示转化关系,请回答下列问题:
的知识网络图,其中D为红棕色固体,C的溶液具有挥发性,盐为钠盐。图中“一”表示反应关系,“→”表示转化关系,请回答下列问题:
(1)A属于上述五种类别中的
(2)D和E反应的化学方程式为
(3)图中的反应没有涉及的基本反应类型是
您最近一年使用:0次
【推荐3】Ⅰ.某化学小组为探究离子反应发生的条件,依次向水槽中加入下列物质,并记录灯泡的变化:
①硫酸铁粉末:灯泡不亮;
②加入蒸馏水:灯泡变亮;
③逐滴滴加氢氧化钡稀溶液:灯泡变化为亮→暗→熄灭→亮。
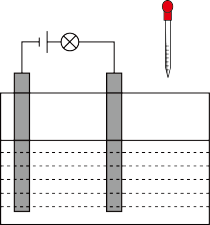
(1)硫酸铁溶液和氢氧化钡稀溶液发生_______ (填标号)。
A.氧化还原反应 B.复分解反应 C.置换反应
(2)加入蒸馏水后,灯泡变亮的原因是_______ (用电离方程式表示)。
(3)加入氢氧化钡稀溶液的过程中,灯泡由熄灭变亮的原因是_______ 。
Ⅱ.探究碳酸钠的性质:
(4)向一定量的碳酸钠固体中加入少许水,迅速用温度计测量其温度,发现温度计读数_______ (填“上升”“下降”或“不变”),当碳酸钠固体完全溶解后,依次加入几滴酚酞溶液、过量的稀盐酸。溶液颜色由红色最终变为无色,用离子方程式表示其变化的原因_______ 。
Ⅲ.离子反应在工农业生产和日常生活中有着广泛的应用:
(5)工业上得到的粗盐中往往含有 、
、 ,要除去这两种离子,需要加入试剂的化学式依次为NaOH、
,要除去这两种离子,需要加入试剂的化学式依次为NaOH、_______ 、_______ ,过滤,再加入适量的盐酸调节溶液呈中性,通过加热蒸发得到氯化钠固体。
①硫酸铁粉末:灯泡不亮;
②加入蒸馏水:灯泡变亮;
③逐滴滴加氢氧化钡稀溶液:灯泡变化为亮→暗→熄灭→亮。

(1)硫酸铁溶液和氢氧化钡稀溶液发生
A.氧化还原反应 B.复分解反应 C.置换反应
(2)加入蒸馏水后,灯泡变亮的原因是
(3)加入氢氧化钡稀溶液的过程中,灯泡由熄灭变亮的原因是
Ⅱ.探究碳酸钠的性质:
(4)向一定量的碳酸钠固体中加入少许水,迅速用温度计测量其温度,发现温度计读数
Ⅲ.离子反应在工农业生产和日常生活中有着广泛的应用:
(5)工业上得到的粗盐中往往含有
 、
、 ,要除去这两种离子,需要加入试剂的化学式依次为NaOH、
,要除去这两种离子,需要加入试剂的化学式依次为NaOH、
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】有一包不纯的固体烧碱,其中可能含有Na2SO4、MgSO4、Ba(OH)2、NaCl中的一种或几种,取少量烧碱样品,按下图所示步进行实验:
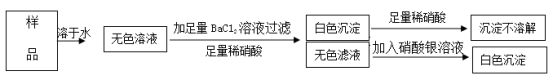
由此可推知该固体烧碱中一定含有__________ ;一定不含有______________ 。

由此可推知该固体烧碱中一定含有
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】检验 的正确操作
的正确操作
 的正确操作
的正确操作| 实验操作 | 实验现象 | 离子方程式 |
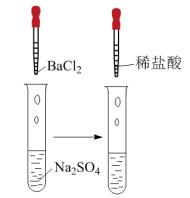 | 加入BaCl2生成 | |
 | 加入BaCl2生成 |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】某溶液,只含以下离子中的若干种:K+、Cu2+、Ba2+、Cl-、NO 、SO
、SO ,现取三份100mL溶液分别进行如下实验:
,现取三份100mL溶液分别进行如下实验:
①第一份加入硝酸钡溶液无明显现象,再加入AgNO3溶液有沉淀产生
②第二份加足量NaOH溶液后,有蓝色沉淀产生
③第三份加足量Na2SO4溶液后,有白色沉淀产生,加盐酸,沉淀质量不变
根据以上实验,回答下列问题:
(1)溶液中不能确定是否存在的离子是___ ,一定存在的离子是___ 。
(2)溶液中不存在的离子是___ ,实验②发生反应的离子方程式为___ 。
(3)写出第三份溶液中生成白色沉淀的离子方程式:___ 。
 、SO
、SO ,现取三份100mL溶液分别进行如下实验:
,现取三份100mL溶液分别进行如下实验:①第一份加入硝酸钡溶液无明显现象,再加入AgNO3溶液有沉淀产生
②第二份加足量NaOH溶液后,有蓝色沉淀产生
③第三份加足量Na2SO4溶液后,有白色沉淀产生,加盐酸,沉淀质量不变
根据以上实验,回答下列问题:
(1)溶液中不能确定是否存在的离子是
(2)溶液中不存在的离子是
(3)写出第三份溶液中生成白色沉淀的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】溴元素被称为海洋元素,它主要以溴离子形式存在于海水中。工业上制备粗溴( )的流程如图:
)的流程如图:

已知:①在酸性条件下, 具有强氧化性;②
具有强氧化性;② 。回答下列问题:
。回答下列问题:
(1)“置换”时通入 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(2)单质溴可用热空气吹出,其原因是___________ 。
(3)写出“酸化”时发生反应的化学方程式:___________ 。
(4)用 溶液而不用盐酸“酸化”的原因可能是
溶液而不用盐酸“酸化”的原因可能是___________ 。
(5)为了除去粗溴中微量的氯气,可向粗溴中加入适量___________ (填字母),充分反应后,分液。
a.饱和NaCl溶液 b.NaOH溶液 c. 溶液 d.
溶液 d. 溶液
溶液
 )的流程如图:
)的流程如图:
已知:①在酸性条件下,
 具有强氧化性;②
具有强氧化性;② 。回答下列问题:
。回答下列问题:(1)“置换”时通入
 发生反应的离子方程式为
发生反应的离子方程式为(2)单质溴可用热空气吹出,其原因是
(3)写出“酸化”时发生反应的化学方程式:
(4)用
 溶液而不用盐酸“酸化”的原因可能是
溶液而不用盐酸“酸化”的原因可能是(5)为了除去粗溴中微量的氯气,可向粗溴中加入适量
a.饱和NaCl溶液 b.NaOH溶液 c.
 溶液 d.
溶液 d. 溶液
溶液
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】亚氯酸钠( )主要用于棉纺,造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下
)主要用于棉纺,造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下 )受热易分解;
)受热易分解;
②高浓度的 易爆炸。
易爆炸。
(1) 与
与 ,因有强氧化性而用作常用消毒剂,消毒时均被还原为
,因有强氧化性而用作常用消毒剂,消毒时均被还原为 ,则
,则 的消毒能力是等质量的
的消毒能力是等质量的 的
的_____ 倍(保留小数点后一位)。
(2)反应1涉及的反应方程式为: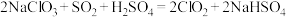 反应中生成的氧化产物与还原产物的个数比为
反应中生成的氧化产物与还原产物的个数比为_____ ;“反应1”需要鼓入空气,空气的作用是_____ 。
(3)“反应2”发生反应的化学方程式:_____ 。“反应2”需要控制反应温度不能过高,温度过高可能导致_____ ;_____ 。
(4)从“母液”中可回收的主要物质是_____ 。
(5)为探究 的氧化性,可以选择下列试剂
的氧化性,可以选择下列试剂_____ 。根据选择的试剂,描述能体现 氧化性的实验现象是
氧化性的实验现象是_____ 。
A.淀粉 溶液 B.酸性高锰酸钾溶液 C.氯水 D.
溶液 B.酸性高锰酸钾溶液 C.氯水 D. 溶液
溶液
(6)针对不同物品的消毒,亚氯酸钠溶液需要稀释到不同的浓度来使用。取含亚氯酸钠18.1g/L的消毒液lmL,加水稀释至100mL,则稀释后的溶液中亚氯酸钠的物质的量浓度为_____  。
。
 )主要用于棉纺,造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下
)主要用于棉纺,造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下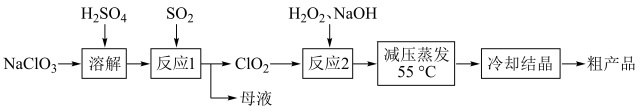
 )受热易分解;
)受热易分解;②高浓度的
 易爆炸。
易爆炸。(1)
 与
与 ,因有强氧化性而用作常用消毒剂,消毒时均被还原为
,因有强氧化性而用作常用消毒剂,消毒时均被还原为 ,则
,则 的消毒能力是等质量的
的消毒能力是等质量的 的
的(2)反应1涉及的反应方程式为:
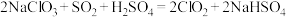 反应中生成的氧化产物与还原产物的个数比为
反应中生成的氧化产物与还原产物的个数比为(3)“反应2”发生反应的化学方程式:
(4)从“母液”中可回收的主要物质是
(5)为探究
 的氧化性,可以选择下列试剂
的氧化性,可以选择下列试剂 氧化性的实验现象是
氧化性的实验现象是A.淀粉
 溶液 B.酸性高锰酸钾溶液 C.氯水 D.
溶液 B.酸性高锰酸钾溶液 C.氯水 D. 溶液
溶液(6)针对不同物品的消毒,亚氯酸钠溶液需要稀释到不同的浓度来使用。取含亚氯酸钠18.1g/L的消毒液lmL,加水稀释至100mL,则稀释后的溶液中亚氯酸钠的物质的量浓度为
 。
。
您最近一年使用:0次
【推荐3】“大象牙膏”是一种神奇的化学反应,它会喷出大量的泡沫,就像是普通牙膏一样,人们给它取了一个大象牙膏的名字,大象牙膏( )的原理是双氧水+催化剂+发泡剂,混合时催化剂加快双氧水分解速率,分解出大量氧气。某小组同学欲探究
)的原理是双氧水+催化剂+发泡剂,混合时催化剂加快双氧水分解速率,分解出大量氧气。某小组同学欲探究 的性质,过程如下:
的性质,过程如下:
【预测】聚焦 中的
中的 作为核心元素,因此预测
作为核心元素,因此预测 既具有氧化性,也具有还原性。
既具有氧化性,也具有还原性。
(1)预测其具有氧化性的思路是___________ 。
【实验和观察】小组同学分别选用酸性 溶液、酸性
溶液、酸性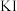 溶液与
溶液与 溶液反应以验证预测。已知:
溶液反应以验证预测。已知: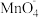 酸性条件下被还原成
酸性条件下被还原成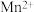 ,淀粉遇
,淀粉遇 变蓝色。
变蓝色。
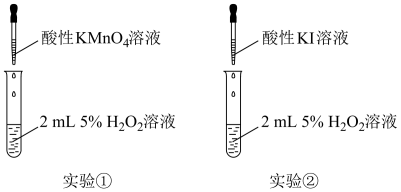
(2)实验①利用了酸性高锰酸钾的___________ (填“氧化性”或“还原性”),该实验中,证明酸性 溶液与
溶液与 溶液反应的现象除了溶液颜色变浅或褪色外还有
溶液反应的现象除了溶液颜色变浅或褪色外还有___________ 。写出该反应的离子方程式___________ 。
(3)实验②是为了验证 的
的___________ (填“氧化性”或“还原性”),在反应后的溶液中加入淀粉溶液,可观察到溶液变蓝,写出该反应的离子方程式___________ 。
【解释和结论】
(4)以上实验可得出的结论是___________ 。
 )的原理是双氧水+催化剂+发泡剂,混合时催化剂加快双氧水分解速率,分解出大量氧气。某小组同学欲探究
)的原理是双氧水+催化剂+发泡剂,混合时催化剂加快双氧水分解速率,分解出大量氧气。某小组同学欲探究 的性质,过程如下:
的性质,过程如下:【预测】聚焦
 中的
中的 作为核心元素,因此预测
作为核心元素,因此预测 既具有氧化性,也具有还原性。
既具有氧化性,也具有还原性。(1)预测其具有氧化性的思路是
【实验和观察】小组同学分别选用酸性
 溶液、酸性
溶液、酸性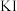 溶液与
溶液与 溶液反应以验证预测。已知:
溶液反应以验证预测。已知: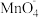 酸性条件下被还原成
酸性条件下被还原成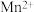 ,淀粉遇
,淀粉遇 变蓝色。
变蓝色。
(2)实验①利用了酸性高锰酸钾的
 溶液与
溶液与 溶液反应的现象除了溶液颜色变浅或褪色外还有
溶液反应的现象除了溶液颜色变浅或褪色外还有(3)实验②是为了验证
 的
的【解释和结论】
(4)以上实验可得出的结论是
您最近一年使用:0次



