据报道,某些花岗岩会释放氡 ,对人体造成伤害。
,对人体造成伤害。
(1)氡原子的核外电子数是___________ ,中子数是___________ 。
(2)请将Rn的原子结构示意图补全___________ 。
(3)请根据Rn的原子结构预测氡气的化学性质___________
(4)研究发现,镭能蜕变为 ,故将
,故将 称为镭射气;钍能蜕变为
称为镭射气;钍能蜕变为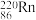 ,故将
,故将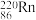 称为钍射气;锕能蜕变为
称为钍射气;锕能蜕变为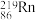 ,
,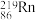 故将称为锕射气。
故将称为锕射气。 、
、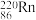 、
、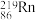
___________ 。
A.属于同种元素B.互为同位素C.属于同种核素D.属于同种原子
判断依据:___________ 决定元素种类,___________ 决定核素种类。
 ,对人体造成伤害。
,对人体造成伤害。(1)氡原子的核外电子数是
(2)请将Rn的原子结构示意图补全

(3)请根据Rn的原子结构预测氡气的化学性质___________
| A.非常活泼,容易与氧气等非金属单质反应 |
| B.比较活泼,能与钠等金属反应 |
| C.不太活泼,与氮气性质相似 |
| D.很难与其他物质发生反应 |
 ,故将
,故将 称为镭射气;钍能蜕变为
称为镭射气;钍能蜕变为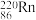 ,故将
,故将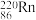 称为钍射气;锕能蜕变为
称为钍射气;锕能蜕变为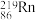 ,
,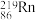 故将称为锕射气。
故将称为锕射气。 、
、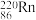 、
、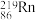
A.属于同种元素B.互为同位素C.属于同种核素D.属于同种原子
判断依据:
更新时间:2022-12-19 22:51:11
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】有A、B、C、X四种微粒。请根据已知信息,回答下列问题:
①当A微粒失去3个电子后,其电子层结构与氖原子相同;
②当B微粒得到1个电子后,其电子层结构与氩原子相同;
③C微粒带两个单位正电荷,核电荷数为12;
④X微粒不带电,原子核中只有一个质子,两个中子。
(1)写出以下微粒的化学符号:A___________ ,B___________ ,C___________ 。
(2)B微粒的结构示意图为___________ ,11g的X2O含有的中子数目为___________ 。(用NA表示阿伏伽德罗常数)
①当A微粒失去3个电子后,其电子层结构与氖原子相同;
②当B微粒得到1个电子后,其电子层结构与氩原子相同;
③C微粒带两个单位正电荷,核电荷数为12;
④X微粒不带电,原子核中只有一个质子,两个中子。
(1)写出以下微粒的化学符号:A
(2)B微粒的结构示意图为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】I.用序号按要求回答下列问题:
(1)下列各种物质:①H2O②NH3③KOH④Na2O2⑤MgCl2⑥Ne,不存在化学键的是________ ;只存在离子键的是________ ;含有非极性键的离子化合物的是________ 。
(2)下列变化过程:①碘的升华②NaCl固体溶于水③O2溶于水④HCl气体溶于水⑤烧碱熔化⑥氯化铵受热分解,化学键没有被破坏的是________ ;仅破坏离子键的是________ ;仅破坏共价键的是________ ,既破坏离子键,又破坏共价键的是________ 。
(3)Na2O2的电子式为________________________ ,用电子式表示H2O的形成过程:________________________________________________ 。
Ⅱ.有A、B、C、D、E五种微粒。已知:
①当A微粒失去3个电子后,其电子层结构与氖原子相同;
②当B微粒得到1个电子后,其电子层结构与氩原子相同;
③C微粒带两个单位正电荷,核电荷数为12;
④D微粒有18个电子,当失去2个电子后显电中性;
⑤E微粒不带电,原子核中只有一个质子。请回答:
(1)写出这五种微粒的符号:
A______ ,B______ ,C______ ,D______ ,E______ 。
(2)B微粒的结构示意图为____________ ,C微粒的结构示意图为____________ 。
(3)A的单质与EB溶液反应的离子方程式为______________________________________ 。
(1)下列各种物质:①H2O②NH3③KOH④Na2O2⑤MgCl2⑥Ne,不存在化学键的是
(2)下列变化过程:①碘的升华②NaCl固体溶于水③O2溶于水④HCl气体溶于水⑤烧碱熔化⑥氯化铵受热分解,化学键没有被破坏的是
(3)Na2O2的电子式为
Ⅱ.有A、B、C、D、E五种微粒。已知:
①当A微粒失去3个电子后,其电子层结构与氖原子相同;
②当B微粒得到1个电子后,其电子层结构与氩原子相同;
③C微粒带两个单位正电荷,核电荷数为12;
④D微粒有18个电子,当失去2个电子后显电中性;
⑤E微粒不带电,原子核中只有一个质子。请回答:
(1)写出这五种微粒的符号:
A
(2)B微粒的结构示意图为
(3)A的单质与EB溶液反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】原子序数为114号的稳定同位素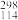 X预测。
X预测。
(1)114X元素位于元素周期表第________ 周期____ 族,为________ 元素(“金属”、“非金属”)。
(2)其最高价氧化物及其对应水化物的分子式分别是____ 、____ (用含X的式子表示),并估计后者为_______ 性(酸碱、两性)。
(3)它与氯生成化合物的分子式________ 、________ (用含X的式子表示)。
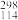 X预测。
X预测。(1)114X元素位于元素周期表第
(2)其最高价氧化物及其对应水化物的分子式分别是
(3)它与氯生成化合物的分子式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】3316S2-中的质子数是________ ,中子数是________ ,核外电子数是________ ,质量数是________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】亚铁氰化钾(K4[Fe(CN)6])双称黄血盐,是一种重要的化工原料。检验三价铁发生的反应为:K4[Fe(CN)6]+FeCl3=KFe[Fe(CN)6]↓(滕氏蓝)+3KCl,回答问题:
(1)写出基态Fe3+的核外电子排布式_______ 。
(2)黄血盐中C、N、O的第一电离能由大到小的排序为_______ ,电负性由大到小的排序为_______ 。
(1)写出基态Fe3+的核外电子排布式
(2)黄血盐中C、N、O的第一电离能由大到小的排序为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】安全气囊在汽车部件中非常重要,它的工作原理是汽车碰撞时传感器产生的电流触发气体发生如下反应:
2NaN3(s)=3N2(g)+2Na(s)
6Na(s)+Fe2O3(s)=3Na2O(s)+2Fe(s)
Na2O(s)+2CO2(g)+H2O(g)=2NaHCO3(s)
(1)上述反应所涉及元素中,某元素原子失去一个电子即可形成8电子稳定结构,该元素原子结构示意图为___________ ;某元素的最外层电子数是电子层数的3倍,则其简单离子的电子式为___________ ,能量最高的电子为___________ 层上的电子。反应中涉及的主族元素的简单离子半径从大到小的顺序是___________ (用离子符号表示)。
(2)氮的最高价氧化物对应的水化物与其氢化物反应生成一种盐,该盐晶体中含有的化学键类型是___________ ,其水溶液显___________ 性(填“酸”、“碱”或“中”),原因是___________ (用离子方程式表示)。
(3)汽车行驶过程中,能保护司机不受伤害的气囊需要0.065m3N2(S.T.P),其中约含有___________ 个氮原子(保留三个有效数字);已知获得上述N2需要NaN3130g,反应生成N2的产率是___________ %(产率= ×100%)
×100%)
2NaN3(s)=3N2(g)+2Na(s)
6Na(s)+Fe2O3(s)=3Na2O(s)+2Fe(s)
Na2O(s)+2CO2(g)+H2O(g)=2NaHCO3(s)
(1)上述反应所涉及元素中,某元素原子失去一个电子即可形成8电子稳定结构,该元素原子结构示意图为
(2)氮的最高价氧化物对应的水化物与其氢化物反应生成一种盐,该盐晶体中含有的化学键类型是
(3)汽车行驶过程中,能保护司机不受伤害的气囊需要0.065m3N2(S.T.P),其中约含有
 ×100%)
×100%)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】在氢、氮、氯和钠四种元素中:
(1)四种元素中最外层电子数最多的原子的结构示意图为___________________ 。
(2)由2种元素组成的共价化合物的水溶液显酸性,这种化合物的电子式是___ ;
(3)由两种元素组成的共价化合物的水溶液呈碱性,这种化合物的结构式为____________ ;
(4)四种元素对应的化学性质最稳定的单质的电子式为_____________________ 。
(5)由两种元素组成的离子化合物,其化学式为_____________ ;
(6)由三种元素组成的离子化合物,用电子式表示其形成过程_______________ 。
(7)与氯同属卤族元素的各元素的氢化物中稳定性最好的是_________________ ,其稳定的原因是__________________________________________ 。
(1)四种元素中最外层电子数最多的原子的结构示意图为
(2)由2种元素组成的共价化合物的水溶液显酸性,这种化合物的电子式是
(3)由两种元素组成的共价化合物的水溶液呈碱性,这种化合物的结构式为
(4)四种元素对应的化学性质最稳定的单质的电子式为
(5)由两种元素组成的离子化合物,其化学式为
(6)由三种元素组成的离子化合物,用电子式表示其形成过程
(7)与氯同属卤族元素的各元素的氢化物中稳定性最好的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】人们运用元素周期律和元素周期表,可以系统研究元素的性质。试回答:
(1)碱金属元素中,锂原子的结构示意图为_______ ,其中6Li、7Li互为_______ ;
(2)金属钾19K位于元素周期表中的第_______ 周期第_______ 族,钾的氧化物有多种,其中过氧化钾(K2O2)和超氧化钾(KO2)常作供氧剂,写出过氧化钾与CO2反应的化学方程式:_______ ;
(3)第三周期元素中,酸性最强的HClO4中氯元素的化合价为_______ 、可作半导体材料的元素是_______ (填名称),已知H2+Cl2 2HCl,请用电子式表达HCl的形成过程
2HCl,请用电子式表达HCl的形成过程_______ 。
(1)碱金属元素中,锂原子的结构示意图为
(2)金属钾19K位于元素周期表中的第
(3)第三周期元素中,酸性最强的HClO4中氯元素的化合价为
 2HCl,请用电子式表达HCl的形成过程
2HCl,请用电子式表达HCl的形成过程
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】按要求回答下列问题:
(1)以下六组物质中,互为同位素的是___________ ,互为同素异形体的是___________ (填序号).
①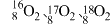 ②H、D、T ③
②H、D、T ③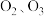 ④白磷和红磷 ⑤液氯和氯气 ⑥
④白磷和红磷 ⑤液氯和氯气 ⑥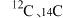
(2)在① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ 中,属于共价化合物的是
中,属于共价化合物的是___________ (填序号,下同),既存在共价键又存在离子键的是___________ ,溶于水存在共价键的断裂和形成的是___________ .
(3)请各写出相应的化学用语:含中子数为30,原子序数为26的铁元素的一种核素___________ ,含三个原子核的18电子的共价化合物化学式___________
(1)以下六组物质中,互为同位素的是
①
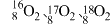 ②H、D、T ③
②H、D、T ③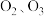 ④白磷和红磷 ⑤液氯和氯气 ⑥
④白磷和红磷 ⑤液氯和氯气 ⑥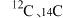
(2)在①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ 中,属于共价化合物的是
中,属于共价化合物的是(3)请各写出相应的化学用语:含中子数为30,原子序数为26的铁元素的一种核素
您最近一年使用:0次

 ,该元素符号为
,该元素符号为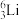 、
、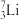 、
、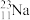 、
、 、
、 、
、 中
中

