安全气囊在汽车部件中非常重要,它的工作原理是汽车碰撞时传感器产生的电流触发气体发生如下反应:
2NaN3(s)=3N2(g)+2Na(s)
6Na(s)+Fe2O3(s)=3Na2O(s)+2Fe(s)
Na2O(s)+2CO2(g)+H2O(g)=2NaHCO3(s)
(1)上述反应所涉及元素中,某元素原子失去一个电子即可形成8电子稳定结构,该元素原子结构示意图为___________ ;某元素的最外层电子数是电子层数的3倍,则其简单离子的电子式为___________ ,能量最高的电子为___________ 层上的电子。反应中涉及的主族元素的简单离子半径从大到小的顺序是___________ (用离子符号表示)。
(2)氮的最高价氧化物对应的水化物与其氢化物反应生成一种盐,该盐晶体中含有的化学键类型是___________ ,其水溶液显___________ 性(填“酸”、“碱”或“中”),原因是___________ (用离子方程式表示)。
(3)汽车行驶过程中,能保护司机不受伤害的气囊需要0.065m3N2(S.T.P),其中约含有___________ 个氮原子(保留三个有效数字);已知获得上述N2需要NaN3130g,反应生成N2的产率是___________ %(产率= ×100%)
×100%)
2NaN3(s)=3N2(g)+2Na(s)
6Na(s)+Fe2O3(s)=3Na2O(s)+2Fe(s)
Na2O(s)+2CO2(g)+H2O(g)=2NaHCO3(s)
(1)上述反应所涉及元素中,某元素原子失去一个电子即可形成8电子稳定结构,该元素原子结构示意图为
(2)氮的最高价氧化物对应的水化物与其氢化物反应生成一种盐,该盐晶体中含有的化学键类型是
(3)汽车行驶过程中,能保护司机不受伤害的气囊需要0.065m3N2(S.T.P),其中约含有
 ×100%)
×100%)
更新时间:2024-01-23 22:24:13
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】现有14.4gCO和CO2的混合气体,在标准状况下所占的体积约为8.96L。回答下列问题:
(1)该混合气体的平均摩尔质量:___________ 。
(2)混合气体中碳原子的个数:___________ 。(用NA表示阿伏加德罗常数的值)
(3)将混合气体依次通过如图装置,最后收集在气球中。
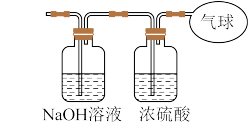
①气球中收集到的气体摩尔质量:___________ ;
②标准状况下气球中收集到的气体的体积为___________ ;
③气球中收集到的气体的电子总数___________ 。(用NA表示阿伏加德罗常数的值)
(1)该混合气体的平均摩尔质量:
(2)混合气体中碳原子的个数:
(3)将混合气体依次通过如图装置,最后收集在气球中。

①气球中收集到的气体摩尔质量:
②标准状况下气球中收集到的气体的体积为
③气球中收集到的气体的电子总数
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】400℃时,向一个容积为10L、盛有催化剂的密闭容器中,充入一定量的SO2和14mol O2,发生反应:2SO2(g)+O2(g)  2SO3(g)。2min后,测得容器中剩余2mol SO2和12mol O2.请分析计算(请写出计算过程):
2SO3(g)。2min后,测得容器中剩余2mol SO2和12mol O2.请分析计算(请写出计算过程):
(1)生成SO3的物质的量________ ;
(2)SO2的起始的物质的量浓度________ ;
(3)2min内,SO2和SO3的反应速率________ 。
 2SO3(g)。2min后,测得容器中剩余2mol SO2和12mol O2.请分析计算(请写出计算过程):
2SO3(g)。2min后,测得容器中剩余2mol SO2和12mol O2.请分析计算(请写出计算过程):(1)生成SO3的物质的量
(2)SO2的起始的物质的量浓度
(3)2min内,SO2和SO3的反应速率
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
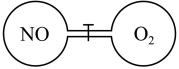
【推荐3】如图所示,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO和O2,且恰好使两容器内气体密度相同.打开活塞,使NO与O2充分反应(已知反应方程式为2NO+O2=2NO2 , 装置中不存在其它化学反应)。
(1)开始时左右两室分子数_____________ (填“相同”或“不相同”)。
(2)反应前后NO室压强_____________ (填“增大”或“减小”)。
(3)最终容器内密度与原来_____________ (填“相同”或“不相同”)。
(1)开始时左右两室分子数
(2)反应前后NO室压强
(3)最终容器内密度与原来
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】写出下列盐溶于水后发生水解反应的离子方程式。
(1)CH3COONa___________ 。
(2)NH4Cl___________ 。
(3)Na2CO3___________ 。
(4)Al2(SO4)3___________ 。
(1)CH3COONa
(2)NH4Cl
(3)Na2CO3
(4)Al2(SO4)3
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】盐类水解的方程式书写通式:弱酸阴离子+水⇌弱酸+OH-或弱碱阳离子+水⇌弱碱+H+
(1)一般情况下,盐类水解的程度较小,用可逆符号“⇌”连接,且一般不会产生沉淀和气体(双水解除外),故方程式中通常没有“↑”、“↓”符号。
(2)多元弱酸,其酸根离子的水解是分步进行的,水解反应必须分步表示,不能合并,以第一步为主,第二步很微弱。
(3)多元弱碱阳离子的水解也是分步进行的,但通常简化为一步表示。
(1)一般情况下,盐类水解的程度较小,用可逆符号“⇌”连接,且一般不会产生沉淀和气体(双水解除外),故方程式中通常没有“↑”、“↓”符号。
(2)多元弱酸,其酸根离子的水解是分步进行的,水解反应必须分步表示,不能合并,以第一步为主,第二步很微弱。
(3)多元弱碱阳离子的水解也是分步进行的,但通常简化为一步表示。
| 盐的类型 | 实例 | 水解的离子方程式 |
| 一元弱酸盐/弱碱盐 | NH4Cl | |
| CH3COONa | ||
| 多元弱酸盐 | Na2CO3 | |
| Na2S | ||
| 多元弱碱盐 | FeCl3 | |
| CuCl2 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】按照要求填空:
(1)在氨水中存在下列电离平衡:NH3·H2O
 +OH-,下列情况能引起电离平衡向正向移动的有
+OH-,下列情况能引起电离平衡向正向移动的有____________ ;
①加NH4Cl固体 ②加NaOH溶液 ③加CH3COOH溶液 ④加水
(2)常温下,pH=10的NaOH 溶液中,由水电离的OH-浓度为___________ mol/L;
(3)在室温下,0.1mol/L NH4Cl 溶液①呈_________ 性(填“酸”“碱”或“中”),其原因是______________________ (用离子方程式表示)
(4)在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
①当三种酸的物质的量浓度相同时,c(H+)由大到小的顺序是________ ;(用序号表示,下同)
②若三者c(H+)相同时,物质的量浓度由大到小的顺序是____________ 。
(1)在氨水中存在下列电离平衡:NH3·H2O

 +OH-,下列情况能引起电离平衡向正向移动的有
+OH-,下列情况能引起电离平衡向正向移动的有①加NH4Cl固体 ②加NaOH溶液 ③加CH3COOH溶液 ④加水
(2)常温下,pH=10的NaOH 溶液中,由水电离的OH-浓度为
(3)在室温下,0.1mol/L NH4Cl 溶液①呈
(4)在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
①当三种酸的物质的量浓度相同时,c(H+)由大到小的顺序是
②若三者c(H+)相同时,物质的量浓度由大到小的顺序是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】下表是部分元素周期表,序号代表某一元素请用化学用语回答下列问题。
(1)①~⑩中,最活泼的金属元素是______ (写元素符号);惰性元素名称是_____ ;⑦的气态氢化物化学式是______ 。
(2)①、④、⑤原子半径由大到小的顺序是______ 。
(3)⑧、⑨的气态氢化物,更稳定的是______ (填化学式);结构式为______ 。
(4)①~⑨的最高价氧化物的水化物中:酸性最强的是______ (填化学式);碱性最强的物质的电子式为______ ,它与⑥的最高价氧化物的水化物反应的离子方程式为__________________ 。
族 周期 | ⅠA | 0 | ||||||
1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
2 | ① | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)①、④、⑤原子半径由大到小的顺序是
(3)⑧、⑨的气态氢化物,更稳定的是
(4)①~⑨的最高价氧化物的水化物中:酸性最强的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】回答下列问题。
(1)26号元素价层电子排布式为___________ ;L原子核外电子占有9个轨道,而且有一个未成对电子,L是___________ 元素。
(2)硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物。
①基态硒原子的价层电子排布式为___________ 。
②锗、砷、硒三种元素的第一电离能由大到小排序为___________ 。(填元素符号)
(3)①Cu元素基态原子的价层电子排布式为___________ 。
②下列说法正确的是___________ (填字母)。
A.第一电离能:As>Ga B.电负性:As>Ga C.原子半径:As>Ga
③在第二周期中,第一电离能位于硼元素与氮元素之间的元素有___________ 种。
(1)26号元素价层电子排布式为
(2)硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物。
①基态硒原子的价层电子排布式为
②锗、砷、硒三种元素的第一电离能由大到小排序为
(3)①Cu元素基态原子的价层电子排布式为
②下列说法正确的是
A.第一电离能:As>Ga B.电负性:As>Ga C.原子半径:As>Ga
③在第二周期中,第一电离能位于硼元素与氮元素之间的元素有
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】写出有关的元素符号或名称
(1)某元素最外层电子数是次外层电子数的2倍,该元素符号是______ 。
(2)某元素K层与M层电子数相同,该元素名称是______ 。
(1)某元素最外层电子数是次外层电子数的2倍,该元素符号是
(2)某元素K层与M层电子数相同,该元素名称是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】最外层电子数目的变化
除第1周期外,每隔一定数目的元素,元素原子的最外层电子数重复出现从_____ 逐渐增加到_____ 的周期性变化。
除第1周期外,每隔一定数目的元素,元素原子的最外层电子数重复出现从
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】A、B、C、D、E代表5种元素。请填空:
(1)A 元素基态原子的最外层有2 个未成对电子,次外层有2 个电子,其元素符号为______ ;
(2) B 元素的负一价离子和C元素的正一价离子的电子层结构都与氖相同,B 的元素符号为______ , C的元素符号为______ 。
(3) D 元素的正二价离子的3d能级为半充满,D的元素符号为_____ ,其基态原子的电子排布式为______ ,它位于第________ 周期第______ 族;
(4) E 元素基态原子的M 层能量最高的能级半充满,N 层没有成对电子,只有一个未成对电子,E 的元素符号为_____________ , 其基态原子的电子排布式为_______________ 。
(1)A 元素基态原子的最外层有2 个未成对电子,次外层有2 个电子,其元素符号为
(2) B 元素的负一价离子和C元素的正一价离子的电子层结构都与氖相同,B 的元素符号为
(3) D 元素的正二价离子的3d能级为半充满,D的元素符号为
(4) E 元素基态原子的M 层能量最高的能级半充满,N 层没有成对电子,只有一个未成对电子,E 的元素符号为
您最近一年使用:0次



