按照要求填空:
(1)在氨水中存在下列电离平衡:NH3·H2O
 +OH-,下列情况能引起电离平衡向正向移动的有
+OH-,下列情况能引起电离平衡向正向移动的有____________ ;
①加NH4Cl固体 ②加NaOH溶液 ③加CH3COOH溶液 ④加水
(2)常温下,pH=10的NaOH 溶液中,由水电离的OH-浓度为___________ mol/L;
(3)在室温下,0.1mol/L NH4Cl 溶液①呈_________ 性(填“酸”“碱”或“中”),其原因是______________________ (用离子方程式表示)
(4)在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
①当三种酸的物质的量浓度相同时,c(H+)由大到小的顺序是________ ;(用序号表示,下同)
②若三者c(H+)相同时,物质的量浓度由大到小的顺序是____________ 。
(1)在氨水中存在下列电离平衡:NH3·H2O

 +OH-,下列情况能引起电离平衡向正向移动的有
+OH-,下列情况能引起电离平衡向正向移动的有①加NH4Cl固体 ②加NaOH溶液 ③加CH3COOH溶液 ④加水
(2)常温下,pH=10的NaOH 溶液中,由水电离的OH-浓度为
(3)在室温下,0.1mol/L NH4Cl 溶液①呈
(4)在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
①当三种酸的物质的量浓度相同时,c(H+)由大到小的顺序是
②若三者c(H+)相同时,物质的量浓度由大到小的顺序是
更新时间:2020-12-04 22:57:04
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】常压下,取不同浓度、不同温度的氨水进行各项内容的测定,得到下表实验数据。
(1)温度升高, 的电离平衡向
的电离平衡向________ (填“左”或“右”)移动,能支持该结论的表中数据是________ (填序号)。
a.电离常数 b.电离度 c. d.
d.
(2)表中 基本不变的原因是
基本不变的原因是________________ 。
(3)常温下,在氨水中加入一定量的氯化铵晶体,下列说法错误的是________ (填序号)。
A.溶液的 增大 B.氨水的电离度减小 C.
增大 B.氨水的电离度减小 C. 减小 D.
减小 D. 减小
减小
温度 | 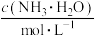 | 电离常数 | 电离度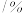 |  |
| 0 | 16.56 | 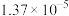 | 9.098 | 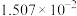 |
| 10 | 15.16 | 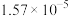 | 10.18 | 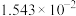 |
| 20 | 13.63 | 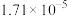 | 11.2 | 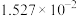 |
(1)温度升高,
 的电离平衡向
的电离平衡向a.电离常数 b.电离度 c.
 d.
d.
(2)表中
 基本不变的原因是
基本不变的原因是(3)常温下,在氨水中加入一定量的氯化铵晶体,下列说法错误的是
A.溶液的
 增大 B.氨水的电离度减小 C.
增大 B.氨水的电离度减小 C. 减小 D.
减小 D. 减小
减小
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】电离平衡常数(用 表示)的大小可以判断电解质的相对强弱。
表示)的大小可以判断电解质的相对强弱。
(1)水是极弱的电解质, 可表示水的电离程度,其表达式是
可表示水的电离程度,其表达式是_______ ,温度升高, 的值
的值_______ (填“变大”“变小”或“不变”)。
(2) 通常表示弱酸的电离平衡常数,
通常表示弱酸的电离平衡常数, 值越大表示该弱酸的酸性
值越大表示该弱酸的酸性_______ ,当用蒸馏水稀释 醋酸时,醋酸的
醋酸时,醋酸的
_______ (填“变大”“变小”或“不变”)。
(3)常温下, 的盐酸中由水电离出的
的盐酸中由水电离出的 浓度为
浓度为_______ , 的NaOH溶液中由水电离出的
的NaOH溶液中由水电离出的 浓度为
浓度为_______ 。
(4)常温下,4种酸的电离平衡常数如下:
①物质的量浓度相同的HF、 、
、 、HClO中,
、HClO中, 由大到小的顺序是
由大到小的顺序是_______ 。
② 、
、 、
、 、
、 、
、 结合
结合 的能力由大到小的顺序是
的能力由大到小的顺序是_______ 。
 表示)的大小可以判断电解质的相对强弱。
表示)的大小可以判断电解质的相对强弱。(1)水是极弱的电解质,
 可表示水的电离程度,其表达式是
可表示水的电离程度,其表达式是 的值
的值(2)
 通常表示弱酸的电离平衡常数,
通常表示弱酸的电离平衡常数, 值越大表示该弱酸的酸性
值越大表示该弱酸的酸性 醋酸时,醋酸的
醋酸时,醋酸的
(3)常温下,
 的盐酸中由水电离出的
的盐酸中由水电离出的 浓度为
浓度为 的NaOH溶液中由水电离出的
的NaOH溶液中由水电离出的 浓度为
浓度为(4)常温下,4种酸的电离平衡常数如下:
| 化学式 | HF |  |  | HClO |
| 电离平衡常数 | 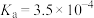 |  |   | 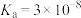 |
 、
、 、HClO中,
、HClO中, 由大到小的顺序是
由大到小的顺序是②
 、
、 、
、 、
、 、
、 结合
结合 的能力由大到小的顺序是
的能力由大到小的顺序是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】根据下列化合物:①NaCl、②NaOH、③HCl、④NH4Cl、⑤CH3COONa、⑥CH3COOH、⑦NH3·H2O、⑧H2O,回答下列问题。
(1)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=________ ,在pH=3的CH3COOH溶液中,水电离出来的c(H+)=________ 。
(2)已知纯水中存在如下平衡:H2O+H2O H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是
H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是________ (填字母序号)。
A.向水中加入NaHSO4固体 B.向水中加Na2CO3固体
C.加热至100℃ D.向水中加入(NH4)2SO4固体
(3)若将等pH、等体积的②NaOH和⑦NH3·H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH仍相等,则m________ n (填“<”、“>”或“=”)。
(4)除⑧H2O外,若其余7种溶液的物质的量浓度相同,则这7种溶液按pH由大到小的顺序为:_________________________________________________ ( 填序号)。
(1)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=
(2)已知纯水中存在如下平衡:H2O+H2O
 H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是
H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是A.向水中加入NaHSO4固体 B.向水中加Na2CO3固体
C.加热至100℃ D.向水中加入(NH4)2SO4固体
(3)若将等pH、等体积的②NaOH和⑦NH3·H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH仍相等,则m
(4)除⑧H2O外,若其余7种溶液的物质的量浓度相同,则这7种溶液按pH由大到小的顺序为:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】书写下列化学用语:
(1)实验室制取氯气的离子方程式____________ 。
(2)泡沫灭火器所用的原料为硫酸铝和碳酸氢钠,用离子方程式表示泡沫灭火器的灭火原理_______ 。
(3)向含有Mg(OH)2固体的浊液中加入浓NH4Cl溶液,Mg(OH)2固体溶解,用化学方程式解释原因_____________ 。
(4)以甲烷、空气为燃料,以KOH为电解质溶液的燃料电池,负极反应式________ ,正极反应式_________ 。
(1)实验室制取氯气的离子方程式
(2)泡沫灭火器所用的原料为硫酸铝和碳酸氢钠,用离子方程式表示泡沫灭火器的灭火原理
(3)向含有Mg(OH)2固体的浊液中加入浓NH4Cl溶液,Mg(OH)2固体溶解,用化学方程式解释原因
(4)以甲烷、空气为燃料,以KOH为电解质溶液的燃料电池,负极反应式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】写出下列物质在水溶液中的水解离子方程式及沉淀溶解平衡方程式:
(1)NaClO水解离子方程式___________________________
(2)NH4Cl水解离子方程式____________________________
(3)KAl(SO4)2·12H2O水解离子方程式__________________________
(4)CaCO3沉淀溶解平衡方程式__________________________
(5)Fe(OH)3沉淀溶解平衡方程式__________________________
(1)NaClO水解离子方程式
(2)NH4Cl水解离子方程式
(3)KAl(SO4)2·12H2O水解离子方程式
(4)CaCO3沉淀溶解平衡方程式
(5)Fe(OH)3沉淀溶解平衡方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】填空。
(1)HClO中Cl的化合价为___________ ,该分子的电子式为___________
(2)“84”消毒液的主要成分为NaClO,该溶液呈___________ (填“酸性”、“中性”或“碱性”),其主要原因:___________ (用离子方程说明)。
(1)HClO中Cl的化合价为
(2)“84”消毒液的主要成分为NaClO,该溶液呈
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】醋酸溶液与氨水溶液都是高中化学中常见的电解质溶液。
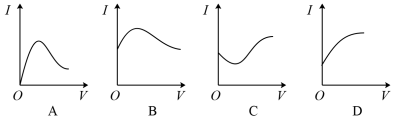
(1)向0.1mol/L的醋酸溶液中逐滴加入氨水至过量时,溶液的导电能力将发生相应的变化,其电流强(I)随加入氨水的体积(V)变化的曲线关系是图中的____ 。
(2)往醋酸钠溶液中滴加几滴酚酞试液,然后将溶液加热片刻,整个过程中可观察到__________ ,产生该现象的原因是_____________________________________________ (用必要的文字和离子方程式加以解释)。
(3)现有常温下浓度均为0.1mol/L的3种溶液:①HCl;②氨水;③NH4Cl。
a.上述三种溶液的pH值由小到大的顺序是___________________ (用编号表示)。
b.上述三种溶液中水的电离程度由大到小的顺序是____________ (用编号表示)。
c.将①②混合后,溶液中的c(NH )=c(Cl-),则盐酸的体积
)=c(Cl-),则盐酸的体积_______ 氨水的体积(填 “>”、“<”或“=”)。
(4)下列有关(NH4)2SO4溶液的说法正确的是____。
(1)向0.1mol/L的醋酸溶液中逐滴加入氨水至过量时,溶液的导电能力将发生相应的变化,其电流强(I)随加入氨水的体积(V)变化的曲线关系是图中的

(2)往醋酸钠溶液中滴加几滴酚酞试液,然后将溶液加热片刻,整个过程中可观察到
(3)现有常温下浓度均为0.1mol/L的3种溶液:①HCl;②氨水;③NH4Cl。
a.上述三种溶液的pH值由小到大的顺序是
b.上述三种溶液中水的电离程度由大到小的顺序是
c.将①②混合后,溶液中的c(NH
 )=c(Cl-),则盐酸的体积
)=c(Cl-),则盐酸的体积(4)下列有关(NH4)2SO4溶液的说法正确的是____。
A.电离方程式:(NH4)2SO4=2NH +SO +SO |
B.水解离子方程式:NH +H2O=NH3·H2O+H+ +H2O=NH3·H2O+H+ |
C.离子浓度关系:c(NH )+c(H+)=c(SO )+c(H+)=c(SO )+c(OH-) )+c(OH-) |
D.微粒浓度大小:c(NH )>c(SO )>c(SO )>c(H+)>c(NH3·H2O)>c(OH-) )>c(H+)>c(NH3·H2O)>c(OH-) |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】在日常生活和工农业生产中常用到盐的水解反应。
(1)实验室在保存FeCl3溶液时,常在溶液中加入___________ ,以抑制其水解;把AlCl3溶液蒸干并充分灼烧,最后得到的固体是___________ 。
(2)热的纯碱溶液去油污能力增强,请结合离子方程式和平衡移动原理进行解释___________ 。
(1)实验室在保存FeCl3溶液时,常在溶液中加入
(2)热的纯碱溶液去油污能力增强,请结合离子方程式和平衡移动原理进行解释
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】常温下,有0.1mol/L的四种溶液:①HCl②NH3•H2O③NaOH④Na2CO3
(1)用化学用语解释溶液①呈酸性的原因:_______ 。
(2)溶液③的pH=_______ 。
(3)溶液②、③分别与等量的溶液①恰好完全反应,消耗的体积:②________ ③(填“>”、“<”或“=”)。
(4)用广泛pH试纸测得④溶液的pH=11,用离子方程式解释Na2CO3溶液显碱性的原因:_______ 。溶液中由水电离出的c(OH−)为_______ 。
(5)常温下,下列关于溶液②的判断正确的是_______ 。
a.c( )=0.1mol/L
)=0.1mol/L
b.溶液中c(OH−)>c( )>c(H+)
)>c(H+)
c.加入NH4Cl(s),c(OH−)不变
d.滴入少量浓盐酸,溶液导电性增强
(1)用化学用语解释溶液①呈酸性的原因:
(2)溶液③的pH=
(3)溶液②、③分别与等量的溶液①恰好完全反应,消耗的体积:②
(4)用广泛pH试纸测得④溶液的pH=11,用离子方程式解释Na2CO3溶液显碱性的原因:
(5)常温下,下列关于溶液②的判断正确的是
a.c(
 )=0.1mol/L
)=0.1mol/Lb.溶液中c(OH−)>c(
 )>c(H+)
)>c(H+)c.加入NH4Cl(s),c(OH−)不变
d.滴入少量浓盐酸,溶液导电性增强
您最近一年使用:0次



