常压下,取不同浓度、不同温度的氨水进行各项内容的测定,得到下表实验数据。
(1)温度升高, 的电离平衡向
的电离平衡向________ (填“左”或“右”)移动,能支持该结论的表中数据是________ (填序号)。
a.电离常数 b.电离度 c. d.
d.
(2)表中 基本不变的原因是
基本不变的原因是________________ 。
(3)常温下,在氨水中加入一定量的氯化铵晶体,下列说法错误的是________ (填序号)。
A.溶液的 增大 B.氨水的电离度减小 C.
增大 B.氨水的电离度减小 C. 减小 D.
减小 D. 减小
减小
温度 | 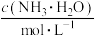 | 电离常数 | 电离度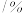 |  |
| 0 | 16.56 | 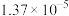 | 9.098 | 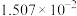 |
| 10 | 15.16 | 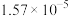 | 10.18 | 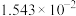 |
| 20 | 13.63 | 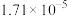 | 11.2 | 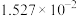 |
(1)温度升高,
 的电离平衡向
的电离平衡向a.电离常数 b.电离度 c.
 d.
d.
(2)表中
 基本不变的原因是
基本不变的原因是(3)常温下,在氨水中加入一定量的氯化铵晶体,下列说法错误的是
A.溶液的
 增大 B.氨水的电离度减小 C.
增大 B.氨水的电离度减小 C. 减小 D.
减小 D. 减小
减小
18-19高二·全国·课时练习 查看更多[4]
鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第2节 弱电解质的电离 盐类的水解 课时1 弱电解质的电离平衡人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第一节 电离平衡 作业帮(已下线)3.1 电离平衡-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)福建师范大学附属中学2021-2022学年高二上学期期中考试化学试题
更新时间:2020-09-14 10:09:40
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】水溶液中存在多种多样的化学反应和平衡,按要求完成下列填空。
(1)25℃时,有pH=3的盐酸和pH=10的Ba(OH)2溶液中由水电离出的c(H+)之比为_______
(2)在常温下,将pH=5的硫酸溶液与pH=12的氢氧化钠溶液等体积混合,所得溶液的pH=_______
(3)常温下,有pH相同、体积相同的醋酸和盐酸两种溶液,采取以下措施:
①加适量醋酸钠晶体后,醋酸溶液中c(H+)_______ (填“增大”“减小”或“不变”,下同),盐酸中c(H+)_______ 。
②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是_______ (填字母)。(①表示盐酸,②表示醋酸)

(4)已知:H2CO3:Ka1=4.3×10-7;Ka2=5.6×10-11,HCN:Ka= 4.9×10-10。
①你认为H2CO3的Ka1远大于Ka2的原因是:_______ 。
②则将CO2气体通入足量的NaCN溶液中的离子反应方程式为:_______
(1)25℃时,有pH=3的盐酸和pH=10的Ba(OH)2溶液中由水电离出的c(H+)之比为
(2)在常温下,将pH=5的硫酸溶液与pH=12的氢氧化钠溶液等体积混合,所得溶液的pH=
(3)常温下,有pH相同、体积相同的醋酸和盐酸两种溶液,采取以下措施:
①加适量醋酸钠晶体后,醋酸溶液中c(H+)
②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是

(4)已知:H2CO3:Ka1=4.3×10-7;Ka2=5.6×10-11,HCN:Ka= 4.9×10-10。
①你认为H2CO3的Ka1远大于Ka2的原因是:
②则将CO2气体通入足量的NaCN溶液中的离子反应方程式为:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】亚磷酸(H3PO3)是二元酸,与足量NaOH溶液反应生成Na2HPO3。
(1)PCl3水解可制取亚磷酸,化学方程式为__ 。
(2)H3PO3溶液中存在电离平衡:H3PO3 H2PO
H2PO +H+。
+H+。
①某温度下,0.10mol·L-1的H3PO3溶液pH=1.6,即溶液中c(H+)=2.5×10-2mol·L-1。该温度下上述电离平衡的平衡常数K=__ (H3PO3的第二步电离忽略不计,结果保留两位有效数字)。
②根据H3PO3的性质可推测Na2HPO3稀溶液的pH___ 7(填“>”、“=”或“<”),已知该溶液中离子浓度由大到小的顺序是c(Na+)>c(HPO )>c(OH-)>c(H2PO
)>c(OH-)>c(H2PO )>c(H+)。
)>c(H+)。
(1)PCl3水解可制取亚磷酸,化学方程式为
(2)H3PO3溶液中存在电离平衡:H3PO3
 H2PO
H2PO +H+。
+H+。①某温度下,0.10mol·L-1的H3PO3溶液pH=1.6,即溶液中c(H+)=2.5×10-2mol·L-1。该温度下上述电离平衡的平衡常数K=
②根据H3PO3的性质可推测Na2HPO3稀溶液的pH
 )>c(OH-)>c(H2PO
)>c(OH-)>c(H2PO )>c(H+)。
)>c(H+)。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】人体内尿酸(HUr)含量偏高,关节滑液中产生尿酸钠晶体(NaUr)会引发痛风,NaUr(s)  Na+(aq)+Ur−(aq) ∆H >0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
Na+(aq)+Ur−(aq) ∆H >0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
已知:①37℃时,Ka(HUr) = 4×10−6,Kw = 2.4×10−14,Ksp(NaUr) = 6.4×10−5
②37℃时,模拟关节滑液pH =7.4,c(Ur-) =4.6×10−4 mol∙L−1
(1)尿酸电离方程式为_______
(2)Kh为盐的水解常数,37℃时,Kh(Ur−)=_______ 。
(3)37℃时,向HUr溶液中加入NaOH溶液配制“模拟关节滑液”,溶液中c(Na+)_______ c(Ur−) (填“>”、“<”或“=”)。
(4)37℃时,向模拟关节滑液中加入NaCl(s)至c(Na+) = 0.2 mol∙L−1时,通过计算判断是否有NaUr晶体析出,请写出判断过程_______
(5)对于尿酸偏高的人群,下列建议正确的是_______ 。
a.加强锻炼,注意关节保暖 b.多饮酒,利用乙醇杀菌消毒
c.多喝水,饮食宜少盐、少脂 d.减少摄入易代谢出尿酸的食物
 Na+(aq)+Ur−(aq) ∆H >0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
Na+(aq)+Ur−(aq) ∆H >0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:已知:①37℃时,Ka(HUr) = 4×10−6,Kw = 2.4×10−14,Ksp(NaUr) = 6.4×10−5
②37℃时,模拟关节滑液pH =7.4,c(Ur-) =4.6×10−4 mol∙L−1
(1)尿酸电离方程式为
(2)Kh为盐的水解常数,37℃时,Kh(Ur−)=
(3)37℃时,向HUr溶液中加入NaOH溶液配制“模拟关节滑液”,溶液中c(Na+)
(4)37℃时,向模拟关节滑液中加入NaCl(s)至c(Na+) = 0.2 mol∙L−1时,通过计算判断是否有NaUr晶体析出,请写出判断过程
(5)对于尿酸偏高的人群,下列建议正确的是
a.加强锻炼,注意关节保暖 b.多饮酒,利用乙醇杀菌消毒
c.多喝水,饮食宜少盐、少脂 d.减少摄入易代谢出尿酸的食物
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】H2S溶于水的电离方程式为_______________________ 。
(1)向H2S溶液中加入CuSO4溶液时,电离平衡向_______ (左或右,下同)移动,c(H+)_______ ,c(S2-)________ 。(填偏大、偏小、不变,下同)
(2)向H2S溶液中加入NaOH固体时,电离平衡向________ 移动,c(H+)_________ ,c(S2-)__________ 。
(3)若将H2S溶液加热至沸腾,c(H2S)____________ 。
(1)向H2S溶液中加入CuSO4溶液时,电离平衡向
(2)向H2S溶液中加入NaOH固体时,电离平衡向
(3)若将H2S溶液加热至沸腾,c(H2S)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如右图所示。请回答:
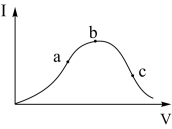
(1)a、b、c三点溶液中c(H+)由大到小的顺序为_____________ ;
(2)a、b、c三点中醋酸电离度最大的是_____________ ;
(3)若使C点溶液的c(CH3COO-)提高,在如下措施中可采取_____ (填标号)
A.通HCl气体
B.加Zn粒
C.加入固体KOH
D.加水
E.加固体CH3COONa

(1)a、b、c三点溶液中c(H+)由大到小的顺序为
(2)a、b、c三点中醋酸电离度最大的是
(3)若使C点溶液的c(CH3COO-)提高,在如下措施中可采取
A.通HCl气体
B.加Zn粒
C.加入固体KOH
D.加水
E.加固体CH3COONa
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】一水合氨(NH3·H2O)是一种常见的弱碱,回答下列问题:
在0.1mol·L﹣1氨水中加入下列物质,一水合氨的电离平衡及平衡时物质的浓度的变化:
(1)写出NH3·H2O的电离方程式____ 。
(2)向氨水中加入NH4Cl固体,电离平衡向___ 移动(填“正向”、“逆向”或“不移动”,下同);pH ___ (填“增大”、“减小”或“不变”,下同)
(3)向氨水中加入FeCl3固体,电离平衡向_____ 移动;c(NH3·H2O)______
(4)已知常温下,NH3·H2O的电离常数为Kb=1.8×10-5,若氨水的浓度为2.0mol∙L-1,则溶液中OH-的浓度是___ mol∙L-1。
在0.1mol·L﹣1氨水中加入下列物质,一水合氨的电离平衡及平衡时物质的浓度的变化:
(1)写出NH3·H2O的电离方程式
(2)向氨水中加入NH4Cl固体,电离平衡向
(3)向氨水中加入FeCl3固体,电离平衡向
(4)已知常温下,NH3·H2O的电离常数为Kb=1.8×10-5,若氨水的浓度为2.0mol∙L-1,则溶液中OH-的浓度是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】25℃时有以下5种溶液:①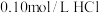 溶液;②
溶液;②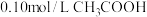 溶液;③
溶液;③ 溶液;④
溶液;④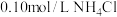 溶液;⑤
溶液;⑤ 溶液。
溶液。
(1)泡沫灭火器中的原料之一是上述5种溶液中的一种,此灭火器灭火的原理为_______ (用离子方程式表示)。
(2)往②加入少量 固体,此溶液的pH
固体,此溶液的pH_______ (填“增大”“减小”或“不变”)。
(3)①和②两种溶液中水的电离程度大小为①_______ ②(填“>”“<”或者“=”)。
(4)将②与③等体积混合后,溶液中存在的离子浓度由大到小的顺序是_______ (用离子符号表示)。
(5)用pH试纸测得④的 ,则此溶液中水电离出来的氢氧根离子浓度为
,则此溶液中水电离出来的氢氧根离子浓度为_______  。
。
(6)用 的标准盐酸滴定50.00mL未知浓度的NaOH溶液的酸碱中和滴定实验中,下列有关说法正确的是_______。
的标准盐酸滴定50.00mL未知浓度的NaOH溶液的酸碱中和滴定实验中,下列有关说法正确的是_______。
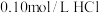 溶液;②
溶液;②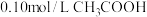 溶液;③
溶液;③ 溶液;④
溶液;④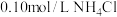 溶液;⑤
溶液;⑤ 溶液。
溶液。(1)泡沫灭火器中的原料之一是上述5种溶液中的一种,此灭火器灭火的原理为
(2)往②加入少量
 固体,此溶液的pH
固体,此溶液的pH(3)①和②两种溶液中水的电离程度大小为①
(4)将②与③等体积混合后,溶液中存在的离子浓度由大到小的顺序是
(5)用pH试纸测得④的
 ,则此溶液中水电离出来的氢氧根离子浓度为
,则此溶液中水电离出来的氢氧根离子浓度为 。
。(6)用
 的标准盐酸滴定50.00mL未知浓度的NaOH溶液的酸碱中和滴定实验中,下列有关说法正确的是_______。
的标准盐酸滴定50.00mL未知浓度的NaOH溶液的酸碱中和滴定实验中,下列有关说法正确的是_______。| A.用蒸馏水洗净酸式滴定管、锥形瓶后可分别直接注入标准盐酸和待测液NaOH溶液 |
| B.滴定时左手旋转滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视滴定管液面变化 |
| C.此中和滴定实验的指示剂可采用酚酞,滴定终点的现象为:溶液由无色变为红色,且30s内颜色不变 |
| D.若滴定前仰视读数、滴定后俯视读数,则所测NaOH溶液的浓度偏低 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】常温下,有c(H+)相同、体积相同的醋酸和盐酸两种溶液,采取以下措施:
(1)加适量醋酸钠晶体后,醋酸溶液中c(H+)_______ (填“增大”“减小”或“不变”,下同),盐酸中c(H+)______ 。
(2)加水稀释10倍后,醋酸溶液中的c(H+)______ (填“>”“=”或“<”)盐酸中的c(H+)。
(3)加等浓度的NaOH溶液至恰好中和,所需NaOH溶液的体积:醋酸_______ (填“>”“=”或“<”)盐酸。
(4)使温度都升高20℃,溶液中c(H+):醋酸________ (填“>”“=”或“<”)盐酸。
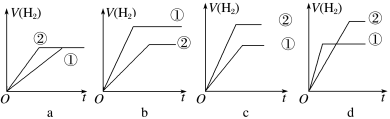
(5)分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是_______ (填字母)。(①表示盐酸,②表示醋酸)
(1)加适量醋酸钠晶体后,醋酸溶液中c(H+)
(2)加水稀释10倍后,醋酸溶液中的c(H+)
(3)加等浓度的NaOH溶液至恰好中和,所需NaOH溶液的体积:醋酸
(4)使温度都升高20℃,溶液中c(H+):醋酸
(5)分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】ⅰ.(1)氨气极易溶于水,氨气与水反应的化学方程式为_____________________ ;
氨水显碱性的原因是_____________________________ (用离子方程式表示)。
(2)在6份0.01 mol·L-1的氨水中分别加入下列物质:
A.浓氨水 B.纯水 C.少量浓硫酸 D.少量NaOH固体 E.少量Al2(SO4)3固体
①能使c(OH-)减少、c(NH4+)增大的是____ (填字母,下同)。
②能使c(OH-)增大、c(NH4+)减少的是____ 。
③能使c(OH-)和c(NH4+)都增大的是____ 。
④能使c(OH-)和c(NH4+)都减少的是____ 。
ⅱ.某温度下纯水中c(H+)=2×10-7 mol·L-1,则此时c(OH-)=________ ;该温度下向纯水中加盐酸使c(H+)=5×10-6 mol·L-1,则此时c(OH-)=______________________________ 。
氨水显碱性的原因是
(2)在6份0.01 mol·L-1的氨水中分别加入下列物质:
A.浓氨水 B.纯水 C.少量浓硫酸 D.少量NaOH固体 E.少量Al2(SO4)3固体
①能使c(OH-)减少、c(NH4+)增大的是
②能使c(OH-)增大、c(NH4+)减少的是
③能使c(OH-)和c(NH4+)都增大的是
④能使c(OH-)和c(NH4+)都减少的是
ⅱ.某温度下纯水中c(H+)=2×10-7 mol·L-1,则此时c(OH-)=
您最近一年使用:0次

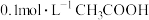 溶液的
溶液的

