25℃时有以下5种溶液:①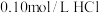 溶液;②
溶液;②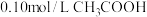 溶液;③
溶液;③ 溶液;④
溶液;④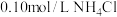 溶液;⑤
溶液;⑤ 溶液。
溶液。
(1)泡沫灭火器中的原料之一是上述5种溶液中的一种,此灭火器灭火的原理为_______ (用离子方程式表示)。
(2)往②加入少量 固体,此溶液的pH
固体,此溶液的pH_______ (填“增大”“减小”或“不变”)。
(3)①和②两种溶液中水的电离程度大小为①_______ ②(填“>”“<”或者“=”)。
(4)将②与③等体积混合后,溶液中存在的离子浓度由大到小的顺序是_______ (用离子符号表示)。
(5)用pH试纸测得④的 ,则此溶液中水电离出来的氢氧根离子浓度为
,则此溶液中水电离出来的氢氧根离子浓度为_______  。
。
(6)用 的标准盐酸滴定50.00mL未知浓度的NaOH溶液的酸碱中和滴定实验中,下列有关说法正确的是_______。
的标准盐酸滴定50.00mL未知浓度的NaOH溶液的酸碱中和滴定实验中,下列有关说法正确的是_______。
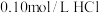 溶液;②
溶液;②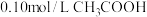 溶液;③
溶液;③ 溶液;④
溶液;④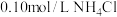 溶液;⑤
溶液;⑤ 溶液。
溶液。(1)泡沫灭火器中的原料之一是上述5种溶液中的一种,此灭火器灭火的原理为
(2)往②加入少量
 固体,此溶液的pH
固体,此溶液的pH(3)①和②两种溶液中水的电离程度大小为①
(4)将②与③等体积混合后,溶液中存在的离子浓度由大到小的顺序是
(5)用pH试纸测得④的
 ,则此溶液中水电离出来的氢氧根离子浓度为
,则此溶液中水电离出来的氢氧根离子浓度为 。
。(6)用
 的标准盐酸滴定50.00mL未知浓度的NaOH溶液的酸碱中和滴定实验中,下列有关说法正确的是_______。
的标准盐酸滴定50.00mL未知浓度的NaOH溶液的酸碱中和滴定实验中,下列有关说法正确的是_______。| A.用蒸馏水洗净酸式滴定管、锥形瓶后可分别直接注入标准盐酸和待测液NaOH溶液 |
| B.滴定时左手旋转滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视滴定管液面变化 |
| C.此中和滴定实验的指示剂可采用酚酞,滴定终点的现象为:溶液由无色变为红色,且30s内颜色不变 |
| D.若滴定前仰视读数、滴定后俯视读数,则所测NaOH溶液的浓度偏低 |
更新时间:2022-11-05 22:57:26
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】电解质的水溶液中存在电离平衡。
(1)NH3·H2O是常见的弱碱。
①NH3·H2O在水溶液中的电离方程式为_______ 。
②下列方法中,可以使氨水中NH3·H2O电离程度减小的是(填字母序号)________ 。
a.微热溶液 b.滴加浓盐酸 c.加水稀释 d.加入氯化铵晶体
(2)常温条件下,用0.1000mol/L NaOH溶液分别滴定体积均为 、浓度均为0.1000mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。
、浓度均为0.1000mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。_______ 。
②滴定醋酸的曲线是_______ (填“I”或“Ⅱ”),则V1______ V2(填“>”、 “<”“或“=”)。
(3)如图为盛放盐酸的滴定管中液面的位置。盐酸的体积读数:滴定后读数为_____ mL。 未知浓度的醋酸放入锥形瓶中,用0.1000mol/L NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
未知浓度的醋酸放入锥形瓶中,用0.1000mol/L NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
①该滴定过程应选择______ (填“甲基橙”或“酚酞”)为指示剂,根据上述数据,可计算出该醋酸的浓度约为_____  。
。
②在上述实验中,下列操作会造成测定结果偏大的有______ 。(填字母序号)。
A.滴定前仰视读数,滴定后俯视读数
B.碱式滴定管使用前,水洗后未用标准氢氧化钠溶液润洗
C.滴定过程中,溶液刚出现变色,立即停止滴定
D.锥形瓶水洗后未干燥
E.碱式滴定管尖嘴部分有气泡,滴定后消失
(1)NH3·H2O是常见的弱碱。
①NH3·H2O在水溶液中的电离方程式为
②下列方法中,可以使氨水中NH3·H2O电离程度减小的是(填字母序号)
a.微热溶液 b.滴加浓盐酸 c.加水稀释 d.加入氯化铵晶体
(2)常温条件下,用0.1000mol/L NaOH溶液分别滴定体积均为
 、浓度均为0.1000mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。
、浓度均为0.1000mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。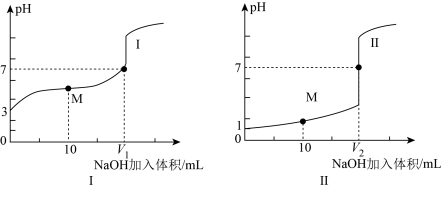
②滴定醋酸的曲线是
(3)如图为盛放盐酸的滴定管中液面的位置。盐酸的体积读数:滴定后读数为

 未知浓度的醋酸放入锥形瓶中,用0.1000mol/L NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
未知浓度的醋酸放入锥形瓶中,用0.1000mol/L NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。| 实验编号 | NaOH溶液的浓度(mol·L-1) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测醋酸的体积(mL) |
| 1 | 0.1000 | 22.48 | 20.00 |
| 2 | 0.1000 | 25.72 | 20.00 |
| 3 | 0.1000 | 22.52 | 20.00 |
 。
。②在上述实验中,下列操作会造成测定结果偏大的有
A.滴定前仰视读数,滴定后俯视读数
B.碱式滴定管使用前,水洗后未用标准氢氧化钠溶液润洗
C.滴定过程中,溶液刚出现变色,立即停止滴定
D.锥形瓶水洗后未干燥
E.碱式滴定管尖嘴部分有气泡,滴定后消失
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】某化学小组用中和滴定法测定烧碱样品的纯度,请回答下列问题:
(1)准确称量5.0000 g含有少量易溶杂质的样品(假设杂质不与盐酸反应),配成250 mL待测溶液,用到的玻璃仪器有烧杯、玻璃棒、 胶头滴管、___________
(2)滴定时,用0.2000mol/L的盐酸来滴定待测溶液,量取待测液10.00 mL应选用下图中的___________ (填“甲”或“乙”),该仪器的名称是___________
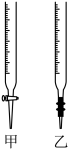
(3)滴定过程中,眼睛应注视___________ ;若以酚酞溶液做指示剂,则滴定终点的现象是 ___________ 。
(4)由下表可知,第二次所用盐酸的实际体积明显偏大,其原因可能是___________(填序号)
(5)根据表中数据,计算被测烧碱样品的纯度是___________ %。
(1)准确称量5.0000 g含有少量易溶杂质的样品(假设杂质不与盐酸反应),配成250 mL待测溶液,用到的玻璃仪器有烧杯、玻璃棒、 胶头滴管、
(2)滴定时,用0.2000mol/L的盐酸来滴定待测溶液,量取待测液10.00 mL应选用下图中的

(3)滴定过程中,眼睛应注视
(4)由下表可知,第二次所用盐酸的实际体积明显偏大,其原因可能是___________(填序号)
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前的读数/mL | 滴定后的读数/mL | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 2.10 | 24.20 |
| 第三次 | 10.00 | 4.10 | 24.00 |
| A.锥形瓶用待测液润洗 | B.滴定过程中锥形瓶内溶液溅出瓶外 |
| C.滴定前滴定管尖嘴有气泡,滴定后气泡消失 | D.滴定结束时,俯视读数 |
(5)根据表中数据,计算被测烧碱样品的纯度是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】(1)内因:___________________ 。
(2)外因:①浓度:_________________________
②温度:________________________________________
③酸碱度
(3)酸式盐溶液的酸碱性:强酸酸式盐显__________ ,原因是_____________________________ 。多元弱酸酸式盐溶液的酸碱性取决于_____________________________________ ,例如NaHCO3溶液显碱性,原因是_________________ ,_______________________________ (离子方程式和文字说明);
NaHSO3溶液显酸性的原因是________________ ,_____________________ (离子方程式和文字说明)。
(4)用↑、↓、→、←表示,填表:CH3COONa溶液改变下列条件,填写变化情况:CH3COO-+H2O CH3COOH+OH-
CH3COOH+OH-_______________
(2)外因:①浓度:
②温度:
③酸碱度
(3)酸式盐溶液的酸碱性:强酸酸式盐显
NaHSO3溶液显酸性的原因是
(4)用↑、↓、→、←表示,填表:CH3COONa溶液改变下列条件,填写变化情况:CH3COO-+H2O
 CH3COOH+OH-
CH3COOH+OH-| 改变条件 | 平衡移动 | c(CH3COO-) | c(OH-) | 水解 |
| 加入CH3COONa | ||||
| 通入HCl | ||||
| 升温 | ||||
| 加水 | ||||
| 加NaOH | ||||
| 加HAc | ||||
| 加NH4Cl |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)氨水中存在:NH3·H2O
 +OH-,在5份0.01 mol∙L−1的氨水中分别加入下列各物质:A、浓氨水,B、纯水,C、少量NaOH固体, D、NH4Cl固体。
+OH-,在5份0.01 mol∙L−1的氨水中分别加入下列各物质:A、浓氨水,B、纯水,C、少量NaOH固体, D、NH4Cl固体。
按照要求填空(答案选填物质对应的字母):
①电离平衡会向正向移动是_________ ,电离平衡会向逆向移动是__________ 。
②c( )、c(OH-)都增大的是
)、c(OH-)都增大的是___________ ,c( )、c(OH-)都变小的是
)、c(OH-)都变小的是___________ 。
③c( )增大,c(OH-)减小的是
)增大,c(OH-)减小的是___________ 。
④c( )减小,c(OH-)增大的是
)减小,c(OH-)增大的是___________ 。
(2)将6 g CH3COOH溶于水制成1 L溶液,此溶液的物质的量浓度为_________ ,若此温度下醋酸的电离常数K=1×10−5,pH为______ ,若升高温度, K将___________ (填“变大”、“变小”或“不变”)。
(3)Ⅰ、现有浓度均为0.1 mol∙L−1的盐酸、硫酸、醋酸三种溶液,回答下列问题:
①若三种溶液中c(H+)分别为a mol∙L−1、b mol∙L−1、c mol∙L−1,则它们的大小关系为__________ 。
②等体积的以上三种酸分别与过量的NaOH溶液反应,若生成的盐的物质的量依次为A mol、B mol、C mol,则它们的大小关系为__________ 。
Ⅱ、现有pH=3的盐酸、硫酸、醋酸三种溶液,回答下列问题:
①分别用以上三种酸中和一定量的NaOH溶液生成正盐,若需要酸的体积分别为V1、V2、V3,其大小关系为________________ 。
②分别与Zn反应,开始时生成H2的速率为v1、v2、v3,其大小关系为____________ 。

 +OH-,在5份0.01 mol∙L−1的氨水中分别加入下列各物质:A、浓氨水,B、纯水,C、少量NaOH固体, D、NH4Cl固体。
+OH-,在5份0.01 mol∙L−1的氨水中分别加入下列各物质:A、浓氨水,B、纯水,C、少量NaOH固体, D、NH4Cl固体。按照要求填空(答案选填物质对应的字母):
①电离平衡会向正向移动是
②c(
 )、c(OH-)都增大的是
)、c(OH-)都增大的是 )、c(OH-)都变小的是
)、c(OH-)都变小的是③c(
 )增大,c(OH-)减小的是
)增大,c(OH-)减小的是④c(
 )减小,c(OH-)增大的是
)减小,c(OH-)增大的是(2)将6 g CH3COOH溶于水制成1 L溶液,此溶液的物质的量浓度为
(3)Ⅰ、现有浓度均为0.1 mol∙L−1的盐酸、硫酸、醋酸三种溶液,回答下列问题:
①若三种溶液中c(H+)分别为a mol∙L−1、b mol∙L−1、c mol∙L−1,则它们的大小关系为
②等体积的以上三种酸分别与过量的NaOH溶液反应,若生成的盐的物质的量依次为A mol、B mol、C mol,则它们的大小关系为
Ⅱ、现有pH=3的盐酸、硫酸、醋酸三种溶液,回答下列问题:
①分别用以上三种酸中和一定量的NaOH溶液生成正盐,若需要酸的体积分别为V1、V2、V3,其大小关系为
②分别与Zn反应,开始时生成H2的速率为v1、v2、v3,其大小关系为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】人体内尿酸(HUr)含量偏高,关节滑液中产生尿酸钠晶体(NaUr)会引发痛风,NaUr(s)  Na+(aq)+Ur−(aq) ∆H >0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
Na+(aq)+Ur−(aq) ∆H >0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
已知:①37℃时,Ka(HUr) = 4×10−6,Kw = 2.4×10−14,Ksp(NaUr) = 6.4×10−5
②37℃时,模拟关节滑液pH =7.4,c(Ur-) =4.6×10−4 mol∙L−1
(1)尿酸电离方程式为_______
(2)Kh为盐的水解常数,37℃时,Kh(Ur−)=_______ 。
(3)37℃时,向HUr溶液中加入NaOH溶液配制“模拟关节滑液”,溶液中c(Na+)_______ c(Ur−) (填“>”、“<”或“=”)。
(4)37℃时,向模拟关节滑液中加入NaCl(s)至c(Na+) = 0.2 mol∙L−1时,通过计算判断是否有NaUr晶体析出,请写出判断过程_______
(5)对于尿酸偏高的人群,下列建议正确的是_______ 。
a.加强锻炼,注意关节保暖 b.多饮酒,利用乙醇杀菌消毒
c.多喝水,饮食宜少盐、少脂 d.减少摄入易代谢出尿酸的食物
 Na+(aq)+Ur−(aq) ∆H >0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
Na+(aq)+Ur−(aq) ∆H >0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:已知:①37℃时,Ka(HUr) = 4×10−6,Kw = 2.4×10−14,Ksp(NaUr) = 6.4×10−5
②37℃时,模拟关节滑液pH =7.4,c(Ur-) =4.6×10−4 mol∙L−1
(1)尿酸电离方程式为
(2)Kh为盐的水解常数,37℃时,Kh(Ur−)=
(3)37℃时,向HUr溶液中加入NaOH溶液配制“模拟关节滑液”,溶液中c(Na+)
(4)37℃时,向模拟关节滑液中加入NaCl(s)至c(Na+) = 0.2 mol∙L−1时,通过计算判断是否有NaUr晶体析出,请写出判断过程
(5)对于尿酸偏高的人群,下列建议正确的是
a.加强锻炼,注意关节保暖 b.多饮酒,利用乙醇杀菌消毒
c.多喝水,饮食宜少盐、少脂 d.减少摄入易代谢出尿酸的食物
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】(1)配平下列离子方程式:
___  +
+___ H2C2O4+___ H+ =___ Mn2++___ +___ H2O
(2)3.4 gOH-含有的电子数目是___________ 。
(3)2CuH+2HCl=Cu+CuCl2+2H2↑,反应产生4.48 LH2(标准状况)时,转移的电子数为___________ 。
(4)物质的量浓度相同的三种盐NaX、NaY和NaZ的溶液中,其pH分别为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是___________ 。
(5)用原子符号表示中子数为11的Na原子___________ 。
(6)30 gHCHO和CH3COOH含有的共价键数目为___________ 。
(7)C4H8ClBr有___________ 种同分异构体。
 +
+(2)3.4 gOH-含有的电子数目是
(3)2CuH+2HCl=Cu+CuCl2+2H2↑,反应产生4.48 LH2(标准状况)时,转移的电子数为
(4)物质的量浓度相同的三种盐NaX、NaY和NaZ的溶液中,其pH分别为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是
(5)用原子符号表示中子数为11的Na原子
(6)30 gHCHO和CH3COOH含有的共价键数目为
(7)C4H8ClBr有
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】(1)物质的量浓度相等的①(NH4)2SO4、②(NH4)2CO3、③(NH4)2Fe(SO4)2、④NH4Cl四种溶液中:c( )由大到小的关系
)由大到小的关系___________ (填序号)
(2)已知 25℃ 时有关弱酸的电离平衡常数:
等物质的量浓度的①NaCN、②Na2CO3、③NaHCO3、④CH3COONa溶液 pH由大到小关系为:_______ (填序号)
 )由大到小的关系
)由大到小的关系(2)已知 25℃ 时有关弱酸的电离平衡常数:
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
等物质的量浓度的①NaCN、②Na2CO3、③NaHCO3、④CH3COONa溶液 pH由大到小关系为:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】常温下,将某一元酸 和
和 溶液等体积混合,两种溶液的浓度和混合后所得溶液的
溶液等体积混合,两种溶液的浓度和混合后所得溶液的 如下表:
如下表:
(1)从①组情况分析, 是强酸还是弱酸?
是强酸还是弱酸?___________ 。
(2)②组情况表明,
___________ (填“>”、“<”或“=”,下同)0.2.混合溶液中离子浓度
___________  。
。
(3)从③组实验结果分析, 的电离程度
的电离程度___________ (填“>”、“<”或“=”) 的水解程度,该混合溶液中离子浓度由大到小的顺序是
的水解程度,该混合溶液中离子浓度由大到小的顺序是___________ 。
(4)从以上实验分析,将 的
的 溶液与
溶液与 的
的 溶液等体积混合,所得混合溶液中
溶液等体积混合,所得混合溶液中
___________ (填“>”、“<”或“=”) 。
。
 和
和 溶液等体积混合,两种溶液的浓度和混合后所得溶液的
溶液等体积混合,两种溶液的浓度和混合后所得溶液的 如下表:
如下表:| 实验编号 |  溶液的物质的量浓度 溶液的物质的量浓度 |  溶液的物质的量浓度 溶液的物质的量浓度 | 混合溶液的 |
| ① | 0.1 | 0.1 |  |
| ② |  | 0.2 |  |
| ③ | 0.2 | 0.1 |  |
 是强酸还是弱酸?
是强酸还是弱酸?(2)②组情况表明,


 。
。(3)从③组实验结果分析,
 的电离程度
的电离程度 的水解程度,该混合溶液中离子浓度由大到小的顺序是
的水解程度,该混合溶液中离子浓度由大到小的顺序是(4)从以上实验分析,将
 的
的 溶液与
溶液与 的
的 溶液等体积混合,所得混合溶液中
溶液等体积混合,所得混合溶液中
 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】汽车是人们出行的重要交通工具,其中蕴含着大量的化学知识,回答下列问题:
(1)汽车中包含多种材料,制轮胎的丁苯橡胶属于_______ (填“天然”或“合成”)橡胶。
(2)汽车安全气囊启动时发生的反应有: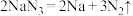 ,用单线桥表示该反应中的电子转移情况:
,用单线桥表示该反应中的电子转移情况:_______ 。
(3)在催化剂作用下,汽车尾气中的 与
与 能转化成两种无污染的气体,写出反应的化学方程式
能转化成两种无污染的气体,写出反应的化学方程式_______ 。
(4)汽车排放的 会加剧温室效应,实验室用
会加剧温室效应,实验室用 溶液吸收
溶液吸收 ,当
,当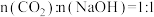 时,所得溶液呈碱性,原因是
时,所得溶液呈碱性,原因是_______ ,
_______ 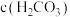 (填“>”或“<”)。
(填“>”或“<”)。
(5)使用燃料电池汽车可解决 的排放,写出
的排放,写出 溶液环境下甲醇燃料电池的负极电极反应式
溶液环境下甲醇燃料电池的负极电极反应式_______ 。
(1)汽车中包含多种材料,制轮胎的丁苯橡胶属于
(2)汽车安全气囊启动时发生的反应有:
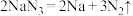 ,用单线桥表示该反应中的电子转移情况:
,用单线桥表示该反应中的电子转移情况:(3)在催化剂作用下,汽车尾气中的
 与
与 能转化成两种无污染的气体,写出反应的化学方程式
能转化成两种无污染的气体,写出反应的化学方程式(4)汽车排放的
 会加剧温室效应,实验室用
会加剧温室效应,实验室用 溶液吸收
溶液吸收 ,当
,当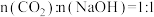 时,所得溶液呈碱性,原因是
时,所得溶液呈碱性,原因是
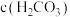 (填“>”或“<”)。
(填“>”或“<”)。(5)使用燃料电池汽车可解决
 的排放,写出
的排放,写出 溶液环境下甲醇燃料电池的负极电极反应式
溶液环境下甲醇燃料电池的负极电极反应式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】常温下,有四种溶液:
①0.1 mol·L-1 CH3COOH溶液 ②0.1 mol·L-1 CH3COONa溶液 ③0.1 mol·L-1 NaHSO3溶液④0.1 mol·L-1 NaHCO3溶液
(1)溶液①的pH____ (填“>”“<”或“=”)7,溶液中离子的电荷守恒关系式是___ 。
(2)溶液②呈______ (填“酸”“碱”或“中”)性。其原因是___ (用离子方程式说明)。
(3)下列有关①和②两种溶液的说法正确的是____ (填字母)。
a. 两种溶液中c(CH3COO-) 都小于0.1 mol·L-1
b. 两种溶液中c(CH3COO-) 都等于0.1 mol·L-1
c. CH3COOH溶液中c(CH3COO-) 小于CH3COONa溶液中c(CH3COO-)
(4)NaHCO3溶液的pH>7,NaHSO3溶液的pH<7,则,NaHCO3溶液中c(H2CO3)______ (填“>”“<”或“=”,下同)c( ),NaHSO3溶液中c(H2SO3)
),NaHSO3溶液中c(H2SO3)____ c( )
)
①0.1 mol·L-1 CH3COOH溶液 ②0.1 mol·L-1 CH3COONa溶液 ③0.1 mol·L-1 NaHSO3溶液④0.1 mol·L-1 NaHCO3溶液
(1)溶液①的pH
(2)溶液②呈
(3)下列有关①和②两种溶液的说法正确的是
a. 两种溶液中c(CH3COO-) 都小于0.1 mol·L-1
b. 两种溶液中c(CH3COO-) 都等于0.1 mol·L-1
c. CH3COOH溶液中c(CH3COO-) 小于CH3COONa溶液中c(CH3COO-)
(4)NaHCO3溶液的pH>7,NaHSO3溶液的pH<7,则,NaHCO3溶液中c(H2CO3)
 ),NaHSO3溶液中c(H2SO3)
),NaHSO3溶液中c(H2SO3) )
)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】回答下列问题:
(1)泡沫灭火器的灭火原理是_______ (用离子方程式表示)。
(2)①已知T ℃时,Kw=1×10-12 mol2·L-2,在该温度时,将pH=9的NaOH溶液a L与pH=2的H2SO4溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=3,则a∶b=_______ 。
②某二元酸(用H2A表示)在水中的电离方程式是:H2A=H++HA-,HA- H++A2-,则NaHA溶液中,写出物料守恒式
H++A2-,则NaHA溶液中,写出物料守恒式_______ 。
(3)pH=2的两种一元酸HA和HB,体积均为100 mL,稀释过程中pH与溶液体积的关系如图。

①则NaB水溶液呈_______ (填“中性”或“碱性”),原因_______ (用离子方程式表示)。
②则HA的酸性_______ (填“大于”“小于”或“等于”)HB的酸性,理由是_______ 。
(4)NaHSO3溶液呈酸性,则溶液中各离子浓度由大到小的顺序为_______ 。
(1)泡沫灭火器的灭火原理是
(2)①已知T ℃时,Kw=1×10-12 mol2·L-2,在该温度时,将pH=9的NaOH溶液a L与pH=2的H2SO4溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=3,则a∶b=
②某二元酸(用H2A表示)在水中的电离方程式是:H2A=H++HA-,HA-
 H++A2-,则NaHA溶液中,写出物料守恒式
H++A2-,则NaHA溶液中,写出物料守恒式(3)pH=2的两种一元酸HA和HB,体积均为100 mL,稀释过程中pH与溶液体积的关系如图。

①则NaB水溶液呈
②则HA的酸性
(4)NaHSO3溶液呈酸性,则溶液中各离子浓度由大到小的顺序为
您最近一年使用:0次

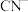 ,一种测定其含量的方法是:取废水50mL,再加KI溶液1mL,用c
,一种测定其含量的方法是:取废水50mL,再加KI溶液1mL,用c
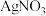 溶液滴定,消耗
溶液滴定,消耗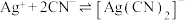 (无色),
(无色),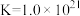 ;
;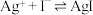 ,
,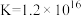 。滴定终点的现象是
。滴定终点的现象是

