下图中X、Y、Z为单质,其它为化合物,它们之间存在如下转化关系(部分产物已略去)。已知,G溶液中滴加KSCN溶液显血红色,Z单质是航空工业常用的金属材料。
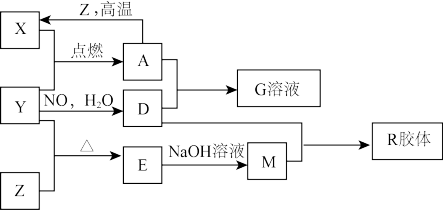
回答下列问题:
(1)A物质的化学式为_______ ,M的名称_______ 。
(2)一定条件下,Z的氢化物与水反应的化学方程式为_______ 。
(3)A和D的稀溶液反应的现象为_______ 。

回答下列问题:
(1)A物质的化学式为
(2)一定条件下,Z的氢化物与水反应的化学方程式为
(3)A和D的稀溶液反应的现象为
更新时间:2022-12-20 19:59:27
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知A与D均为非金属单质,其中A有多种同素异形体,其转化关系如下图。
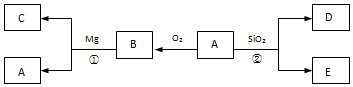
请回答:
(1)反应②为工业制粗硅原理,写出化学方程式:______ 。
(2)反应①可同时产生黑白两种固体的化学方程式为_____ 。

请回答:
(1)反应②为工业制粗硅原理,写出化学方程式:
(2)反应①可同时产生黑白两种固体的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下图是中学化学中常见物质的转化关系,部分物质和反应条件略去。

(1)写出单质B与强碱溶液反应的离子方程式___________________________ ,写出由沉淀J生成H溶液的离子方程式_______________________________ 。
(2)溶液E中加入氨水时,先生成白色沉淀L,白色沉淀L最终变为红褐色沉淀G,写出L变为G的化学反应方程式______________________________ 。
(3) K是一种集消毒与净水为一体的新型净水剂,试写出G→K的化学方程式:_______________
(4)溶液I中所含金属离子是__________________ 。

(1)写出单质B与强碱溶液反应的离子方程式
(2)溶液E中加入氨水时,先生成白色沉淀L,白色沉淀L最终变为红褐色沉淀G,写出L变为G的化学反应方程式
(3) K是一种集消毒与净水为一体的新型净水剂,试写出G→K的化学方程式:
(4)溶液I中所含金属离子是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某化学小组设计如图1所示实验装置制备硝酸并探究其性质。
Ⅰ、硝酸的制备:

(1)a处最合适的装置是______ (填“图2”或“图3”)。
(2)装置b中 的作用是
的作用是______ 。
Ⅱ、硝酸的性质探究:
(3)常温下,同学甲在硝酸的制备实验结束后,用pH计测得装置e中溶液的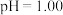 。
。
①这说明装置e中发生的反应可能为________________________ (填化学方程式)。
②同学乙做同样实验,测得装置e中溶液的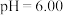 ,可能的原因是
,可能的原因是____________ 。
(4)用如图4所示装置进行硝酸与铜的反应。
①硝酸一般盛放在棕色试剂瓶中,请用化学方程式说明其原因:____________ 。
②装置g中为稀硝酸时,反应开始后,装置g中溶液颜色变蓝。写出装置g中反应的离子方程式:____________ 。
③装置g中为浓硝酸时,反应开始后,装置g中溶液颜色变绿。反应较②中剧烈许多的原因是____________ 。
④对比②与③反应后装置g中溶液颜色,推测其原因是③反应后装置g溶液中溶有 且达饱和。为证明该推测正确,向③反应后装置g溶液中加入
且达饱和。为证明该推测正确,向③反应后装置g溶液中加入______ ,会观察到溶液颜色由绿色变为蓝色。
⑤已知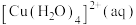 呈蓝色、
呈蓝色、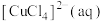 呈黄色。取②中少量蓝色溶液于试管中,向其中滴加饱和NaCl溶液,观察到溶液颜色由蓝色变为蓝绿色,再加热该混合溶液,溶液颜色逐渐变为黄绿色。结合离子方程式解释其原因:
呈黄色。取②中少量蓝色溶液于试管中,向其中滴加饱和NaCl溶液,观察到溶液颜色由蓝色变为蓝绿色,再加热该混合溶液,溶液颜色逐渐变为黄绿色。结合离子方程式解释其原因:________________________ 。
Ⅰ、硝酸的制备:

(1)a处最合适的装置是
(2)装置b中
 的作用是
的作用是Ⅱ、硝酸的性质探究:
(3)常温下,同学甲在硝酸的制备实验结束后,用pH计测得装置e中溶液的
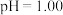 。
。①这说明装置e中发生的反应可能为
②同学乙做同样实验,测得装置e中溶液的
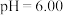 ,可能的原因是
,可能的原因是(4)用如图4所示装置进行硝酸与铜的反应。
①硝酸一般盛放在棕色试剂瓶中,请用化学方程式说明其原因:
②装置g中为稀硝酸时,反应开始后,装置g中溶液颜色变蓝。写出装置g中反应的离子方程式:
③装置g中为浓硝酸时,反应开始后,装置g中溶液颜色变绿。反应较②中剧烈许多的原因是
④对比②与③反应后装置g中溶液颜色,推测其原因是③反应后装置g溶液中溶有
 且达饱和。为证明该推测正确,向③反应后装置g溶液中加入
且达饱和。为证明该推测正确,向③反应后装置g溶液中加入⑤已知
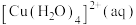 呈蓝色、
呈蓝色、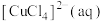 呈黄色。取②中少量蓝色溶液于试管中,向其中滴加饱和NaCl溶液,观察到溶液颜色由蓝色变为蓝绿色,再加热该混合溶液,溶液颜色逐渐变为黄绿色。结合离子方程式解释其原因:
呈黄色。取②中少量蓝色溶液于试管中,向其中滴加饱和NaCl溶液,观察到溶液颜色由蓝色变为蓝绿色,再加热该混合溶液,溶液颜色逐渐变为黄绿色。结合离子方程式解释其原因:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某学习小组在实验室研究SO2与Ba(NO3)2溶液的反应:
实验:向盛有2mL 0.1 mol∙L−1 Ba(NO3)2 溶液的试管中,缓慢通入SO2气体,试管内有白色沉淀产生,液面上方略显浅棕色。
探究1:白色沉淀产生的原因。
(1)白色沉淀是 。
(2)分析白色沉淀产生的原因,甲同学认为是 氧化了SO2,乙同学认为是溶液中溶解的O2氧化了SO2。
氧化了SO2,乙同学认为是溶液中溶解的O2氧化了SO2。
①支持甲同学观点的实验证据是_______ 。
②依据甲的推断,请写出Ba(NO3)2溶液与SO2反应的离子方程式_______ 。
③乙同学通过下列实验证明了自己的推测正确,请完成实验方案:
探究2:在氧化SO2的过程中, 和O2哪种微粒起到了主要作用。
和O2哪种微粒起到了主要作用。
(3)图1,在无氧条件下,BaCl2溶液pH下降的原因是_______ 。
(4)图2,BaCl2溶液中发生反应的离子方程式为_______ 。
(5)依据上述图像你得出的结论是_______ ,说明理由_______ 。
实验:向盛有2mL 0.1 mol∙L−1 Ba(NO3)2 溶液的试管中,缓慢通入SO2气体,试管内有白色沉淀产生,液面上方略显浅棕色。
探究1:白色沉淀产生的原因。
(1)白色沉淀是 。
(2)分析白色沉淀产生的原因,甲同学认为是
 氧化了SO2,乙同学认为是溶液中溶解的O2氧化了SO2。
氧化了SO2,乙同学认为是溶液中溶解的O2氧化了SO2。①支持甲同学观点的实验证据是
②依据甲的推断,请写出Ba(NO3)2溶液与SO2反应的离子方程式
③乙同学通过下列实验证明了自己的推测正确,请完成实验方案:
| 实验操作 | 实验现象 |
| 向2mL |
 和O2哪种微粒起到了主要作用。
和O2哪种微粒起到了主要作用。| 实验操作 | 实验数据 |
| 向烧杯中加入煮沸了的0.1 mol∙L−1的BaCl2溶液25mL,再加入25mL植物油,冷却至室温,用pH传感器测定溶液pH随时间(t)的变化曲线 |  图1:向BaCl2(无氧)溶液中通入SO2 |
| 向烧杯中分别加入25mL 0.1 mol∙L−1的BaCl2溶液、Ba(NO3)2溶液,通入SO2 ,用pH传感器分别测定溶液pH随时间(t)变化的曲线。 |  图2:分别向BaCl2、Ba(NO3)2溶液中通入SO2 图2:分别向BaCl2、Ba(NO3)2溶液中通入SO2 |
(4)图2,BaCl2溶液中发生反应的离子方程式为
(5)依据上述图像你得出的结论是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】亚硝酰氯(NOCl)是有机物合成中的重要试剂,是一种红褐色液体或黄色气体,遇水剧烈反应,熔点:-64.5℃,沸点:-5.5℃。某研究性学习小组在实验室中按照下图所示装置制备NOCl。请回答下列问题:

(1)仪器a中发生反应的离子方程式为___________ 。
(2)盛装无水 的仪器名称为
的仪器名称为___________ ,无水 的作用是
的作用是___________ 。
(3)试剂X和试剂Y分别是___________ 、___________ 。
(4)实验时,先在D中的三颈烧瓶内通入 ,开始通入NO气体的标志是三颈烧瓶中
,开始通入NO气体的标志是三颈烧瓶中___________ 。
(5)装置D中,将三颈烧瓶浸在冰盐浴中的目的是___________ 。
(6)尾气中含有少量NOCl,可用NaOH溶液吸收,请写出发生反应的化学方程式:___________ 。

(1)仪器a中发生反应的离子方程式为
(2)盛装无水
 的仪器名称为
的仪器名称为 的作用是
的作用是(3)试剂X和试剂Y分别是
(4)实验时,先在D中的三颈烧瓶内通入
 ,开始通入NO气体的标志是三颈烧瓶中
,开始通入NO气体的标志是三颈烧瓶中(5)装置D中,将三颈烧瓶浸在冰盐浴中的目的是
(6)尾气中含有少量NOCl,可用NaOH溶液吸收,请写出发生反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】有A、B、C、D、E五种化合物,其中A、B、C、D是含铝元素的化合物,F是一种气体,标准状况下相对于空气的密度为1.103。它们之间有下列的转化关系:
①A+NaOH→D+H2O ②B→A+ H2O ③C+ NaOH→B+NaCl ④E+ H2O→NaOH+F
⑴写出A、B、C、D的化学式:
A_____________ ,B____________ ,C__________ ,E__________ 。
⑵写出①③④的离子方程式:
①__________________________________________________ ,
③__________________________________________________ ,
④__________________________________________________ 。
①A+NaOH→D+H2O ②B→A+ H2O ③C+ NaOH→B+NaCl ④E+ H2O→NaOH+F
⑴写出A、B、C、D的化学式:
A
⑵写出①③④的离子方程式:
①
③
④
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D均为中学化学中常见的物质,它们之间转化关系如图(部分产物已略去):
A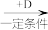 B
B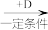 C
C
试回答:
(1)若D是具有氧化性的单质,则属于主族的金属A为___________ (填元素符号)
(2)若D是金属,C溶液在储存时应加入少量金属D,其理由是(用必要的文字和离子方程式表示)______
(3)若A、B、C为含同一种金属元素的无机化合物,且三种物质中有一种是白色不溶物。在溶液中A和C反应生成B。请写出B转化为C的所有可能的离子力程式_________ 、_________
(4)某一离子反应体系有反应物和产物共以下六种:MnO4-、H+、O2、H2O、H2O2、Mn2+。
①写出该氧化还原反应的离子方程式_______
②溶液随着酸性的增强氧化性不断增强,应选择_________ (选填“稀硫酸”或“浓盐酸”)进行KMnO4溶液的酸化。
③如反应转移了0.6mol电子,则产生的气体在标准状况下体积为__________
(5)一份溶液中可能含有K+、Al3+、Mg2+、Fe2+、 H+、NH4+、Cl-、HCO3-、ClO-、AlO2-等离子中的若干种。为了确定溶液的组成,进行了如下操作:
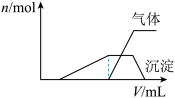
往该溶液中逐滴加入NaOH溶液并适当加热,产生沉淀和气体的物质的量(n)与加入NaOH溶液的体积关系如图所示;则该溶液中一定存在的离子是_______ ,一定不存在的离子是________ 。
A
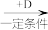 B
B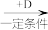 C
C试回答:
(1)若D是具有氧化性的单质,则属于主族的金属A为
(2)若D是金属,C溶液在储存时应加入少量金属D,其理由是(用必要的文字和离子方程式表示)
(3)若A、B、C为含同一种金属元素的无机化合物,且三种物质中有一种是白色不溶物。在溶液中A和C反应生成B。请写出B转化为C的所有可能的离子力程式
(4)某一离子反应体系有反应物和产物共以下六种:MnO4-、H+、O2、H2O、H2O2、Mn2+。
①写出该氧化还原反应的离子方程式
②溶液随着酸性的增强氧化性不断增强,应选择
③如反应转移了0.6mol电子,则产生的气体在标准状况下体积为
(5)一份溶液中可能含有K+、Al3+、Mg2+、Fe2+、 H+、NH4+、Cl-、HCO3-、ClO-、AlO2-等离子中的若干种。为了确定溶液的组成,进行了如下操作:

往该溶液中逐滴加入NaOH溶液并适当加热,产生沉淀和气体的物质的量(n)与加入NaOH溶液的体积关系如图所示;则该溶液中一定存在的离子是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素。在一定条件下相互转化的关系如下图所示。
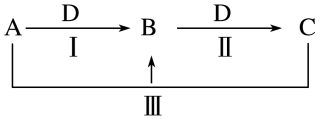
请回答下列问题。
(1)若A、B、C为含有同种金属元素的化合物,D为强酸或强碱溶液,当D为强碱溶液时,写出A中阳离子的结构示意图_______ ;C中通入过量CO2的离子方程式为_______ 。
(2)若A、B、C的溶液均显碱性,C为焙制糕点的发酵粉的主要成分之一:
①D的电子式为_______ 。
②除去B固体中混有的C固体的方法为_______ (填除杂方法的名称);若向B的饱和溶液中通入足量的D,则可观察到的现象为_______ 。
(3)若A为气体单质,D为一种黑色金属单质。
①反应Ⅲ的离子方程式为_______ 。
②一定条件下,D能与水发生反应,该反应的化学方程式为_______ 。
③将C与NaHCO3溶液混合产生白色沉淀且3 min后沉淀颜色不变。实验探究沉淀的组成。已知Fe(HCO3)2在水中不存在。
i.取少量白色沉淀充分洗涤,向其中加入稀硫酸,沉淀完全溶解,产生无色气泡。
ii.向i所得溶液中滴入KSCN溶液,溶液几乎不变红。
iii.向ii溶液中再滴入少量H2O2,溶液立即变为红色。
由此可知,白色沉淀中一定含有的离子为_______ (填离子符号)。探究过程中发现白色沉淀在空气中久置,最终变为红褐色。则该沉淀比Fe(OH)2_______ (填“难”或“易”)于被空气氧化。

请回答下列问题。
(1)若A、B、C为含有同种金属元素的化合物,D为强酸或强碱溶液,当D为强碱溶液时,写出A中阳离子的结构示意图
(2)若A、B、C的溶液均显碱性,C为焙制糕点的发酵粉的主要成分之一:
①D的电子式为
②除去B固体中混有的C固体的方法为
(3)若A为气体单质,D为一种黑色金属单质。
①反应Ⅲ的离子方程式为
②一定条件下,D能与水发生反应,该反应的化学方程式为
③将C与NaHCO3溶液混合产生白色沉淀且3 min后沉淀颜色不变。实验探究沉淀的组成。已知Fe(HCO3)2在水中不存在。
i.取少量白色沉淀充分洗涤,向其中加入稀硫酸,沉淀完全溶解,产生无色气泡。
ii.向i所得溶液中滴入KSCN溶液,溶液几乎不变红。
iii.向ii溶液中再滴入少量H2O2,溶液立即变为红色。
由此可知,白色沉淀中一定含有的离子为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D都是中学化学中常见物质。其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去)。根据题意回答下列问题:
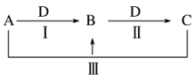
(1)若A、B、C的焰色反应均为黄色,C为食品工业中的一种应用广泛的疏松剂,D的过度排放会造成温室效应。
①A的化学式:____ ,B的俗名:___ 。
②反应II的离子方程式是____ 。
(2)若A、D均为单质,且A为气体,D元素的一种红棕色氧化物常用作颜料。
①反应II的离子方程式是____ 。
②反应III的离子方程式是___ 。
③设计实验方案检验B中阳离子___ 。

(1)若A、B、C的焰色反应均为黄色,C为食品工业中的一种应用广泛的疏松剂,D的过度排放会造成温室效应。
①A的化学式:
②反应II的离子方程式是
(2)若A、D均为单质,且A为气体,D元素的一种红棕色氧化物常用作颜料。
①反应II的离子方程式是
②反应III的离子方程式是
③设计实验方案检验B中阳离子
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知:粉末化合物A是红棕色,粉末单质B是金属单质
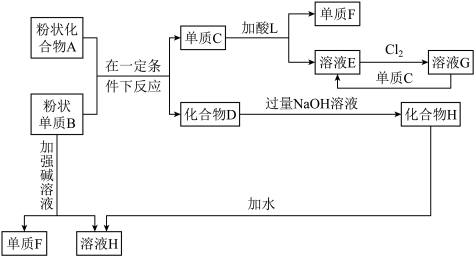
(1)溶液E加入氢氧化钠溶液的现象是___________ ; 产生此现象的原因为___________ (用化学反应方程式解释)
(2)写出下列反应的化学方程式: A+B→C+D___________ ;D→H:___________ 。
(3)写出下列反应的离子方程式: E+Cl2→G:___________ ; G+C→E:___________ ; B→F+H:___________ 。

(1)溶液E加入氢氧化钠溶液的现象是
(2)写出下列反应的化学方程式: A+B→C+D
(3)写出下列反应的离子方程式: E+Cl2→G:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A~G各物质间的关系如图,其中B、D为气态单质。
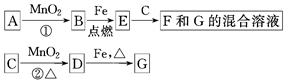
请回答下列问题。
(1)物质C和E的名称分别为_______ 、_______ ;
(2)可选用不同的A进行反应①,若能在常温下进行,其化学方程式为___________________ ;若只能在加热情况下进行,则反应物A应为_______ ;
(3)MnO2在反应①和反应②中的作用分别是_______ 、_______ ;
(4)新配制的F溶液应加入_______ 以防止其转化为G。检验G溶液中阳离子的常用试剂是_______ ,实验现象为_________________________________________ 。

请回答下列问题。
(1)物质C和E的名称分别为
(2)可选用不同的A进行反应①,若能在常温下进行,其化学方程式为
(3)MnO2在反应①和反应②中的作用分别是
(4)新配制的F溶液应加入
您最近一年使用:0次




