现有反应:
A.CaCO3 CaO+CO2↑ B.Zn+H2SO4=ZnSO4+H2↑
CaO+CO2↑ B.Zn+H2SO4=ZnSO4+H2↑
C.C+CO2 2CO D.2KOH+H2SO4=K2SO4+2H2O
2CO D.2KOH+H2SO4=K2SO4+2H2O
(1)上述四个反应中属于氧化还原反应且反应过程中能量变化符合如图的是_______ (填反应序号)。
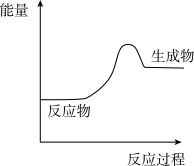
(2)在常温下,上述四个反应中可用于设计原电池的是_______ (填反应序号),根据该原电池回答下列问题:
①负极发生_______ (填“氧化”或“还原”)反应;正极的电极反应式为_______ 。
②当导线中有1 mol电子通过时,理论上发生的变化是_______ (填序号)。
a.溶液增重32.5 g b.溶液增重31.5 g c.析出1g H2 d.析出11.2LH2
(3)对于反应B,将足量且等量的形状相同的锌块分别加入到等浓度等体积的两份稀硫酸X、Y中,同时向X中加入少量饱和CuSO4溶液,发生反应生成氢气的体积(V)与时间(t)的关系如图所示。
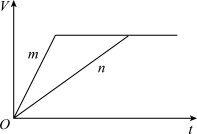
反应速率变快的原因是_______(填序号)。
A.CaCO3
 CaO+CO2↑ B.Zn+H2SO4=ZnSO4+H2↑
CaO+CO2↑ B.Zn+H2SO4=ZnSO4+H2↑C.C+CO2
 2CO D.2KOH+H2SO4=K2SO4+2H2O
2CO D.2KOH+H2SO4=K2SO4+2H2O(1)上述四个反应中属于氧化还原反应且反应过程中能量变化符合如图的是

(2)在常温下,上述四个反应中可用于设计原电池的是
①负极发生
②当导线中有1 mol电子通过时,理论上发生的变化是
a.溶液增重32.5 g b.溶液增重31.5 g c.析出1g H2 d.析出11.2LH2
(3)对于反应B,将足量且等量的形状相同的锌块分别加入到等浓度等体积的两份稀硫酸X、Y中,同时向X中加入少量饱和CuSO4溶液,发生反应生成氢气的体积(V)与时间(t)的关系如图所示。

反应速率变快的原因是_______(填序号)。
| A.CuSO4作催化剂 |
B.加入硫酸铜溶液增大了c( ) ) |
| C.Zn首先与Cu2+反应,生成的Cu与Zn、稀硫酸构成原电池 |
| D.加入硫酸铜溶液增大了溶液体积 |
更新时间:2023-01-04 14:02:03
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。阅读下列有关能源的材料,回答有关问题:
(1)从能量的角度看,断开化学键要___ ,形成化学键要___ 。
(2)焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时:
①2SO2(g)+O2(g) 2SO3(g)ΔH1=-197kJ/mol;
2SO3(g)ΔH1=-197kJ/mol;
②H2O(g)=H2O(l)ΔH2=-44kJ/mol;
③2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l)ΔH3=-545kJ/mol。
写出SO3(g)与H2O(l)反应的热化学方程式是____ 。
(3)已知一定条件下,CO(g)+H2O(g) CO2(g)+H2(g)反应过程能量变化如图所示,该反应为
CO2(g)+H2(g)反应过程能量变化如图所示,该反应为___ 反应(填“吸热”或“放热”)。
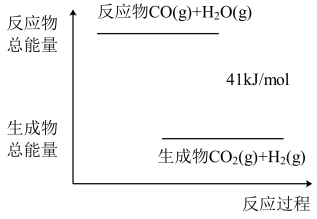
(4)已知热化学方程式:SO2(g)+ O2(g)
O2(g) SO3(g)ΔH=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为
SO3(g)ΔH=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为_____ 。
A.98.32kJ B.196.64kJ/mol C.<196.64kJ D.>196.64kJ
(1)从能量的角度看,断开化学键要
(2)焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时:
①2SO2(g)+O2(g)
 2SO3(g)ΔH1=-197kJ/mol;
2SO3(g)ΔH1=-197kJ/mol;②H2O(g)=H2O(l)ΔH2=-44kJ/mol;
③2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l)ΔH3=-545kJ/mol。
写出SO3(g)与H2O(l)反应的热化学方程式是
(3)已知一定条件下,CO(g)+H2O(g)
 CO2(g)+H2(g)反应过程能量变化如图所示,该反应为
CO2(g)+H2(g)反应过程能量变化如图所示,该反应为
(4)已知热化学方程式:SO2(g)+
 O2(g)
O2(g) SO3(g)ΔH=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为
SO3(g)ΔH=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为A.98.32kJ B.196.64kJ/mol C.<196.64kJ D.>196.64kJ
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用___________ (填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热饭盒”给人们生活带来方便,它可利用下面___________(填字母)反应释放的热量加热食物。
II.研究含碳、氮的物质间转化的热效应,在日常生活与工业生产中均有很重要的意义。
(3)已知:H2O(l)= H2O(g) △H= +44.0kJ·mol-1,甲烷完全燃烧与不完全燃烧的热效应如下图所示。
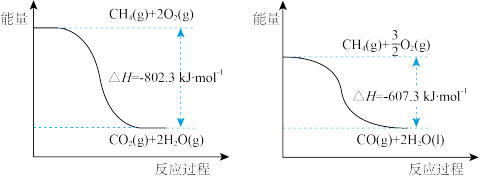
①写出表示甲烷燃烧热的热化学方程式:_____________________________ 。
②CO的燃烧热△H=_______ kJ·mol-1。
(4)以NH3、CO2为原料生产尿素[CONH2)2]的反应历程与能量变化示意图如下。
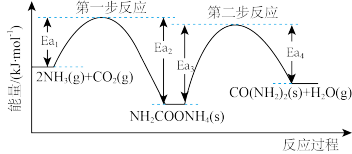
①第一步反应的热化学方程式为_______ 。
②第二步反应的△H_______ 0(填“>”、“<”或“=”)。
③从图象分析决定生产尿素的总反应的反应速率的步骤是第_______ 步反应。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用
(2)“即热饭盒”给人们生活带来方便,它可利用下面___________(填字母)反应释放的热量加热食物。
| A.生石灰和水 | B.浓硫酸和水 | C.纯碱和水 | D.食盐和白醋 |
II.研究含碳、氮的物质间转化的热效应,在日常生活与工业生产中均有很重要的意义。
(3)已知:H2O(l)= H2O(g) △H= +44.0kJ·mol-1,甲烷完全燃烧与不完全燃烧的热效应如下图所示。

①写出表示甲烷燃烧热的热化学方程式:
②CO的燃烧热△H=
(4)以NH3、CO2为原料生产尿素[CONH2)2]的反应历程与能量变化示意图如下。

①第一步反应的热化学方程式为
②第二步反应的△H
③从图象分析决定生产尿素的总反应的反应速率的步骤是第
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】化学能转化为电能的原理的发现和各式各样电池装置的发明,是贮能和功能技术的巨大进步。
回答下列问题:
(1)上图中C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为__________________ ,反应进行一段时间后溶液C的pH将___________ (填“升高”“降低”或“基本不变”)。
(2)若将反应Cu +2Ag+=2Ag +Cu2+按图1所示设计一个原电池装置,则负极A的材料为___________ ,溶液C为___________ ,当导线上有2.5mole-流过时,正极生成银的质量为________________ 。
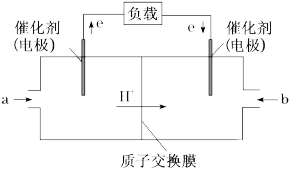
(3)下图为甲烷(CH4)燃料电池的构造示意图,d 电极是___________ (填“正极”或“负极”),C电极的反应方程式为___________________________ 。
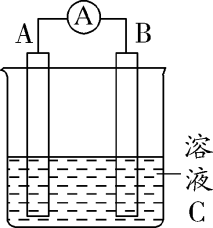
回答下列问题:
(1)上图中C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为
(2)若将反应Cu +2Ag+=2Ag +Cu2+按图1所示设计一个原电池装置,则负极A的材料为
(3)下图为甲烷(CH4)燃料电池的构造示意图,d 电极是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】依据原电池原理,回答下列问题:

如图是使用固体电解质的燃料电池,装置中,以稀土金属材料作惰性电极,在两极上分别通入 和空气,其中固体电解质是掺杂了
和空气,其中固体电解质是掺杂了 的
的 固体,它在高温下能传导正极生成的
固体,它在高温下能传导正极生成的 (
( )。
)。
(1)c电极为_______ (填“正”或“负”)极。
(2)d电极上的电极反应为_______ 。
(3)如果消耗 甲烷,假设化学能完全转化为电能,则转移电子的数目为
甲烷,假设化学能完全转化为电能,则转移电子的数目为_______ (用 表示),需要消耗标准状况下氧气的体积为
表示),需要消耗标准状况下氧气的体积为_______ L。

如图是使用固体电解质的燃料电池,装置中,以稀土金属材料作惰性电极,在两极上分别通入
 和空气,其中固体电解质是掺杂了
和空气,其中固体电解质是掺杂了 的
的 固体,它在高温下能传导正极生成的
固体,它在高温下能传导正极生成的 (
( )。
)。(1)c电极为
(2)d电极上的电极反应为
(3)如果消耗
 甲烷,假设化学能完全转化为电能,则转移电子的数目为
甲烷,假设化学能完全转化为电能,则转移电子的数目为 表示),需要消耗标准状况下氧气的体积为
表示),需要消耗标准状况下氧气的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】请根据化学反应与热能的有关知识,填写下列空白:
(1)下列反应中,属于吸热反应的是______ (填数字序号,下同),属于放热反应的是______ 。
①煅烧石灰石制生石灰②燃烧木炭取暖 ③炸药爆炸 ④酸碱中和反应⑤生石灰与水作用制熟石灰 ⑥食物因氧化而腐败
(2)已知H2和O2反应放热,且断开1molH-H、1molO=O、1molO-H键需吸收的能量分别为Q1kJ、Q2kJ、Q3kJ,由此可以推知下列关系正确的是______ (填字母编号)。
A. Q1+ Q2> Q3 B. 2Q1+ Q2<4 Q3 C. Q1+Q2>2Q3 D. 2Q1+Q2<2Q3
(3)用导线连接锌片、铜片后浸入稀硫酸溶液中,构成了原电池,工作一段时间后,锌片的质量减少了3.25g,此电池负极的电极反应式是______________ ,铜片表面析出了氢气____ L(标准状况)。
(1)下列反应中,属于吸热反应的是
①煅烧石灰石制生石灰②燃烧木炭取暖 ③炸药爆炸 ④酸碱中和反应⑤生石灰与水作用制熟石灰 ⑥食物因氧化而腐败
(2)已知H2和O2反应放热,且断开1molH-H、1molO=O、1molO-H键需吸收的能量分别为Q1kJ、Q2kJ、Q3kJ,由此可以推知下列关系正确的是
A. Q1+ Q2> Q3 B. 2Q1+ Q2<4 Q3 C. Q1+Q2>2Q3 D. 2Q1+Q2<2Q3
(3)用导线连接锌片、铜片后浸入稀硫酸溶液中,构成了原电池,工作一段时间后,锌片的质量减少了3.25g,此电池负极的电极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学电源在生产生活中有着广泛的应用,同学们常常通过设计实验和查阅资料的方式学习化学电源的相关知识。
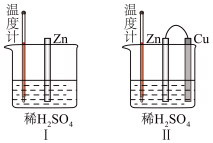
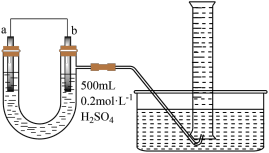
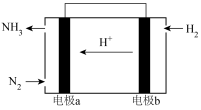
(1)甲同学为了解化学反应中的能量转化,设计了一组对比实验(实验装置如图Ⅰ和图Ⅱ)。预计产生气体的速率Ⅰ___________ Ⅱ(>、<或=),温度计的示数Ⅰ___________ II(>、<或=);___________ ,当量筒中收集到336mL(标准状况下)气体时,通过导线的电子的物质的量为___________ 。___________ 极(填“正”或“负”),若原料气H2中混有CO,单位体积原料气合成氨气的物质的量不变,只是在电极b附近需增设排气口,排出气体主要含有___________ 。
(1)甲同学为了解化学反应中的能量转化,设计了一组对比实验(实验装置如图Ⅰ和图Ⅱ)。预计产生气体的速率Ⅰ
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
(1)请完成此实验设计,其中:V1=________ ,V6=________ ,V9=________ ;
(2)反应一段时间后,实验A中的金属呈________ 色,实验E中的金属呈________ 色;
(3)该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因________________________ 。
实验 混合溶液 | A | B | C | D | E | F |
4 mol·L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
(1)请完成此实验设计,其中:V1=
(2)反应一段时间后,实验A中的金属呈
(3)该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某学生为了探究锌与盐酸反应过程中的速率变化,在 100 mL 稀盐酸中加入足量的锌粉,标准状况下测得数据累计值如下:
(1)在 0~1、1~2、2~3、3~4、4~5 min 各时间段中:反应速率最大的时间段是_______________ ; 在 0~5min 内,反应速率变化的原因是______________________________________________________________________________________
(2)在 2~3 min 时间段内,用盐酸的浓度变化表示的反应速率为_______________
(3)为了减缓反应速率但不减少产生气的量,在盐酸中分别加入等体积的下列液体:
A.蒸馏水 B.Na2SO4 溶液 C.NaOH 溶液 D.H2SO4 溶液 E.Na2CO3
你认为可行的是(填编号)_______________ 。
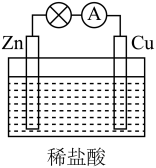
(4)为了加快锌和盐酸的反应,采用了如图的装置。
此装置中负极为_______________ ,写出正极的电极反应式______________ ;
若收集到标况下 2.24L 气体,转移了电子_______________________ mol,溶解了Zn______________ g.
时间(min) | 1 | 2 | 3 | 4 | 5 |
氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
(1)在 0~1、1~2、2~3、3~4、4~5 min 各时间段中:反应速率最大的时间段是
(2)在 2~3 min 时间段内,用盐酸的浓度变化表示的反应速率为
(3)为了减缓反应速率但不减少产生气的量,在盐酸中分别加入等体积的下列液体:
A.蒸馏水 B.Na2SO4 溶液 C.NaOH 溶液 D.H2SO4 溶液 E.Na2CO3
你认为可行的是(填编号)
(4)为了加快锌和盐酸的反应,采用了如图的装置。

此装置中负极为
若收集到标况下 2.24L 气体,转移了电子
您最近一年使用:0次

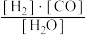 ,写出它所对应反应的化学方程式:
,写出它所对应反应的化学方程式:

