新冠疫情的发生,消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一,而氯气是制取消毒液的重要原料之一。
请回答下列问题:
(1)请写出舍勒发现氯气的化学反应方程式___________________________________ ,若收集到标准状况下3.36LCl2,则被氧化的HCl的物质的量为_____________ mol。
(2)84消毒液(主要成分是NaClO)是常用的消毒剂,工业上将氯气通入烧碱溶液中制取84消毒液,写出此反应的离子方程式_______________________________________ ,若要制取1.5L 2 mol/L的84消毒液,则需要标准状况下___________ L 氯气。
(3)新冠疫情下,人们对杀菌消毒特别重视,曾有报道某居民将84消毒液与洁厕灵(主要成分是浓盐酸)混合使用而中毒,请解释原因__________________________________ (用化学方程式表示), 该反应中氧化剂是______________ 。
请回答下列问题:
(1)请写出舍勒发现氯气的化学反应方程式
(2)84消毒液(主要成分是NaClO)是常用的消毒剂,工业上将氯气通入烧碱溶液中制取84消毒液,写出此反应的离子方程式
(3)新冠疫情下,人们对杀菌消毒特别重视,曾有报道某居民将84消毒液与洁厕灵(主要成分是浓盐酸)混合使用而中毒,请解释原因
更新时间:2022-12-21 16:02:21
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】12.5g CuSO4﹒5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。

请回答下列问题:
(1)试确定200℃时固体物质的化学式___________ 。
(2)取270℃所得样品,于570℃灼烧得到的主要产物是黑色粉末和一种氧化性气体,该反应的化学方程式为___________ 。把该黑色粉末溶解于稀硫酸中,经浓缩、冷却,有蓝色晶体析出,该晶体的化学式为___________ ,其存在的最高温度是___________ 。
(3)若在0.05mol·L-1 硫酸铜溶液中通入足量 H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的pH值约为___________ 。

请回答下列问题:
(1)试确定200℃时固体物质的化学式
(2)取270℃所得样品,于570℃灼烧得到的主要产物是黑色粉末和一种氧化性气体,该反应的化学方程式为
(3)若在0.05mol·L-1 硫酸铜溶液中通入足量 H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的pH值约为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】如图是氮元素的几种价态与物质类别的对应关系。请回答下列问题:
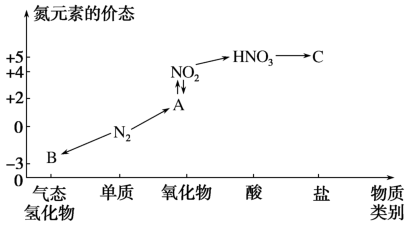
(1)写出N2的一种用途:___________ 。
(2)B物质的电子式为:___________ 。
(3)HNO3与图中的物质C常用于检验Cl-的存在,则C的化学式为___________ 。
(4)实验室制取物质B的化学方程式为___________ 。
(5)浓硝酸与木炭在加热条件下反应的化学方程式为___________ 。
(6)如图装置可用于探究氯气与氨气的反应。实验时先通过三颈瓶瓶口 1 通入氨气,然后关闭 b 活塞,再通过瓶口 2 通入氯气。
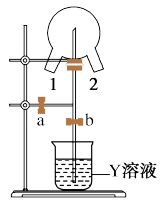
①实验中三颈瓶内出现白烟并在内壁凝结成固体,发生反应的化学方程式为___________ 。
② 实验完毕后,观察到三颈瓶内还有黄绿色气体, 简述如何处理才能不污染环境___________ 。
(7)将3.2 g铜与60.0 mL一定浓度的硝酸发生反应,铜完全溶解,产生NO2和NO混合气体的体积为8.96 L(标况)。待产生的气体全部释放后,向溶液加入100 mL 2.0 mol/L 的 NaOH 溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为___________ mol/L。

(1)写出N2的一种用途:
(2)B物质的电子式为:
(3)HNO3与图中的物质C常用于检验Cl-的存在,则C的化学式为
(4)实验室制取物质B的化学方程式为
(5)浓硝酸与木炭在加热条件下反应的化学方程式为
(6)如图装置可用于探究氯气与氨气的反应。实验时先通过三颈瓶瓶口 1 通入氨气,然后关闭 b 活塞,再通过瓶口 2 通入氯气。

①实验中三颈瓶内出现白烟并在内壁凝结成固体,发生反应的化学方程式为
② 实验完毕后,观察到三颈瓶内还有黄绿色气体, 简述如何处理才能不污染环境
(7)将3.2 g铜与60.0 mL一定浓度的硝酸发生反应,铜完全溶解,产生NO2和NO混合气体的体积为8.96 L(标况)。待产生的气体全部释放后,向溶液加入100 mL 2.0 mol/L 的 NaOH 溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为
您最近一年使用:0次
【推荐1】高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钾的主要反应为: ,
,
①该反应中的还原剂是__________ ,每生成1molNa2FeO4转移___________ mol电子。
②简要说明K2FeO4作为水处理剂时所起的作用:_________________ 。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、 、
、 、
、 、
、 、H2O。
、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式:_______________ 。
②低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),说明什么问题?__________ 。
(3)焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质: NH4Cl、FeCl3、N2、Fe2O3、Fe和X。
①根据题意,可判断出X是_____________ (写化学式)。
②写出并配平该反应的化学方程式_______________
(1)干法制备高铁酸钾的主要反应为:
 ,
,①该反应中的还原剂是
②简要说明K2FeO4作为水处理剂时所起的作用:
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、
 、
、 、
、 、
、 、H2O。
、H2O。①写出并配平湿法制高铁酸钾的离子反应方程式:
②低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),说明什么问题?
(3)焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质: NH4Cl、FeCl3、N2、Fe2O3、Fe和X。
①根据题意,可判断出X是
②写出并配平该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】物质的类别和核心元素的化合价是研究物质化学性质的两个重要角度。硫元素的价类二维图如图所示(其中h、g的阳离子均为 ),请回答下列问题:
),请回答下列问题:

(1)e的化学式是___________ 。
(2)实验室常用g和f的浓溶液制备气体c,写出其化学方程式___________ 。
(3)将气体c通入a的水溶液,溶液变浑浊,用化学方程式解释___________ ,体现了c的___________ 性。
(4)过量的铜与f的浓溶液在加热条件下可以发生,化学方程式为___________ ,反应后铜片有剩余,为使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如 溶液),则该反应的离子方程式为
溶液),则该反应的离子方程式为___________ 。
 ),请回答下列问题:
),请回答下列问题:
(1)e的化学式是
(2)实验室常用g和f的浓溶液制备气体c,写出其化学方程式
(3)将气体c通入a的水溶液,溶液变浑浊,用化学方程式解释
(4)过量的铜与f的浓溶液在加热条件下可以发生,化学方程式为
 溶液),则该反应的离子方程式为
溶液),则该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问题。
(1)湿法制备高铁酸钾的反应体系有六种微粒: 。
。
①在碱性条件下,湿法生产高铁酸钾的离子反应方程式是______ 。
②若反应过程中转移了0.6mol电子,则还原产物的物质的量为______ mol。
③高铁酸钾作为一种理想的水处理剂,其处理水的原理______
(2)铁明矾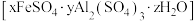 常用于制备高效复合型高效混凝剂。其组成通过下列实验测定。
常用于制备高效复合型高效混凝剂。其组成通过下列实验测定。
①称取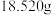 样品,准确配成100mL溶液A。
样品,准确配成100mL溶液A。
②量取 溶液A,加入盐酸酸化的
溶液A,加入盐酸酸化的 溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固
溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固
体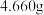 。
。
③再量取 溶液A,滴加适量稀硫酸,用
溶液A,滴加适量稀硫酸,用 溶液滴定至终点,生成
溶液滴定至终点,生成 ,消耗
,消耗 溶液
溶液 。
。
(已知 、
、 的相对分子质量分别是152、342)
的相对分子质量分别是152、342)
①在25.00mL试样中,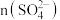
______ mol,
______ mol。
②铁明矾的化学式为______ (写出详细的解题步骤)
(1)湿法制备高铁酸钾的反应体系有六种微粒:
 。
。①在碱性条件下,湿法生产高铁酸钾的离子反应方程式是
②若反应过程中转移了0.6mol电子,则还原产物的物质的量为
③高铁酸钾作为一种理想的水处理剂,其处理水的原理
(2)铁明矾
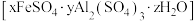 常用于制备高效复合型高效混凝剂。其组成通过下列实验测定。
常用于制备高效复合型高效混凝剂。其组成通过下列实验测定。①称取
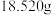 样品,准确配成100mL溶液A。
样品,准确配成100mL溶液A。②量取
 溶液A,加入盐酸酸化的
溶液A,加入盐酸酸化的 溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固
溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固体
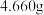 。
。③再量取
 溶液A,滴加适量稀硫酸,用
溶液A,滴加适量稀硫酸,用 溶液滴定至终点,生成
溶液滴定至终点,生成 ,消耗
,消耗 溶液
溶液 。
。(已知
 、
、 的相对分子质量分别是152、342)
的相对分子质量分别是152、342)①在25.00mL试样中,
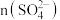

②铁明矾的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。是目前国际上公认的新一代高效、广谱、安全的杀菌、保鲜剂,在水处理等方面有广泛应用的高效安全消毒剂。与Cl2相比ClO2不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
(1)实验室用二氧化锰制备氯气的化学方程式为____ ,氯气和水反应的离子方程式为____ 。
(2)在ClO2的制备方法中,比较实用的有数十种,实验室常用氯酸钠(NaClO3)、亚硫酸钠(Na2SO3)和硫酸共热制备二氧化氯,此化学反应方程式为____ 。
(3)我国最近成功研制出制取ClO2的新方法,其反应的微观过程如图所示:
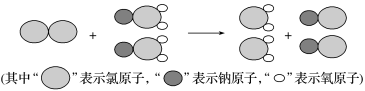
该反应的化学方程式为____ 。
(4)含氯消毒剂的消毒能力可以用氧化性来衡量。每克ClO2的氧化能力相当于____ 克Cl2的氧化能力。(计算结果保留两位小数)
(1)实验室用二氧化锰制备氯气的化学方程式为
(2)在ClO2的制备方法中,比较实用的有数十种,实验室常用氯酸钠(NaClO3)、亚硫酸钠(Na2SO3)和硫酸共热制备二氧化氯,此化学反应方程式为
(3)我国最近成功研制出制取ClO2的新方法,其反应的微观过程如图所示:

该反应的化学方程式为
(4)含氯消毒剂的消毒能力可以用氧化性来衡量。每克ClO2的氧化能力相当于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养。
(1)在实验室中用浓盐酸与MnO2制取Cl2
①写出反应的离子方程式:_____ 。
②下列收集Cl2的正确装置是_____ 。
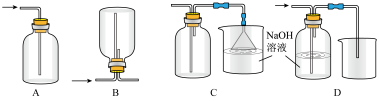
③将Cl2通入水中,所得溶液中具有氧化性的含氯粒子是_____ 。
④若产生标准状况下4.48LCl2,转移的电子数是_____ ,被氧化的HCl的物质的量是:_____ 。
(2)请设计实验证明Fe2+具有还原性:_____ 。
限选试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片。
(3)NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等。“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。NaClO2的有效氯含量为_____ 。(计算结果保留两位小数)
(1)在实验室中用浓盐酸与MnO2制取Cl2
①写出反应的离子方程式:
②下列收集Cl2的正确装置是

③将Cl2通入水中,所得溶液中具有氧化性的含氯粒子是
④若产生标准状况下4.48LCl2,转移的电子数是
(2)请设计实验证明Fe2+具有还原性:
限选试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片。
(3)NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等。“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。NaClO2的有效氯含量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】请回答下列问题:
(1)2 mol的CO2与3 mol的SO3的分子数比是_______ ;原子数比是_______ 。
(2)9.5 g某二价金属氯化物(ACl2)中含有0.2 molCl-,则A的摩尔质量是___________ 。
(3)铁与蒸汽反应的化学方程式_____________________________________ ;
(4)实验室以二氧化锰为原料制氯气的离子方程式____________________________________ 。
(5)中国的瓷器驰名世界,制备陶瓷是以粘土[主要成分Al2Si2O5(OH)4]为原料,经高温烧结而成.若以氧化物形式表示粘土的组成,应写为_________________________ 。
(1)2 mol的CO2与3 mol的SO3的分子数比是
(2)9.5 g某二价金属氯化物(ACl2)中含有0.2 molCl-,则A的摩尔质量是
(3)铁与蒸汽反应的化学方程式
(4)实验室以二氧化锰为原料制氯气的离子方程式
(5)中国的瓷器驰名世界,制备陶瓷是以粘土[主要成分Al2Si2O5(OH)4]为原料,经高温烧结而成.若以氧化物形式表示粘土的组成,应写为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】实验室利用下图装置制备溴苯和硫酸锰。已知反应原理为MnO2 + 2NaBr + 2H2SO4 MnSO4+Na2SO4 +Br2↑+2H2O
MnSO4+Na2SO4 +Br2↑+2H2O
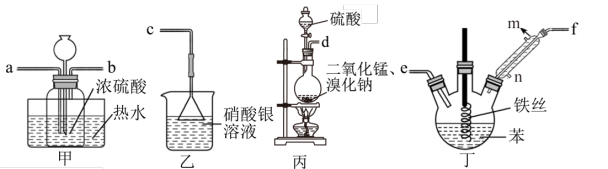
反应结束后,装置丁中液体因溶解了Br2而呈棕褐色,请用离子方程式表示洗去Br2的方法___________ ,干燥之后分离出产物溴苯的方法为___________ 。
 MnSO4+Na2SO4 +Br2↑+2H2O
MnSO4+Na2SO4 +Br2↑+2H2O
反应结束后,装置丁中液体因溶解了Br2而呈棕褐色,请用离子方程式表示洗去Br2的方法
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)化学与生产生活联系密切,请书写对应的化学方程式:
①漂白粉中的 能与空气中的
能与空气中的 和水蒸气发生反应:
和水蒸气发生反应:_________________________ 。
②固体管道疏通剂(主要成分有氢氧化钠和铝粉)的疏通原理:__________________________ 。
③常温下,将氯气通入氢氧化钠溶液中,可以得到一种漂白液:__________________________ 。
(2)海水开发利用的部分过程如图所示:
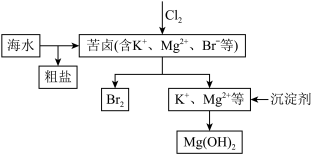
④向苦卤中通入氯气,发生反应的离子方程式是_____________________________________
⑤工业生产中常选用石灰乳作为沉淀剂,相关反应的离子方程式是______________________
⑥富集溴一般先用空气和水蒸气吹出单质溴,再用 将其还原吸收,相关反应的化学方程式是
将其还原吸收,相关反应的化学方程式是_______ 。
(1)化学与生产生活联系密切,请书写对应的化学方程式:
①漂白粉中的
 能与空气中的
能与空气中的 和水蒸气发生反应:
和水蒸气发生反应:②固体管道疏通剂(主要成分有氢氧化钠和铝粉)的疏通原理:
③常温下,将氯气通入氢氧化钠溶液中,可以得到一种漂白液:
(2)海水开发利用的部分过程如图所示:

④向苦卤中通入氯气,发生反应的离子方程式是
⑤工业生产中常选用石灰乳作为沉淀剂,相关反应的离子方程式是
⑥富集溴一般先用空气和水蒸气吹出单质溴,再用
 将其还原吸收,相关反应的化学方程式是
将其还原吸收,相关反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,反应的化学方程式_____________ 漂白粉的有效成分是__________ (填化学式)。
(2)实验室制取氨气的化学方程式:__________________________________
(3)1.2gRSO4中含0.01molR2+,则RSO4的摩尔质量是______________ ;
(4)实验室制Fe(OH)2一般看不到白色的Fe(OH)2沉淀,原因___________________ 现象是:_________________________ 。反应的化学方程式:__________________________________
(5)碳酸钠水解反应的离子方程式(第一步):_________________________ 。
(6)铅蓄电池的负极反应式:_________________________ 。
(7)硫酸钡的沉淀溶解平衡:__________________________________ 。
(2)实验室制取氨气的化学方程式:
(3)1.2gRSO4中含0.01molR2+,则RSO4的摩尔质量是
(4)实验室制Fe(OH)2一般看不到白色的Fe(OH)2沉淀,原因
(5)碳酸钠水解反应的离子方程式(第一步):
(6)铅蓄电池的负极反应式:
(7)硫酸钡的沉淀溶解平衡:
您最近一年使用:0次



