某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为 、
、 、
、 ,不考虑其他杂质)制备七水合硫酸亚铁(
,不考虑其他杂质)制备七水合硫酸亚铁( ),设计了如下流程:
),设计了如下流程:
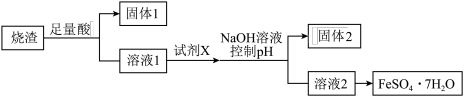
已知① 与酸不反应;②氢氧化铝能与
与酸不反应;②氢氧化铝能与 溶液反应生成偏铝酸钠溶液。
溶液反应生成偏铝酸钠溶液。
下列说法不正确的是
 、
、 、
、 ,不考虑其他杂质)制备七水合硫酸亚铁(
,不考虑其他杂质)制备七水合硫酸亚铁( ),设计了如下流程:
),设计了如下流程:
已知①
 与酸不反应;②氢氧化铝能与
与酸不反应;②氢氧化铝能与 溶液反应生成偏铝酸钠溶液。
溶液反应生成偏铝酸钠溶液。下列说法不正确的是

A.溶解烧渣选用足量硫酸,试剂 选用铁粉 选用铁粉 |
B.固体 中一定有 中一定有 ,加 ,加 溶液控制 溶液控制 是为了使 是为了使 转化为 转化为 进入固体 进入固体 |
C.从溶液 得到 得到 产品的过程中,须控制条件防止其氧化和分解 产品的过程中,须控制条件防止其氧化和分解 |
D.若改变方案,在溶液 中直接加 中直接加 至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到 至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到 |
更新时间:2022-12-23 20:01:37
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】以高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下,下列说法不正确 的是


| A.焙烧时产生的SO2气体可以用NaOH溶液吸收 |
| B.滤液中的铝元素主要以AlO2-存在,可以往滤液中通入过量二氧化碳,经过滤、灼烧生产氧化铝 |
| C.可以将少量Fe3O4产品溶于稀硫酸中,再滴入酸性高锰酸钾溶液,若溶液褪色则证明产品中含有FeO |
| D. Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,理论上完全反应消耗的n(FeS2):n(Fe2O3)=1:16 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某工厂冶炼钛精矿得到钛渣,钛渣的成分及含量(质量分数)为:TiO251.00%、Al2O319.34%、MgO7.20%、CaO4.00%、SiO218.46%,通过下列工艺流程可以得到纳米二氧化钛和某型分子筛(化学式为Na4Al4Si4O16 •9H2O)。

下列说法不正确的是

下列说法不正确的是
| A.钛渣中的TiO2、SiO2不属于碱性氧化物 |
| B.滤液①中溶质只有NaAlO2、NaOH |
C.步骤②中加入盐酸时,反应的离子方程式是Na2TiO3 + 2H+ H2TiO3↓+2Na+ H2TiO3↓+2Na+ |
D.步骤③中加入适量Na2SiO3时,反应的化学方程式为:4NaAlO2 + 4Na2SiO3 +13H2O  Na4Al4Si4O16 •9H2O↓ + 8NaOH Na4Al4Si4O16 •9H2O↓ + 8NaOH |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列为除去括号内的杂质而选用的试剂不正确的是
A.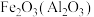 : : 溶液 溶液 | B.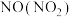 :水 :水 |
C. 溶液 溶液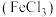 :铁粉 :铁粉 | D.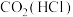 :饱和 :饱和 溶液 溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断错误的是( )
| A.加入KSCN溶液一定不变红色 | B.溶液中一定含Cu2+ |
| C.溶液中一定含Fe2+ | D.剩余固体中一定含铜 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】聚合氯化铝铁[AlFe(OH)nCl6-n]m用于生活给水及工业给水的净化处理。以工业废料(Fe、Al、FeO、Fe2O3、Al2O3)为原料生产该产品的流程如下,下列说法错误的是
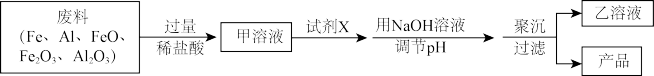
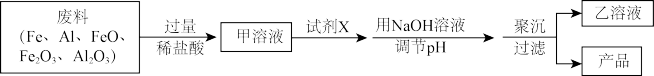
| A.产品中铁元素的化合价为+3 |
| B.甲溶液中一定存在的阳离子有H+、Al3+、Fe2+、Fe3+ |
| C.试剂X可以用H2O2,目的是将Fe2+氧化为Fe3+ |
| D.乙溶液呈酸性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在给定条件下,下列选项所示的物质间转化均能实现的是( )
A.Fe3O4(s)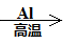 Fe(s) Fe(s)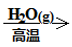 Fe2O3 Fe2O3 |
B.NH4HCO3(s)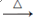 NH3(g) NH3(g) NO2(g) NO2(g) |
C.S(s)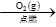 SO3(g) SO3(g)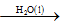 H2SO4(aq) H2SO4(aq) |
D.NaHCO3(s)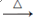 Na2CO3(s) Na2CO3(s)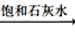 NaOH(aq) NaOH(aq) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验现象对应结论一定正确的是
| A.向浓硝酸中加红热木炭,观察到红棕色气体,能说明浓硝酸被木炭还原成了NO2 |
| B.向碘化亚铁溶液中加入少量氯水,溶液变黄,能说明还原性I->Fe2+ |
| C.用水直接吸收SO3易形成大量酸雾,能说明SO3和水反应放出大量热 |
| D.向铁和高温水蒸气反应后的产物中加入稀硫酸,再加入K3[Fe(CN)6]溶液,产生蓝色沉淀,能说明产物中含二价铁 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某溶液中含如下离子组中的几种K+、Fe3+、Fe2+、Cl-、CO32-、NO3-、SO42-、SiO32-、I-,某同学欲探究该溶液的组成进行了如下实验:
Ⅰ.用铂丝醮取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,此时溶液颜色加深,但无沉淀生成
Ⅲ.取Ⅱ反应后溶液分别置于两支试管中,第一支试管中加入BaCl2溶液有白色沉淀生成,再滴加KSCN溶液,上层清液变红,第二支试管加入CCl4,充分振荡静置后溶液分层,下层为无色。
下列说法正确的是( )
Ⅰ.用铂丝醮取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,此时溶液颜色加深,但无沉淀生成
Ⅲ.取Ⅱ反应后溶液分别置于两支试管中,第一支试管中加入BaCl2溶液有白色沉淀生成,再滴加KSCN溶液,上层清液变红,第二支试管加入CCl4,充分振荡静置后溶液分层,下层为无色。
下列说法正确的是( )
| A.原溶液中肯定不含Fe2+、NO3-、SiO32-、I- |
| B.原溶液中肯定含有K+、Fe3+、Fe2+、NO3-、SO42- |
| C.步骤Ⅱ中无色气体是NO气体,无CO2气体产生 |
| D.为确定是否含有Cl-可取原溶液加入过量硝酸银溶液,观察是否产生白色沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】为了探究铁及其化合物的氧化性和还原性,某同学设计如下实验方案,其中符合实验要求且正确的是
| 选项 | 实验操作 | 实验现象 | 离子反应 |
| A | 在氯化亚铁溶液中滴加新制氯水 | 浅绿色溶液变成棕黄色溶液 | 2Fe2++Cl2=2Fe3++2Cl- |
| B | 在氯化亚铁溶液中加入锌片 | 浅绿色溶液变成无色溶液 | Fe2++Zn=Fe+Zn2+ |
| C | 在氯化铁溶液中加入铁粉 | 棕黄色溶液变成浅绿色溶液 | Fe3++Fe=2Fe2+ |
| D | 在氯化铁溶液中加入铜粉 | 棕黄色溶液变成蓝色溶液 | 2Fe3++Cu=2Fe2++Cu2+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次


 )产生废液X进行回收处理,流程如图所示,下列说法不正确的是
)产生废液X进行回收处理,流程如图所示,下列说法不正确的是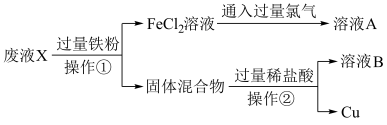
 与Cu完全反应,转移电子数约为
与Cu完全反应,转移电子数约为


 +6H+= 6Fe3++Cl-+3H2O
+6H+= 6Fe3++Cl-+3H2O

