硒是动物和人体所必需的微量元素之一,也是一种重要的工业原料。硒在自然界中稀少而分散,常从精炼铜的阳极泥中提取硒。
(1)粗铜精炼时,通常用精铜作___________ 极(填“阴”或“阳”)。
(2)Se与 处于同一主族,比
处于同一主族,比 原子多1个电子层,Se的原子序数为
原子多1个电子层,Se的原子序数为___________ ,最高价氧化物的化学式为___________ 。
(3)阳极泥中的硒主要以Se和CuSe的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:
i、将含硒阳极泥与浓硫酸混合焙烧,产生 的混合气体;
的混合气体;
ii、用水吸收i中混合气体,可得Se固体。
①请写出 与浓
与浓 反应的化学方程式
反应的化学方程式___________ 。
②焙烧过程产生的烟气中含有少量 ,可用
,可用 溶液吸收,二者反应生成一种盐,该盐的化学式为
溶液吸收,二者反应生成一种盐,该盐的化学式为___________ 。
③写出步骤ii中的化学方程式___________ 。
(1)粗铜精炼时,通常用精铜作
(2)Se与
 处于同一主族,比
处于同一主族,比 原子多1个电子层,Se的原子序数为
原子多1个电子层,Se的原子序数为(3)阳极泥中的硒主要以Se和CuSe的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:
i、将含硒阳极泥与浓硫酸混合焙烧,产生
 的混合气体;
的混合气体;ii、用水吸收i中混合气体,可得Se固体。
①请写出
 与浓
与浓 反应的化学方程式
反应的化学方程式②焙烧过程产生的烟气中含有少量
 ,可用
,可用 溶液吸收,二者反应生成一种盐,该盐的化学式为
溶液吸收,二者反应生成一种盐,该盐的化学式为③写出步骤ii中的化学方程式
更新时间:2022-12-22 16:58:15
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。实验室可通过以下反应制得:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O,回答下列问题:
(1)该反应中还原产物的化学式是______ ,被氧化的元素是______ (填元素符号)。
(2)用双线桥标出上述反应的电子转移情况______ 。
(3)若反应共产生了8.96L(标准状况)气体,则反应转移的电子的物质的量为______ mol,消耗还原剂的物质的量为______ mol。
(4)标准状况下44.8mL的ClO2恰好能与50mL0.1mol•L-1的Na2SO3溶液完全反应,得到的产物之一为Na2SO4,氯元素在产物中的化合价为______ ,此过程说明ClO2具有______ (填“氧化”或“还原”)性。
(5)在硫化钠溶液中通入ClO2可发生如下反应,请完成配平:______ 。
ClO2+ S2- H2O= Cl-+ SO H+
H+
(1)该反应中还原产物的化学式是
(2)用双线桥标出上述反应的电子转移情况
(3)若反应共产生了8.96L(标准状况)气体,则反应转移的电子的物质的量为
(4)标准状况下44.8mL的ClO2恰好能与50mL0.1mol•L-1的Na2SO3溶液完全反应,得到的产物之一为Na2SO4,氯元素在产物中的化合价为
(5)在硫化钠溶液中通入ClO2可发生如下反应,请完成配平:
ClO2+ S2- H2O= Cl-+ SO
 H+
H+
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2 溶液反应的化学方程式:_____________________________________________________________________________ 。
(2)①PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为_______________________________________ 。
②PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为_______________________________________________________________ 。
(3) Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42-,常用作脱氯剂,该反应的离子方程式为___________________________________________________ 。
(2)①PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为
②PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为
(3) Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42-,常用作脱氯剂,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】实验室可用KMnO4和浓盐酸反应制取氯气:KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平)
(1)配平化学方程式,并用单线桥标出电子转移的方向和数目。________ 。
(2)将上述配平的化学方程式改写为离子方程式________ 。
(3)浓盐酸在反应中显示出来的性质是________ 。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(4)若产生0.5mol Cl2,则被氧化的HCl____ mol,转移的电子的数目约为____ 。
(1)配平化学方程式,并用单线桥标出电子转移的方向和数目。
(2)将上述配平的化学方程式改写为离子方程式
(3)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(4)若产生0.5mol Cl2,则被氧化的HCl
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一氧化还原反应的体系中,共有KCl、Cl2、浓H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质。
(1)写出一个包含上述七种物质的氧化还原反应方程式,配平并标出电子转移方向和数目:_____________________________________________________________ 。
(2)上述反应中,还原剂是______________ ,还原产物是________________ 。
(3)在反应后的溶液中加入NaBiO3(不溶于冷水),溶液又变为紫红色,BiO3-反应后变为无色的Bi3+。写出该实验中涉及反应的离子反应方程式:________________________ 。
(4)根据以上实验,写出两个反应中氧化剂、氧化产物的氧化性强弱顺序_____________ 。
(1)写出一个包含上述七种物质的氧化还原反应方程式,配平并标出电子转移方向和数目:
(2)上述反应中,还原剂是
(3)在反应后的溶液中加入NaBiO3(不溶于冷水),溶液又变为紫红色,BiO3-反应后变为无色的Bi3+。写出该实验中涉及反应的离子反应方程式:
(4)根据以上实验,写出两个反应中氧化剂、氧化产物的氧化性强弱顺序
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.(1)①H2 + CuO  Cu + H2O
Cu + H2O
②CaCO3 + 2HCl = CaCl2 + CO2↑ + H2O
③3S + 6NaOH 2Na2S + Na2SO3 + 3H2O
2Na2S + Na2SO3 + 3H2O
④NH4NO3 + Zn = ZnO + N2↑+ 2H2O
⑤Cu2O + 4HCl = 2HCuCl2 + H2O
上述反应中,属于氧化还原反应的是__________________________ (填序号)
(2)SeO2、KI和HNO3可发生反应:SeO2+KI+HNO3→Se+I2+KNO3+H2O,配平该反应的化学方程式并用双线桥法标出电子转移的方向和数目:____________________________ 。
(3)在反应 KIO3 + 6HI = 3I2 + KI + 3H2O中,氧化剂与还原剂的物质的量之比为__________ 。
Ⅱ.已知:
① 2H2O + Cl2 + SO2 = H2SO4 + 2HCl ② 2KMnO4 + 16HCl = 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
(4)根据以上两个反应可以得出氧化剂和还原剂的强弱顺序,请写出由KMnO4、K2SO4 、MnSO4 、SO2、H2O、H2SO4 这六种物质组成的氧化还原反应的方程式并配平:_______________________ 。
在反应②中,若有18.25g HCl被氧化,求:
(5)转移的电子数为:_______________ 。
(6)标况下生成Cl2的体积(请列式计算)_______ 。
 Cu + H2O
Cu + H2O ②CaCO3 + 2HCl = CaCl2 + CO2↑ + H2O
③3S + 6NaOH
 2Na2S + Na2SO3 + 3H2O
2Na2S + Na2SO3 + 3H2O ④NH4NO3 + Zn = ZnO + N2↑+ 2H2O
⑤Cu2O + 4HCl = 2HCuCl2 + H2O
上述反应中,属于氧化还原反应的是
(2)SeO2、KI和HNO3可发生反应:SeO2+KI+HNO3→Se+I2+KNO3+H2O,配平该反应的化学方程式并用双线桥法标出电子转移的方向和数目:
(3)在反应 KIO3 + 6HI = 3I2 + KI + 3H2O中,氧化剂与还原剂的物质的量之比为
Ⅱ.已知:
① 2H2O + Cl2 + SO2 = H2SO4 + 2HCl ② 2KMnO4 + 16HCl = 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
(4)根据以上两个反应可以得出氧化剂和还原剂的强弱顺序,请写出由KMnO4、K2SO4 、MnSO4 、SO2、H2O、H2SO4 这六种物质组成的氧化还原反应的方程式并配平:
在反应②中,若有18.25g HCl被氧化,求:
(5)转移的电子数为:
(6)标况下生成Cl2的体积(请列式计算)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】电解原理在化学工业中有广泛应用。图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式是___________ 。在X极附近观察到的现象是_________________ 。
②Y电极上的电极反应式是______________ , 当阴极产生标况下2.24L气体时,阳极产物的质量是_____ g。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是___________________ ,电极反应式是____________________
②Y电极的材料是___________________ ,电极反应式是____________________

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式是
②Y电极上的电极反应式是
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是
②Y电极的材料是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】电解原理在化学工业中有广泛的应用。如图表示一个电解池,装有电解液a,X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
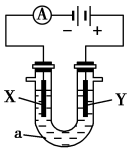
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为___________ ,在X极附近观察到的现象是___________ 。
②Y电极上的电极反应式为___________ 。
(2)如要用电解方法精炼粗铜,则:电解液a选用_______ ,X电极的材料是________ ,Y电极的材料是________ 。
(3)某新型可充电电池,能长时间保持稳定的放电电压,该电池的总反应如下:
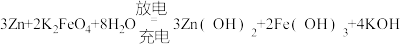 。
。
①放电时负极反应式为___________ ;
②充电时 发生
发生___________ 反应;(填“氧化”或“还原”)
③放电时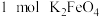 发生反应,转移电子数是
发生反应,转移电子数是___________ 。

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为
②Y电极上的电极反应式为
(2)如要用电解方法精炼粗铜,则:电解液a选用
(3)某新型可充电电池,能长时间保持稳定的放电电压,该电池的总反应如下:
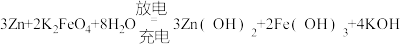 。
。①放电时负极反应式为
②充电时
 发生
发生③放电时
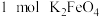 发生反应,转移电子数是
发生反应,转移电子数是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】把与下列元素有关性质相符的曲线标号填入相应空格中:

(1)第ⅢA族元素的最外层电子数:___________ 。
(2)第三周期元素的最高正化合价:___________ 。
(3)碱金属单质的熔点:___________ 。
(4)第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径:___________ 。

(1)第ⅢA族元素的最外层电子数:
(2)第三周期元素的最高正化合价:
(3)碱金属单质的熔点:
(4)第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】比较下列粒子的半径大小
①Na Mg O F___________________
②Na+ Mg2+ O2- F-___________________
③ Na+ Mg2+ S2- Cl-___________________
①Na Mg O F
②Na+ Mg2+ O2- F-
③ Na+ Mg2+ S2- Cl-
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】元素周期表是指导我们系统学习化学的重要工具。(答案都填写化学式)
(1)如图是铁元素在元素周期表中的有关信息。

写出Fe的原子结构示意图__ ,自然界中存在的54Fe和56Fe,它们互称为___ 。将铁片放入冷浓硫酸中,片刻后将铁片移入硫酸铜溶液中,发现铁片表面无明显变化,原因是__ 。通常证明某溶液中含Fe2+的化学方法是___ 。
下表是元素周期表的一部分:

(2)从原子结构角度分析,C、N、O、F四种元素处于同一行,是由于它们的__ 相同。处于同一列的N和P位于元素周期表的__ 族。
(3)通过元素周期表,我们可以知道:
①氮元素的最低化合价为_ ,其气态氢化物的结构式为__ 。
②与硅元素处于同一周期,两性金属元素是__ ,并写出其在元素周期表中的位置:第__ 周期,__ 族,该元素的最高价氧化物对应水化物的电离方程式为__ 。
③第三周期半径最大的金属元素__ ,该元素形成氢氧化物的电子式_ ,检验物质中是否含有该元素的方法是:__ 。
④在上表所列元素的最高价氧化物对应水化物中酸性最强的是__ (写化学式)。该元素与硫元素相比,非金属性较强的元素是__ (填元素符号),请写出证明该结论的一个实验事实:__ 。
⑤如图,将潮湿的Cl2单质通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所盛试剂可能是___ 。

a.浓硫酸 b.NaOH溶液 c.KI溶液 d.饱和食盐水
⑥由于氢元素的化合价,有人提议还可以将其放在第__ 族,又有人提议可将它放在周期表中第IVA族,这样建议的原因是__ 。
⑦科学家通过对某些元素的化合价进行研究,寻找高效农药。这些元素往往位于元素周期表的__ (选填序号)。
a.左下角区域 b.右上角区域 c.左上角区域 d.右下角区域
(1)如图是铁元素在元素周期表中的有关信息。

写出Fe的原子结构示意图
下表是元素周期表的一部分:

(2)从原子结构角度分析,C、N、O、F四种元素处于同一行,是由于它们的
(3)通过元素周期表,我们可以知道:
①氮元素的最低化合价为
②与硅元素处于同一周期,两性金属元素是
③第三周期半径最大的金属元素
④在上表所列元素的最高价氧化物对应水化物中酸性最强的是
⑤如图,将潮湿的Cl2单质通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所盛试剂可能是

a.浓硫酸 b.NaOH溶液 c.KI溶液 d.饱和食盐水
⑥由于氢元素的化合价,有人提议还可以将其放在第
⑦科学家通过对某些元素的化合价进行研究,寻找高效农药。这些元素往往位于元素周期表的
a.左下角区域 b.右上角区域 c.左上角区域 d.右下角区域
您最近一年使用:0次

 使酸性
使酸性 溶液褪色(离子方程式)
溶液褪色(离子方程式) 溶液与稀硫酸的反应(离子方程式)
溶液与稀硫酸的反应(离子方程式) 的燃烧热是
的燃烧热是 ,表示
,表示


