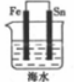
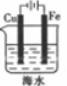
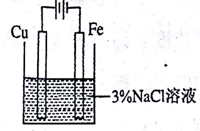
验证牺牲阳极法,实验如下(烧杯内均为经过酸化的3%NaCl溶液)。
下列说法不正确 的是
| ① | ② | ③ |
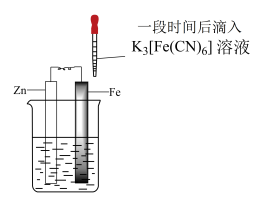 | 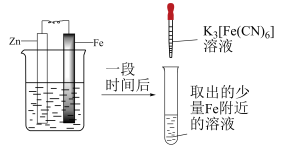 | 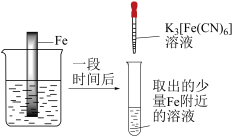 |
| 在Fe表面生成蓝色沉淀 | 试管内无明显变化 | 试管内生成蓝色沉淀 |
A.对比①②, 可能将Fe氧化 可能将Fe氧化 |
| B.对比②③,可以判定Zn保护了Fe |
C.用 酸性溶液代替 酸性溶液代替 溶液,也可验证牺牲阳极法 溶液,也可验证牺牲阳极法 |
| D.将Zn换成Cu,用①的方法无法判断Fe比Cu活泼 |
更新时间:2023-01-07 15:54:58
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】在检验用FeCl3溶液生产铜制印刷线路板后所得的废液成分的实验中,下列根据实验现象得出的结论不正确的是
| A.若用惰性电极电解该废液,阴极没有立即产生红色物质,说明废液中不含Cu2+ |
| B.若向废液中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明废液中含有C1- |
| C.若向废液中加少量铁粉,充分反应后无固体剩余,说明废液中含有Fe3+ |
| D.若向废液中滴加KSCN 溶液,无现象,再加入氯水后溶液呈血红色,说明废液中含有Fe2+ |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列实验操作、现象及所得出的结论或解释均正确的是
| 选项 | 实验操作 | 现象 | 结论或解释 |
| A | 向盐酸中滴加Na2SO3溶液 | 产生使品红溶液褪色的气体 | 非金属性:Cl>S |
| B | 向废FeCl3蚀刻液X中加入少量的铁粉,振荡 | 未出现红色固体 | X中一定不含Cu2+ |
| C | 用c(Fe3+)相同的Fe2(SO4)3和FeCl3溶液,分别清洗做完银镜反应的试管 | FeCl3溶液清洗得较干净 | Fe3++Ag Fe2++Ag+是可逆反应,且AgCl更难溶于水 Fe2++Ag+是可逆反应,且AgCl更难溶于水 |
| D | 用3 mL稀硫酸与纯锌粒反应,再加入几滴 Cu(NO3)2浓溶液 | 迅速产生无色气体 | 形成Zn-Cu原电池加快了制取H2的速率 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】下列方案设计、现象和结论都正确的是
目的 | 方案设计 | 现象和结论 | |
A | 比较金属活泼性 | Mg、Al、NaOH溶液构成原电池装置 | 若Mg片上冒气泡,证明活泼性:Al>Mg |
B | 探究压强对平衡移动的影响 | 用针筒吸入NO2与N2O4的混合气体,将细管端用橡胶塞封闭,然后将活塞向内推,观察颜色变化 | 若颜色先变深后又逐渐变浅,证明压强增大,平衡朝气体分子数减小的方向移动 |
C | 探究反应的可逆性 | 往Fe2(SO4)3溶液中滴加KSCN溶液,再加入少量K2SO4固体 | 若溶液先变成血红色,后无明显变化,说明Fe3+与SCN-的反应不可逆 |
D | 用牺牲阳极法保护铁钉并检验其效果 | 以铁钉和锌棒作电极,酸化的3% NaCl溶液作电解质溶液,接通电源,过一段时间,取铁电极区域溶液于试管中,滴入K3[Fe(CN)6]溶液,观察现象 | 若未出现特征蓝色沉淀,证明铁钉未被腐蚀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】青铜器在潮湿环境中发生电化学腐蚀原理如图所示:多孔催化层中的Cl-扩散到孔口,与电极产物作用生成多孔粉状锈Cu2(OH)3Cl,下列说法正确的是( )
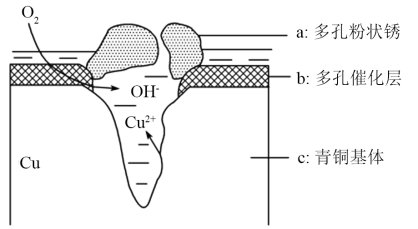

| A.此过程为电化学腐蚀中的析氢腐蚀 |
| B.电极b发生的反应:O2+4e-+2H2O=4OH- |
| C.生成Cu2(OH)3Cl的反应:2Cu2++3H2O+Cl-=Cu2(OH)3Cl↓+3H+ |
| D.若采用牺牲阳极的阴极保护法保护青铜器是利用了电解的原理 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】防止金属锈蚀的方法有多种,如图表示保护铁管的方法为


| A.牺牲阳极的阴极保护法 | B.改变金属的组成和结构法 |
| C.外加电流的阴极保护法 | D.表面覆盖保护层法 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】一种适合在沙漠或偏远地区使用的锂尿电池装置(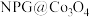 为纳米多孔金包裹
为纳米多孔金包裹 )如图所示,已知
)如图所示,已知 溶液显碱性。下列说法错误的是
溶液显碱性。下列说法错误的是

 为纳米多孔金包裹
为纳米多孔金包裹 )如图所示,已知
)如图所示,已知 溶液显碱性。下列说法错误的是
溶液显碱性。下列说法错误的是
| A.纳米多孔金具有比表面积大、导电性好、耐腐蚀的优点 |
B.电池工作时,正极反应式为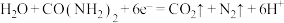 |
C.电池工作时,外电路电流从纳米多孔金流向 板 板 |
| D.电池工作一段时间后,正极区电解质溶液质量增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
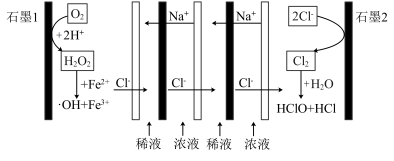
【推荐2】一种利用溶液浓差能驱动的原电池氧化含有甲醛(HCHO)的酸性有机废水的机理如图所示,装置中浓液和稀液的溶质均为NaCl,阴阳离子交换膜将浓液和稀液隔开,•OH具有很强的氧化性,甲醛最终转化为 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是
| A.石墨1为原电池的负极 |
B.正极区处理甲醛的化学方程式为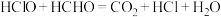 |
C.负极的电极反应式为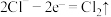 |
D.若处理含  的废水(其他物质不反应),电路中理论上转移2mol电子 的废水(其他物质不反应),电路中理论上转移2mol电子 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】化学镀铜废液中含有一定量的CuSO4,任意排放会污染环境,利用电化学原理可对废液进行回收处理,装置如图,其中质子交换膜只允许H+通过。已知:①Cu2++ HCHO + 3OH-=Cu + HCOO-+ 2H2O;②还原性:HCHO > M(—种金属)> Cu。
下列说法正确的是

下列说法正确的是

| A.反应之前,应将含OH-的HCHO溶液加入到装置的左侧 |
| B.右侧发生的电极反应式:HCHO-2e-+H2O=HCOO-+3H+ |
| C.若将质子交换膜换成阴离子交换膜,放电过程中,大量的OH-将向左侧迁移 |
| D.放电一段时间后打开开关,移去质子交换膜,装置中可能会有红色固体、蓝色絮状物出现 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】有关下列说法中,正确的是
| A.用标准盐酸滴定未知浓度的NaOH溶液,滴定前酸式滴定管尖嘴有气泡未排出,滴定后气泡消失,会造成测定结果偏低 |
| B.工业废水中的Cu2+、Hg2+等重金属阳离子可以通过加入FeS除去 |
| C.工业上常在铁板表面镀上一层锡(俗称马口铁)来防止铁板表面破损后发生电化学腐蚀 |
| D.等体积的pH均为2的酸HA和HB的溶液分别与足量的铁粉反应,HA放出的H2多,说明HA酸性强 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】下列说法不正确 的是
| A.燃料电池、铅蓄电池都利用了原电池原理 |
| B.镀锌的铁表面有划痕时,仍比不镀锌的铁更难被腐蚀 |
C.在使用的燃煤中加入适量 ,可减少 ,可减少 及温室气体的排放 及温室气体的排放 |
| D.选用不同种类的催化剂,甲醛与苯酚可反应制得线型或体型的酚醛树脂 |
您最近一年使用:0次