元素周期表揭示了化学元素间的内在联系,部分元素在周期表中的位置如图所示:
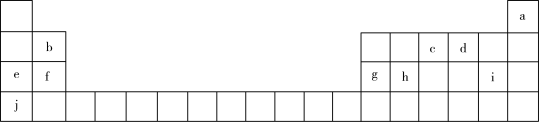
(1)元素h的原子结构示意图为_______ 。
(2)元素e的单质着火时,应该用_______ 来灭火。该单质需密封保存,其中一个目的是与水隔离,原因是_______ (用离子反应方程式表示)。
(3)元素g的氢氧化物化学式为_______ ,其用于中和胃酸的原理是_______ (用离子反应方程式表示)。
(4)写出元素f与元素i形成的化合物的电子式_______ 。
(5)元素b、e、f的最高价氧化物对应的水化物碱性由强到弱的顺序是_______ (用化学式表示)。
(6)实验室检验元素i的简单离子的操作和现象是_______ 。

(1)元素h的原子结构示意图为
(2)元素e的单质着火时,应该用
(3)元素g的氢氧化物化学式为
(4)写出元素f与元素i形成的化合物的电子式
(5)元素b、e、f的最高价氧化物对应的水化物碱性由强到弱的顺序是
(6)实验室检验元素i的简单离子的操作和现象是
更新时间:2023-01-10 12:49:02
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】高铁酸钠(Na2FeO4)具有很强的氧化性,是一种新型的绿色净水消毒剂。工业上可以通过次氯酸钠氧化法制备高铁酸钠,生产过程如下:
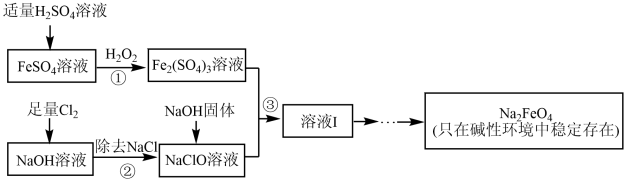
(1)高铁酸钠中铁元素的化合价为_______ ,次氯酸钠的电子式是_______ 。
(2)铁元素位于元素周期表的第四周期第VIII族,原子序数是26,最外层有2个电子。元素铁的原子结构示意图是_______ 。
(3)步骤①反应的离子方程式是_______ 。
(4)工业废水中常含有一定量的 易被人体吸收积累而导致肝癌。处理工业含铬废水的方法通常是将
易被人体吸收积累而导致肝癌。处理工业含铬废水的方法通常是将 转化为Cr3+,再将Cr3+转化为沉淀。利用硫酸工业废气中的SO2可以处理酸性含铬废水,用离子方程式表示反应原理
转化为Cr3+,再将Cr3+转化为沉淀。利用硫酸工业废气中的SO2可以处理酸性含铬废水,用离子方程式表示反应原理_______ 。
(5)已知Ksp[Cr(OH)3]=1×10-30。室温下,除去被SO2还原所得溶液中的Cr3+[使c(Cr3+)≤1×10-6mol·L-1],需调节溶液的pH至少为_______ 。
(6)Cr(OH)3和Al(OH)3类似,也是两性氢氧化物。写出Cr(OH)3与NaOH反应的方程式_______ 。

(1)高铁酸钠中铁元素的化合价为
(2)铁元素位于元素周期表的第四周期第VIII族,原子序数是26,最外层有2个电子。元素铁的原子结构示意图是
(3)步骤①反应的离子方程式是
(4)工业废水中常含有一定量的
 易被人体吸收积累而导致肝癌。处理工业含铬废水的方法通常是将
易被人体吸收积累而导致肝癌。处理工业含铬废水的方法通常是将 转化为Cr3+,再将Cr3+转化为沉淀。利用硫酸工业废气中的SO2可以处理酸性含铬废水,用离子方程式表示反应原理
转化为Cr3+,再将Cr3+转化为沉淀。利用硫酸工业废气中的SO2可以处理酸性含铬废水,用离子方程式表示反应原理(5)已知Ksp[Cr(OH)3]=1×10-30。室温下,除去被SO2还原所得溶液中的Cr3+[使c(Cr3+)≤1×10-6mol·L-1],需调节溶液的pH至少为
(6)Cr(OH)3和Al(OH)3类似,也是两性氢氧化物。写出Cr(OH)3与NaOH反应的方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下表是元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
(1)⑥的原子结构示意图是_______ 。
(2)⑧的一种核素的中子数是20,表示该核素的符号是_______ 。
(3)①、②、③、④四种元素形成的简单离子,半径由大到小的顺序是_______ (用离子符号表示)。
(4)③和⑤的最高价氧化物对应的水化物反应的离子方程式为_______ 。
(5)下列事实能判断⑦和⑧的非金属性强弱的是_______ (填字母,下同)。
a.单质与氢气化合的难易程度 b.氧化物对应的水化物的酸性强弱
c.单质之间的置换反应 d.氢化物水溶液的酸性强弱
(6)①和②形成的原子个数比为1∶2的化合物能与水反应生成一种单质和一种酸,写出该反应的化学方程式_______ 。
族 周期 | IA | 0 | ||||||
| 1 | IIA | IIIA | IVA | VA | VIA | VIIA | ||
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(2)⑧的一种核素的中子数是20,表示该核素的符号是
(3)①、②、③、④四种元素形成的简单离子,半径由大到小的顺序是
(4)③和⑤的最高价氧化物对应的水化物反应的离子方程式为
(5)下列事实能判断⑦和⑧的非金属性强弱的是
a.单质与氢气化合的难易程度 b.氧化物对应的水化物的酸性强弱
c.单质之间的置换反应 d.氢化物水溶液的酸性强弱
(6)①和②形成的原子个数比为1∶2的化合物能与水反应生成一种单质和一种酸,写出该反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】有A、B、C、D四种元素,已知A元素原子的K层和M层电子数相同;B元素原子的L层比K层电子数多5个;C元素的+3价阳离子和氖原子具有相同的电子数;D元素的最外层电子数是次外层电子数的3倍。
(1)写出元素符号:A_______ ,D_______ 。
(2)A的原子结构示意图_______ ,B的离子结构示意图_______ ,C的离子结构示意图_______ 。
(3)C原子的电子式_______ 。
(4)A和B元素组成的物质的化学式为_______ ,它是由_______ (选填“原子”、“离子”或“分子”)构成的物质。
(5)由C和D可组成CD 离子,一个CD
离子,一个CD 离子所带电子数为
离子所带电子数为_______ 。
(1)写出元素符号:A
(2)A的原子结构示意图
(3)C原子的电子式
(4)A和B元素组成的物质的化学式为
(5)由C和D可组成CD
 离子,一个CD
离子,一个CD 离子所带电子数为
离子所带电子数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】已知A、B、C、D、E、F 均为短周期主族元素,原子序数依次增大。C为地壳中含量最高的元素,E原子的次外层电子数是最外层的2倍,F最高价氧化物对应的水化物酸性比H2SO4强。A、D同主族,B、C同周期,气态化合物甲由A、B两种元素组成,其原子个数比为4∶1。
(1)化合物甲的空间结构_______ 。
(2)F在周期表中的位置_______ 。
(3)B、D、E 3种元素原子半径由大到小顺序_______ (用元素符号表示)。
(4)用电子式表示D和F形成化合物的过程_______ 。
(5)B的最高价氧化物和D的一种氧化物能发生反应生成C单质,写出该反应的化学方程式_______ 。
(1)化合物甲的空间结构
(2)F在周期表中的位置
(3)B、D、E 3种元素原子半径由大到小顺序
(4)用电子式表示D和F形成化合物的过程
(5)B的最高价氧化物和D的一种氧化物能发生反应生成C单质,写出该反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】常见金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间存在如下转化关系(图中有些反应的产物和反应的条件没有全部标出)。其中B是地壳中含量居第一的金属元素。请回答下列问题:

(1)气体丙的电子式为_______ 。
(2)写出下列反应的离子方程式:③_______ ;⑤_______ 。
(3)金属C在一定条件下与水蒸气反应的化学方程式为_______ 。
(4)溶液F中加入溶液D后的现象是_______ ,所发生反应的化学方程式为_______ ,_______ 。
(5)溶液F放置于空气中容易变质,检验溶液F是否变质的方法是_______ 。

(1)气体丙的电子式为
(2)写出下列反应的离子方程式:③
(3)金属C在一定条件下与水蒸气反应的化学方程式为
(4)溶液F中加入溶液D后的现象是
(5)溶液F放置于空气中容易变质,检验溶液F是否变质的方法是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下图是元素周期表的部分,针对表中的10种元素,用元素符号或化学式回答相关问题:
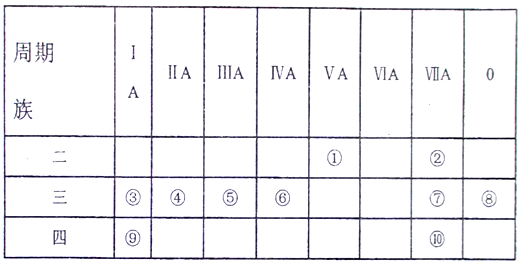
(1)画出④的阳离子结构示意图_________ 。
(2)这些元素中的最高价氧化物对应的水化物中,酸性最强的是______ ,碱性最强的是_____ 。
(3) 将⑦单质通入③与⑩组成的化合物的水溶液中,发生反应的离子方程式为_________ 。
(4)写出下列物质的电子式:
①形成的单质_________ ②与⑨形成的物质_________
用电子式表示④与⑦所组成物质的形成过程_______________ 。

(1)画出④的阳离子结构示意图
(2)这些元素中的最高价氧化物对应的水化物中,酸性最强的是
(3) 将⑦单质通入③与⑩组成的化合物的水溶液中,发生反应的离子方程式为
(4)写出下列物质的电子式:
①形成的单质
用电子式表示④与⑦所组成物质的形成过程
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】随着原子序数的递增,8种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如下图所示:
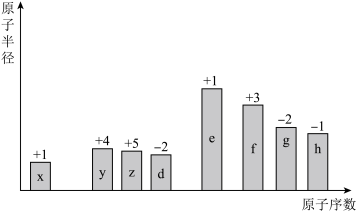
(1)h在元素周期表中的位置是___________ 。
(2)d、g的简单氢化物中热稳定性较强的是___________ (填化学式)。
(3)由10个x原子与4个y原子构成化合物的结构式有___________ 种。
(4)e、g形成的离子化合物的电子式为___________ 。e元素形成的最高价氧化物对应的水化物中含有的化学键类型为___________ 。
(5)e与f相比,金属性较强的是___________ (用元素符号表示),下列事实能证明这一结论的是___________ 。(填字母序号)。
a.e单质的熔点比f单质的低,单质的硬度也比f单质小
b.e单质可与冷水剧烈反应,而f单质与冷水几乎不反应
c.e的最高价氧化物的水化物是强碱,而f的最高价氧化物的水化物具有两性
(6)h的单质能将z从其简单氢化物中置换出来,化学方程式为___________ 。

(1)h在元素周期表中的位置是
(2)d、g的简单氢化物中热稳定性较强的是
(3)由10个x原子与4个y原子构成化合物的结构式有
(4)e、g形成的离子化合物的电子式为
(5)e与f相比,金属性较强的是
a.e单质的熔点比f单质的低,单质的硬度也比f单质小
b.e单质可与冷水剧烈反应,而f单质与冷水几乎不反应
c.e的最高价氧化物的水化物是强碱,而f的最高价氧化物的水化物具有两性
(6)h的单质能将z从其简单氢化物中置换出来,化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】现有H、N、O、Na、Cl、Fe、Cu七种常见元素,回答下列问题:
(1)Cl位于周期表第____ 周期____ 族。
(2)Na+离子的结构示意图为____ 。
(3)能说明非金属性Cl比N强的事实是____ (用方程式表示)。
(4)A~L是由上述七种元素中的一种、二种或三种组成,A的摩尔质量为166g·mol-1,其焰色反应呈黄色;B是最常见的液体;C中两元素的质量比为96∶7; D、E属同类物质,E呈红褐色。F、G、H、I为单质,其中F、G是无色气体,H是紫红色固体,I是黄绿色气体;L是常见的强酸。它们有如下图所示的关系(部分反应条件及产物已略去):
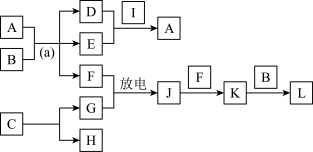
①C的化学式为____ 。
②D的电子式为____ 。
③L的稀溶液与H反应的离子方程式为____ 。
④反应(a)的化学方程式为____ 。
(1)Cl位于周期表第
(2)Na+离子的结构示意图为
(3)能说明非金属性Cl比N强的事实是
(4)A~L是由上述七种元素中的一种、二种或三种组成,A的摩尔质量为166g·mol-1,其焰色反应呈黄色;B是最常见的液体;C中两元素的质量比为96∶7; D、E属同类物质,E呈红褐色。F、G、H、I为单质,其中F、G是无色气体,H是紫红色固体,I是黄绿色气体;L是常见的强酸。它们有如下图所示的关系(部分反应条件及产物已略去):

①C的化学式为
②D的电子式为
③L的稀溶液与H反应的离子方程式为
④反应(a)的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下列为元素周期表中的一部分,除注明外其他都用化学用语回答下列问题:
⑴8种元素中,化学性质最不活泼的是_________ ;非金属性最强的是_____________ ;
⑵①②⑤的最高价氧化物对应水化物的碱性由强到弱的顺序为________________ ;
⑶②③④中形成的简单离子半径由大到小的顺序为_______________________ ;
⑷⑥的氢化物常温下与元素②的过氧化物反应的离子方程式为____________ ;
⑸①和⑥形成的淡黄色固体的电子式为______________ ,所含化学键的类型为(填“离子键”或“共价键”)____________ ;
⑹①和⑤的最高价氧化物对应水化物相互反应的离子方程式为_________________ 。
族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ⑥ | ⑦ | ||||||
3 | ① | ③ | ⑤ | ⑧ | ||||
4 | ② | ④ |
⑴8种元素中,化学性质最不活泼的是
⑵①②⑤的最高价氧化物对应水化物的碱性由强到弱的顺序为
⑶②③④中形成的简单离子半径由大到小的顺序为
⑷⑥的氢化物常温下与元素②的过氧化物反应的离子方程式为
⑸①和⑥形成的淡黄色固体的电子式为
⑹①和⑤的最高价氧化物对应水化物相互反应的离子方程式为
您最近一年使用:0次



