下表是元素周期表的一部分,请回答:
(1)元素⑦的原子结构示意图为_______ ;元素⑩的名称为_______ 。
(2)在这些元素中,化学性质最活泼的金属元素是_______ (填元素符号,下同),最不活泼的元素是_______ ;原子半径最小的元素是_______ 。
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式,下同);具有两性的是_______ 。
(4)用电子式表示⑤⑦形成化合物过程:_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
4 | ⑨ | ⑩ |
(2)在这些元素中,化学性质最活泼的金属元素是
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是
(4)用电子式表示⑤⑦形成化合物过程:
更新时间:2023/01/10 16:55:54
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】我国“四大发明”在人类发展史上起到了非常重要的作用。其中黑火药的爆炸反应:2KNO3+S+3C K2S+N2↑+3CO2↑。
K2S+N2↑+3CO2↑。
(1)该反应中被还原的元素是___________ (填元素符号);氧化性:KNO3___________ CO2(填“>”或“<”)。
(2)硝酸钾是一种氮钾复合肥。从其阳离子看,则属于钾盐,从其阴离子看,则属于硝酸盐,该分类方法称为___________ 。
(3)上述反应物和生成物中属于非电解质的有___________ 。
(4)CO2属于酸性氧化物,可与NaOH、_______ (填与NaOH不同类别的一种具体物质的化学式)等反应。
(5)N2的电子为___________ ;请用电子式表示K2S的形成过程___________ 。
 K2S+N2↑+3CO2↑。
K2S+N2↑+3CO2↑。(1)该反应中被还原的元素是
(2)硝酸钾是一种氮钾复合肥。从其阳离子看,则属于钾盐,从其阴离子看,则属于硝酸盐,该分类方法称为
(3)上述反应物和生成物中属于非电解质的有
(4)CO2属于酸性氧化物,可与NaOH、
(5)N2的电子为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】写出下列物质形成过程的电子式:(离子键、极性键、非极性键)
(1)Cl2__________________ 含有________ 键
(2)HCl__________________ 含有________ 键
(3)MgCl2__________________ 含有________ 键
(4)H2O2______________ 含有________ 、________ 键
(5)NaOH______________ 含有________ 、________ 键
(1)Cl2
(2)HCl
(3)MgCl2
(4)H2O2
(5)NaOH
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】19世纪初,许多新的元素被相继发现,化学家开始关注这些元素在化学性质和物理性质上的相似性和递变性。1869年,俄国化学家门捷列夫编制了一份元素周期表,是化学发展史上的一个里程碑。A、B、C、D为短周期元素,在周期表中所处的位置如图所示,A、C两元素的原子核外电子数之和等于B元素原子的质子数。
(1)A原子的电子式为_______ ,B的氢化物的分子式为_______ ,C离子的结构示意图为_______ 。
(2)D的单质与水反应的化学方程式为_______ 。
| A | C | |
| B | D |
(2)D的单质与水反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】结合下图所示元素周期表,回答下列问题:___________ (填字母,下同);属于主族元素的有___________ 。
(2)f元素位于第___________ 周期第___________ 族。g元素位于第___________ 周期第___________ 族,i元素位于第___________ 周期第___________ 族。
(3)b、c、e三种元素最高价氧化物的水化物两两之间能发生反应。请写出反应的离子方程式:___________ 、___________ 、___________ 。

(2)f元素位于第
(3)b、c、e三种元素最高价氧化物的水化物两两之间能发生反应。请写出反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】如表是元素周期表的一部分,根据表中给出的10种元素,按要求作答。
(1)金属性最强的元素是_______ ;
(2)F的原子结构示意图是________ ;
(3)地壳中含量最多的元素是_______ ;
(4)Ne原子的最外层电子数是_______ ;
(5)N与O原子半径较大的是_______ ;
(6)H2S与HCl热稳定性较弱的是______ ;
(7)Na2O与MgO难与水反应的是______ ;
(8)Mg(OH)2与Al(OH)3能与强碱反应的是______ ;
(9)用于制造光导纤维的物质是______ (填“Si”或“SiO2”);
(10)次氯酸(HClO)具有杀菌漂白作用,其中Cl元素的化合价为____ ,HClO不稳定,易分解生成HCl和O2,写出其在光照条件下分解的化学方程式:____ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | N | O | F | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(1)金属性最强的元素是
(2)F的原子结构示意图是
(3)地壳中含量最多的元素是
(4)Ne原子的最外层电子数是
(5)N与O原子半径较大的是
(6)H2S与HCl热稳定性较弱的是
(7)Na2O与MgO难与水反应的是
(8)Mg(OH)2与Al(OH)3能与强碱反应的是
(9)用于制造光导纤维的物质是
(10)次氯酸(HClO)具有杀菌漂白作用,其中Cl元素的化合价为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】19世纪初,许多新的元素被相继发现,化学家开始关注这些元素在化学性质和物理性质上的相似性和递变性。1869年,俄国化学家门捷列夫编制了一份元素周期表,是化学发展史上的一个里程碑。A、B、C、D为短周期元素,在周期表中所处的位置如图所示,A、C两元素的原子核外电子数之和等于B元素原子的质子数。
(1)A原子的电子式为_______ ,B的氢化物的分子式为_______ ,C离子的结构示意图为_______ 。
(2)D的单质与水反应的化学方程式为_______ 。
| A | C | |
| B | D |
(2)D的单质与水反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
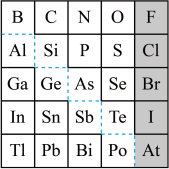
(1)元素Ga在元素周期表中的位置为:第________ 周期第________ 族。
(2)Sn的最高正价为________ ,Cl的最高价氧化物对应水化物的化学式为________ ,Bi的最高价氧化物为________ 。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是________ 元素(填元素符号)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4________ (填“>”“<”或“=”)H2SeO4。
③氢化物的还原性:H2O________ (填“>”“<”或“=”)H2S。
④原子半径比较:N________ (填“>”“<”或“=”)Si。
(4)从下列试剂中选择最佳试剂组合,比较C、Si的非金属性强弱___________________ (可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液)

(1)元素Ga在元素周期表中的位置为:第
(2)Sn的最高正价为
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③氢化物的还原性:H2O
④原子半径比较:N
(4)从下列试剂中选择最佳试剂组合,比较C、Si的非金属性强弱
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】A、B、C、D四种元素在元素周期表中的位置如图所示。

请回答下列问题:
(1)A的元素名称是___ ,它在元素周期表第___ 周期,第___ 族。
(2)A、B、C相比,其原子半径由大到小的顺序是___ (用元素符号表示,下同)。
(3)C与D相比,非金属性较强的是___ ,能证明这一结论的事实是___ (用化学方程式表示)。

请回答下列问题:
(1)A的元素名称是
(2)A、B、C相比,其原子半径由大到小的顺序是
(3)C与D相比,非金属性较强的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】如图是元素周期表的一部分,回答下列问题:
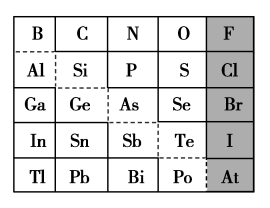
(1)元素Ga在元素周期表中的位置为:第_______ 周期第_______ 族。
(2)Sn的最高正价为_______ ,Cl的最高价氧化物对应的水化物的化学式为_______ ,Bi的最高价氧化物的化学式为_______ 。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是_______ (填元素符号)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4_______ H2SeO4(填“>”或“<”下同)。
③氢化物的还原性:H2O_______ H2S。

(1)元素Ga在元素周期表中的位置为:第
(2)Sn的最高正价为
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③氢化物的还原性:H2O
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题
(1)比较下列有关碱金属元素单质或化合物的性质(填“>”或“<”)。
①熔点:Li_____ Na ②密度:K_____ Rb
③金属性:Li_____ K ④碱性:LiOH_____ NaOH
说说碱金属的性质随原子序数递增有哪些递变规律_____ ?
(2)某碳酸钠溶液中可能含有碳酸钾。小王同学用洁净的铂丝,蘸取该无色溶液,在无色火焰上灼烧,火焰呈黄色。能否判断该溶液中是否含有碳酸钾?如何进一步得出结论_____ ?
(1)比较下列有关碱金属元素单质或化合物的性质(填“>”或“<”)。
①熔点:Li
③金属性:Li
说说碱金属的性质随原子序数递增有哪些递变规律
(2)某碳酸钠溶液中可能含有碳酸钾。小王同学用洁净的铂丝,蘸取该无色溶液,在无色火焰上灼烧,火焰呈黄色。能否判断该溶液中是否含有碳酸钾?如何进一步得出结论
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】元素周期表是学习化学的重要工具。下表为某些元素在周期表中的位置。
(1)按①→②→③→④的顺序,其原子半径逐渐_____ (填“增大”或“减小”),得电子能力逐渐______ (填“增强”或“减弱”,下同),单质的氧化性逐渐______ ,非金属性逐渐______ ,最简单氢化物的稳定性逐渐______ 。
(2)表中化学性质最稳定的元素为___________ (填元素符号)。
(3)⑥与③形成原子个数比为1:1的化合物,属于______ 化合物(填“离子”或“共价”)其电子式为:________ ,含有的化学键________ 。
(4)⑦与⑧的最高价氧化物对应的水化物是否可以相互反应______ (填“是”或“否”)。
(5)⑨的最高价氧化物对应的水化物为________ (填化学式)。
周期 | 族 | |||||||
Ⅰ A | Ⅱ A | Ⅲ A | Ⅳ A | Ⅴ A | Ⅵ A | Ⅶ A | 0 | |
2 | ① | ② | ③ | ④ | ⑤ | |||
3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
(1)按①→②→③→④的顺序,其原子半径逐渐
(2)表中化学性质最稳定的元素为
(3)⑥与③形成原子个数比为1:1的化合物,属于
(4)⑦与⑧的最高价氧化物对应的水化物是否可以相互反应
(5)⑨的最高价氧化物对应的水化物为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】已知氟、氯、溴、碘在元素周期表中位于同一纵行,都是典型的非金属元素,都能与大多数金属化合生成盐,故统称为卤素。卤素单质都具有氧化性,其氧化性强弱顺序是F2>Cl2>Br2>I2,它们都能与H2、H2O等反应。
(1)若用X2表示卤素单质,则X2与H2化合的化学方程式是________________________ ,其反应条件难易规律是________________________________________ 。
(2)氧化性强的卤素单质(如Cl2)能把氧化性弱的卤素从其卤化物(如NaBr或KI)中置换出来。请写出将氯气通入碘化钾溶液中的化学方程式:______________________ ,离子方程式:________________________________ 。
(1)若用X2表示卤素单质,则X2与H2化合的化学方程式是
(2)氧化性强的卤素单质(如Cl2)能把氧化性弱的卤素从其卤化物(如NaBr或KI)中置换出来。请写出将氯气通入碘化钾溶液中的化学方程式:
您最近一年使用:0次



