燃料电池可以将燃料的化学能直接转化为电能,能量利用率高。
(1)碱性燃料电池(AFC)是最早进入实用阶段的燃料电池之一,也是最早用于车辆的燃料电池,以KOH、NaOH溶液之类的强碱性溶液为电解质溶液。其优点为性能可靠,具有较高的效率。甲烷碱性燃料电池正极的电极反应式为_______
(2)某燃料电池主要构成要素如图所示
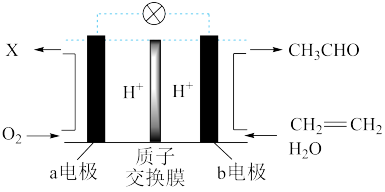
电流方向为__ ;电池工作时,X为___ ; a电极的反应式为___ ; b电极的反应式为____ 。
(1)碱性燃料电池(AFC)是最早进入实用阶段的燃料电池之一,也是最早用于车辆的燃料电池,以KOH、NaOH溶液之类的强碱性溶液为电解质溶液。其优点为性能可靠,具有较高的效率。甲烷碱性燃料电池正极的电极反应式为
(2)某燃料电池主要构成要素如图所示

电流方向为
更新时间:2023-01-11 17:14:59
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】燃料电池是利用燃料(如 、CO、
、CO、 、
、 、
、 等)与
等)与 反应从而将化学能转化为电能的装置。
反应从而将化学能转化为电能的装置。
(1)甲烷燃料电池(NaOH溶液作电解质溶液)的负极反应式为___________ ,正极反应式为___________ ,放电过程中溶液的pH___________ (填“增大”“减小”或“不变”)。
(2)瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如下,下列有关说法正确的是___________ 。
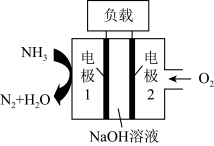
a.电池工作时, 向负极移动
向负极移动
b.电子由电极2经外电路流向电极1
c.电池总反应为
d.电极2发生的电极反应为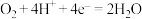
(3)铅酸蓄电池是常用的化学电源,其电极材料分别是Pb和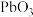 ,电解质溶液为稀硫酸,该电池工作时发生的总反应为
,电解质溶液为稀硫酸,该电池工作时发生的总反应为 。试回答下列问题。
。试回答下列问题。
①铅酸蓄电池的负极材料是___________ ,正极反应为___________ 。
②若有1mol电子从某电极流出,则参加反应的 是
是___________ mol,负极的质量变化是___________ (填“增大”或“减小”)___________ g。
 、CO、
、CO、 、
、 、
、 等)与
等)与 反应从而将化学能转化为电能的装置。
反应从而将化学能转化为电能的装置。(1)甲烷燃料电池(NaOH溶液作电解质溶液)的负极反应式为
(2)瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如下,下列有关说法正确的是

a.电池工作时,
 向负极移动
向负极移动b.电子由电极2经外电路流向电极1
c.电池总反应为

d.电极2发生的电极反应为
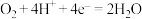
(3)铅酸蓄电池是常用的化学电源,其电极材料分别是Pb和
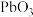 ,电解质溶液为稀硫酸,该电池工作时发生的总反应为
,电解质溶液为稀硫酸,该电池工作时发生的总反应为 。试回答下列问题。
。试回答下列问题。①铅酸蓄电池的负极材料是
②若有1mol电子从某电极流出,则参加反应的
 是
是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)如图所示,杠杆AB两端分别挂有体积相同、质量相同的空心铜球和空心铁球,调节杠杆使其在水中保持平衡,然后小心地向烧杯中央滴入浓 溶液,一段时间后,
溶液,一段时间后,

①当杠杆为导体时,可观察到的现象是:_______ 。
②当杠杆为绝缘体时,可观察到的现象_______ (“相同”或“不相同”)。
(2)某学生利用下面实验装置探究盐桥式原电池的工作原理。
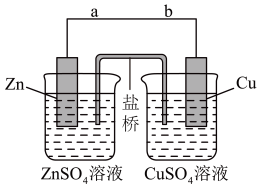
若装置中铜电极的质量增加0.64g,则导线中转移的电子数目为_______ 。
(3)装置中盐桥中除添加琼脂外,还要添加KCl的饱和溶液,电池工作时,对盐桥中的 、
、 的移动方向表述正确的是_______。
的移动方向表述正确的是_______。
(4)若 溶液中含有杂质
溶液中含有杂质 ,会加速Zn电极的腐蚀,还可能导致电流在较短时间内衰减。欲除去
,会加速Zn电极的腐蚀,还可能导致电流在较短时间内衰减。欲除去 ,最好选用下列试剂中的_______(填代号)。
,最好选用下列试剂中的_______(填代号)。
(5)生活中利用原电池原理生产了各种各样的电池,废电池必须进行集中处理的问题已被提到议事日程,其主要原因是_______。
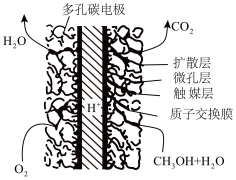
(6)甲醇、氧气在一定条件下可构成如图所示的燃料电池,其正极的电极反应为_______ 。
(1)如图所示,杠杆AB两端分别挂有体积相同、质量相同的空心铜球和空心铁球,调节杠杆使其在水中保持平衡,然后小心地向烧杯中央滴入浓
 溶液,一段时间后,
溶液,一段时间后,
①当杠杆为导体时,可观察到的现象是:
②当杠杆为绝缘体时,可观察到的现象
(2)某学生利用下面实验装置探究盐桥式原电池的工作原理。

若装置中铜电极的质量增加0.64g,则导线中转移的电子数目为
(3)装置中盐桥中除添加琼脂外,还要添加KCl的饱和溶液,电池工作时,对盐桥中的
 、
、 的移动方向表述正确的是_______。
的移动方向表述正确的是_______。A.盐桥中的 向右侧烧杯移动、 向右侧烧杯移动、 向左侧烧杯移动 向左侧烧杯移动 |
B.盐桥中的 向左侧烧杯移动、 向左侧烧杯移动、 向右侧烧杯移动 向右侧烧杯移动 |
C.盐桥中的 、 、 都向左侧烧杯移动 都向左侧烧杯移动 |
D.盐桥中的 、 、 几乎不移动 几乎不移动 |
 溶液中含有杂质
溶液中含有杂质 ,会加速Zn电极的腐蚀,还可能导致电流在较短时间内衰减。欲除去
,会加速Zn电极的腐蚀,还可能导致电流在较短时间内衰减。欲除去 ,最好选用下列试剂中的_______(填代号)。
,最好选用下列试剂中的_______(填代号)。| A.NaOH | B.Zn | C.Fe | D. |
| A.回收利用电池外壳的金属 |
| B.防止电池中汞、镉和铅等重金属离子对土壤、水源的污染 |
| C.防止电池中渗漏的电解液腐蚀其他物品 |
| D.回收其中石墨电极 |

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】到目前为止,由化学能转变的热能或电能仍然是人类使用的主要能源。
(1)从能量变化角度研究反应: 。下图能正确表示该反应中能量变化的是
。下图能正确表示该反应中能量变化的是___________ (填字母)。
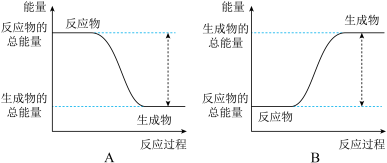
(2)从断键和成键角度分析上述反应中能量的变化,部分化学键的键能如下表:
则生成1 mol  放出热量
放出热量___________ kJ。
(3)将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如图所示装置。
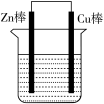
①若电解质溶液为稀硫酸,则Zn棒为原电池的___________ (填“正”或“负”)极,可观察到Cu棒上有气泡生成,写出Cu棒上的电极反应式___________ , 移向
移向___________ 棒。
②若电解质为硫酸铜溶液,则Cu棒上发生___________ (填“氧化”或“还原”)反应,Cu棒上发生的电极反应式为___________ 。
(1)从能量变化角度研究反应:
 。下图能正确表示该反应中能量变化的是
。下图能正确表示该反应中能量变化的是
(2)从断键和成键角度分析上述反应中能量的变化,部分化学键的键能如下表:
| 化学键 | H-H | O=O | H-O |
键能(kJ·mol ) ) | 436 | 496 | 463 |
 放出热量
放出热量(3)将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如图所示装置。

①若电解质溶液为稀硫酸,则Zn棒为原电池的
 移向
移向②若电解质为硫酸铜溶液,则Cu棒上发生
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】
(1)下图原电池装置中,Zn是______ 极(填电极的名称),Cu表面上有___________________ (现象),外电路电子由________ (填电极的名称)通过导线流向_______ (填电极的名称); 溶液中_______ 离子向Cu极移动,________ 离子向Zn极移动。
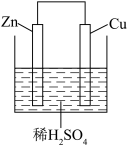
(2)写出电极反应式和总反应方程式:
Zn极:___________________________________________
Cu极:_________________________________________
总反应方程式:___________________________________
(1)下图原电池装置中,Zn是

(2)写出电极反应式和总反应方程式:
Zn极:
Cu极:
总反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)某研究性学习小组为探究Fe3+与Ag反应,进行如下实验:按下图连接装置并加入药品(盐桥中的物质不参与反应)。
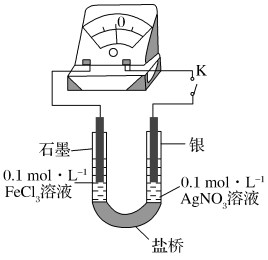
①K闭合时,指针向左偏转,石墨作_____ (填“正极”或“负极”)。
②当指针归零后,向左侧U形管中滴加几滴FeCl2浓溶液,发现指针向右偏转,写出此时银电极的反应式:__________
③结合上述实验分析,写出Fe3+和Ag反应的离子方程式:______________ 。
④丙同学进一步验证其结论:当指针归零后,向右侧U形管中滴加数滴饱和NaCl溶液,可观察到的现象是__________ 。
(2)PbSO4热激活电池可用作火箭、导弹的工作电源。基本结构如图所示,其中作为电解质的无水LiCl—KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。(已知:LiCl熔点605℃,CaCl2熔点772℃)
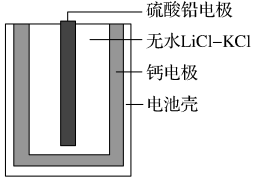
①放电过程中,Li+向________ 填(“负极”或“正极”)移动。
②负极反应式为__________ 。
③电路中每转移0.2 mol电子,理论上生成________ g Pb。(Pb的相对原子质量207)
(1)某研究性学习小组为探究Fe3+与Ag反应,进行如下实验:按下图连接装置并加入药品(盐桥中的物质不参与反应)。

①K闭合时,指针向左偏转,石墨作
②当指针归零后,向左侧U形管中滴加几滴FeCl2浓溶液,发现指针向右偏转,写出此时银电极的反应式:
③结合上述实验分析,写出Fe3+和Ag反应的离子方程式:
④丙同学进一步验证其结论:当指针归零后,向右侧U形管中滴加数滴饱和NaCl溶液,可观察到的现象是
(2)PbSO4热激活电池可用作火箭、导弹的工作电源。基本结构如图所示,其中作为电解质的无水LiCl—KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。(已知:LiCl熔点605℃,CaCl2熔点772℃)

①放电过程中,Li+向
②负极反应式为
③电路中每转移0.2 mol电子,理论上生成
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】人们应用原电池原理制作了多种电池,以满足不同的需要。请根据题中提供的信息,回答下列问题。
(1)铅蓄电池在放电时发生的总反应为 ,负极电极反应式为
,负极电极反应式为_______ 。工作后,铅蓄电池里电解质溶液的pH_______ (填“变大”“变小”或“不变”)。
(2)FeCl3溶液常用于腐蚀印刷电路板,发生反应 ,若将此反应设计成原电池,则负极所用电极材料为
,若将此反应设计成原电池,则负极所用电极材料为_______ 。当转移0.2mol电子时,被腐蚀的铜的质量为_______ g。
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为_______ 。
A铝片、铜片 B.铜片、铝片 C.铝片、铝片
(4)燃料电池是一种高效、环境友好的供电装置。
①如图是电解质溶液为稀硫酸的氢氧燃料电池原理示意图:_______ 。
②将两铂片插入KOH溶液中作为电极,在两极区分别通入甲烷和氧气构成燃料电池,则通入甲烷气体的一极是原电池的_______ 极,该极的电极反应式是_______ 。
(1)铅蓄电池在放电时发生的总反应为
 ,负极电极反应式为
,负极电极反应式为(2)FeCl3溶液常用于腐蚀印刷电路板,发生反应
 ,若将此反应设计成原电池,则负极所用电极材料为
,若将此反应设计成原电池,则负极所用电极材料为(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为
A铝片、铜片 B.铜片、铝片 C.铝片、铝片
(4)燃料电池是一种高效、环境友好的供电装置。
①如图是电解质溶液为稀硫酸的氢氧燃料电池原理示意图:
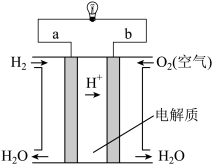
②将两铂片插入KOH溶液中作为电极,在两极区分别通入甲烷和氧气构成燃料电池,则通入甲烷气体的一极是原电池的
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】电能是现代社会应用最广泛的能源之一、
(1)某原电池装置如图所示。其中,Zn电极为原电池的_______ 极(填“正”或“负”)。

(2)Zn电极的电极反应式是_______ 。
(3)Cu电极上发生的反应属于_______ (填“氧化”或“还原”)反应。
(1)某原电池装置如图所示。其中,Zn电极为原电池的

(2)Zn电极的电极反应式是
(3)Cu电极上发生的反应属于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】由锌片、铜片和200mL稀H2SO4组成的原电池如下图所示:
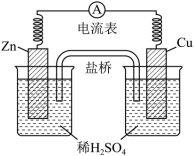
(1)原电池的负极反应式为___________ ,正极反应式为___________ ,盐桥中的K+向___________ (填“铜”或“锌”)电极移动。
(2)一段时间后,当在铜片上放出5.6L(标准状况)气体时,H2SO4恰好消耗一半,则产生这些气体的同时,共消耗___________ g锌,有___________ mol电子通过了导线,原硫酸的物质的量浓度是___________ 。
(3)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为___________ 。

(1)原电池的负极反应式为
(2)一段时间后,当在铜片上放出5.6L(标准状况)气体时,H2SO4恰好消耗一半,则产生这些气体的同时,共消耗
(3)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的重大贡献。
(1)将纯锌片和纯铜片按图甲、图乙方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:______ ,该烧杯中铜片上的现象为______ 。
②在相同时间内,两烧杯中产生气泡的速度:甲______ 乙(填“>”“<”或“=”)。
③形成原电池的装置中电子移动的方向是:流向______ (写电极材料的名称)
④当甲中溶液质量增重31.5g时,电极上转移电子数目为______ 。
(2)燃料电池是一种高效、环境友好的发电装置,图丁为甲烷氧气燃料电池的构造示意图,电解质溶液的溶质是KOH。通甲烷一极的为电池的______ (填“正极”或“负极”),写出负极电极反应式______ 。
(1)将纯锌片和纯铜片按图甲、图乙方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
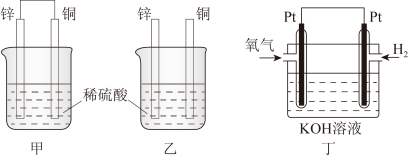
②在相同时间内,两烧杯中产生气泡的速度:甲
③形成原电池的装置中电子移动的方向是:流向
④当甲中溶液质量增重31.5g时,电极上转移电子数目为
(2)燃料电池是一种高效、环境友好的发电装置,图丁为甲烷氧气燃料电池的构造示意图,电解质溶液的溶质是KOH。通甲烷一极的为电池的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为__________ 、_______ 。
(2)用甲烷制取氢气的两步反应的能量变化如下图所示:
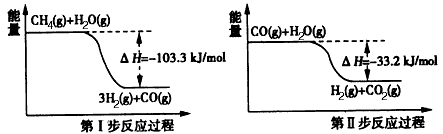
甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是________________ 。
(3)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) △H=-159.5KJ/mol
②NH2CO2NH4(s)= CO(NH2)2(s) +H2O(g) △H=+116.5KJ/mol
③H2O(l)=H2O(g) △H=+44KJ/mol
写出CO2与NH3合成尿素和液态水的热化学方程式__________________ 。
(4)氨气在纯氧中燃烧,生成一种单质和水。科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极在碱性条件下发生反应的电极反应式为_________________ 。
(2)用甲烷制取氢气的两步反应的能量变化如下图所示:

甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是
(3)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) △H=-159.5KJ/mol
②NH2CO2NH4(s)= CO(NH2)2(s) +H2O(g) △H=+116.5KJ/mol
③H2O(l)=H2O(g) △H=+44KJ/mol
写出CO2与NH3合成尿素和液态水的热化学方程式
(4)氨气在纯氧中燃烧,生成一种单质和水。科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极在碱性条件下发生反应的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】电池是人类生产和生活中的重要能量来源,各式各样电池的发明是化学对人类的一项重要贡献。
(1)原电池的设计原理与某一类化学反应有关。你认为下列化学反应,可以设计成原电池的是___________(填字母)。
(2)生活中利用原电池原理生产了各种各样的电池,下列有关电池的叙述正确的是___________ (填字母)。
A.锌锰干电池工作一段时间后正极碳棒会变细
B.氢氧燃料电池可将化学能直接转变为电能
C.太阳能电池的主要材料是高纯度的二氧化硅
D.铅蓄电池负极是 ,正极是
,正极是
E.原电池的负极金属的活动性一定比正极金属的活动性强
F.原电池工作时,阳离子向正极移动,阴离子向负极移动
(3)根据氧化还原反应: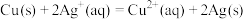 设计原电池,若用铜、银做两个电极,开始两电极质量相等,当电路中转移
设计原电池,若用铜、银做两个电极,开始两电极质量相等,当电路中转移 电子时两电极的质量差为
电子时两电极的质量差为___________ g。
(4)航天技术上使用的氢氧燃料电池具有高能,轻便和不污染环境等优点。氢氧燃料电池有酸式和碱式两种,它们放电时的电池总反应式都可表示为: 。
。
①酸式氢氧燃料电池的电解质是硫酸,其正极的电极反应式为___________ 。
②酸式氢氧燃料电池,工作一段时间后,电解质溶液的 将
将_______ (填“变大”、“变小”或“不变”)。
(5)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压,电池总反应式为: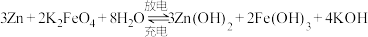 ,负极为
,负极为___________ ,放电时,溶液中 向
向___________ (填“正”或“负”)极移动。
(1)原电池的设计原理与某一类化学反应有关。你认为下列化学反应,可以设计成原电池的是___________(填字母)。
A. |
B. |
C.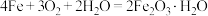 |
D. |
A.锌锰干电池工作一段时间后正极碳棒会变细
B.氢氧燃料电池可将化学能直接转变为电能
C.太阳能电池的主要材料是高纯度的二氧化硅
D.铅蓄电池负极是
 ,正极是
,正极是
E.原电池的负极金属的活动性一定比正极金属的活动性强
F.原电池工作时,阳离子向正极移动,阴离子向负极移动
(3)根据氧化还原反应:
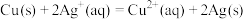 设计原电池,若用铜、银做两个电极,开始两电极质量相等,当电路中转移
设计原电池,若用铜、银做两个电极,开始两电极质量相等,当电路中转移 电子时两电极的质量差为
电子时两电极的质量差为(4)航天技术上使用的氢氧燃料电池具有高能,轻便和不污染环境等优点。氢氧燃料电池有酸式和碱式两种,它们放电时的电池总反应式都可表示为:
 。
。①酸式氢氧燃料电池的电解质是硫酸,其正极的电极反应式为
②酸式氢氧燃料电池,工作一段时间后,电解质溶液的
 将
将(5)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压,电池总反应式为:
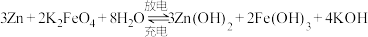 ,负极为
,负极为 向
向
您最近一年使用:0次

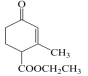 中含有的官能团名称是
中含有的官能团名称是

