钠和氯的化合物常用于化工生产与生活中。
(1)将一小块钠放在水平放置的试管中部,用酒精灯加热至充分反应,化学方程式为_______ 。将试管冷却后加水,发生反应的离子方程式为_______ 。
(2)实验室欲用NaOH固体配制1.0mol/L的NaOH溶液480mL。
①完成本实验需要用托盘天平称量NaOH_______ g。
②在配制过程中,若其他操作都正确,下列操作会使浓度偏高的是_______ (填序号)。
A.定容时仰视刻度线 B.未冷就转移溶液
C.未洗涤烧杯和玻璃棒 D.NaOH已部分变质
(3) 将逐渐用来取代
将逐渐用来取代 成为自来水的消毒剂。已知
成为自来水的消毒剂。已知 是一种易溶于水难溶于有机物的气体,
是一种易溶于水难溶于有机物的气体, 等卤素单质在水中溶解度远小于在有机溶剂
等卤素单质在水中溶解度远小于在有机溶剂 中的溶解度。制备
中的溶解度。制备 的原理为
的原理为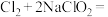
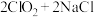 。实验装置如下图:
。实验装置如下图:

①装置A中发生反应的化学方程式为_______ 。
②E中加入的试剂可以是_______ (任意填一种)
③F用于收集 ,可选用
,可选用_______ (气流均左进右出)

④ 在消毒过程中被还原为
在消毒过程中被还原为 。
。 消毒效率是
消毒效率是 的
的_______ 倍。(消毒效率:单位质量消毒剂得到电子数,答案保留到小数点后一位。)
(1)将一小块钠放在水平放置的试管中部,用酒精灯加热至充分反应,化学方程式为
(2)实验室欲用NaOH固体配制1.0mol/L的NaOH溶液480mL。
①完成本实验需要用托盘天平称量NaOH
②在配制过程中,若其他操作都正确,下列操作会使浓度偏高的是
A.定容时仰视刻度线 B.未冷就转移溶液
C.未洗涤烧杯和玻璃棒 D.NaOH已部分变质
(3)
 将逐渐用来取代
将逐渐用来取代 成为自来水的消毒剂。已知
成为自来水的消毒剂。已知 是一种易溶于水难溶于有机物的气体,
是一种易溶于水难溶于有机物的气体, 等卤素单质在水中溶解度远小于在有机溶剂
等卤素单质在水中溶解度远小于在有机溶剂 中的溶解度。制备
中的溶解度。制备 的原理为
的原理为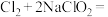
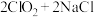 。实验装置如下图:
。实验装置如下图:
①装置A中发生反应的化学方程式为
②E中加入的试剂可以是
③F用于收集
 ,可选用
,可选用
④
 在消毒过程中被还原为
在消毒过程中被还原为 。
。 消毒效率是
消毒效率是 的
的
更新时间:2023-01-13 12:28:54
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】某实验小组在实验室用MnO2和浓盐酸制取Cl2,并验证Cl2的性质。实验装置及所用药品(部分)如图所示:

回答下列问题:
(1)上述制取Cl2装置的连接顺序为:发生装置→____ →收集装置→____ 。
(2)A中选用的装置为____ (填“甲”或“乙”),反应的化学方程式为____ 。盛装浓盐酸的仪器名称是____ ,滴加盐酸时,在旋开旋钮之前需进行的操作是____ 。

(3)通过观察B中现象说明Cl2具有的性质有____ 。
(4)E中反应的离子方程式为____ 。
(5)实验室使用D装置收集氯气,而不用图1装置的原因是____ 。

(6)若要验证干燥氯气不具有漂白作用,可将图2所示装置(可重复使用)连接到原实验装置中,连接的最佳位置是____ (选填序号)。

①A、B间 ②B、C间 ③C、D间
(7)若常温常压下生成1LCl2,理论上需要MnO2的质量为____ g。(已知常温常压下气体的摩尔体积Vm≈24.5L/mol;计算结果保留两位小数)

回答下列问题:
(1)上述制取Cl2装置的连接顺序为:发生装置→
(2)A中选用的装置为

(3)通过观察B中现象说明Cl2具有的性质有
(4)E中反应的离子方程式为
(5)实验室使用D装置收集氯气,而不用图1装置的原因是

(6)若要验证干燥氯气不具有漂白作用,可将图2所示装置(可重复使用)连接到原实验装置中,连接的最佳位置是

①A、B间 ②B、C间 ③C、D间
(7)若常温常压下生成1LCl2,理论上需要MnO2的质量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下图所涉及的物质均为中学化学中的常见物质,其中:①C、D、E、F都为单质,其余为化合物;②C、D、E在常温下为气体,其它物质为固体或液体;③A、I两种化合物的焰色反应分别为紫色和黄色;④反应①、②中的一些生成物已经略去,有些反应的条件未列出,它们存在如下转化关系。

(1)写出有关物质的化学式:A_______ ,D________ ,F_______ ,I________ 。
(2)指出MnO2在相关反应中的作用:反应①中是_______ 剂,反应②中是_______ 剂。
(3)写出B与MnO2共热获得D的化学方程式__________________________________ 。

(1)写出有关物质的化学式:A
(2)指出MnO2在相关反应中的作用:反应①中是
(3)写出B与MnO2共热获得D的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】氯苯在染料、医药工业中常用于制造苯酚、硝基氯苯、苯胺、硝基苯酚等有机中间体。实验室中制备氯苯的装置如图所示 其中夹持仪器已略去
其中夹持仪器已略去 。
。
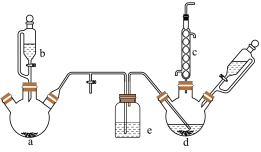
请回答下列问题:
(1)仪器a中盛有 晶体,仪器b中盛有浓盐酸,打开仪器b中的活塞,使浓盐酸缓缓滴下,可观察到仪器a内的现象是
晶体,仪器b中盛有浓盐酸,打开仪器b中的活塞,使浓盐酸缓缓滴下,可观察到仪器a内的现象是___________ ,用离子方程式表示产生该现象的原因:___________ 。
(2)仪器b外侧的细玻璃导管的作用是___________ 。
(3)仪器d中盛有苯、 粉末,仪器a中生成的
粉末,仪器a中生成的 经过仪器e进入仪器d中。
经过仪器e进入仪器d中。
①仪器e盛装的试剂名称是___________ 。
②仪器d中的反应进行过程中,应保持温度在40~60℃之间,以减少副反应的发生。仪器d的加热方式最好采用___________ 加热。
(4)仪器c的作用是___________ 。
(5)该方法制备的氯苯中含有很多杂质。在工业生产中,先通过水洗除去 、
、 及部分
及部分 ,然后通过碱洗除去其余
,然后通过碱洗除去其余 ,碱洗后通过分液得到含氯苯的有机混合物,混合物成分及各成分的沸点如下表所示:
,碱洗后通过分液得到含氯苯的有机混合物,混合物成分及各成分的沸点如下表所示:
①碱洗前先进行水洗的目的是___________ 。
②从该有机混合物中提取氯苯时,采用蒸馏方法,收集___________ ℃左右的馏分。
 其中夹持仪器已略去
其中夹持仪器已略去 。
。
请回答下列问题:
(1)仪器a中盛有
 晶体,仪器b中盛有浓盐酸,打开仪器b中的活塞,使浓盐酸缓缓滴下,可观察到仪器a内的现象是
晶体,仪器b中盛有浓盐酸,打开仪器b中的活塞,使浓盐酸缓缓滴下,可观察到仪器a内的现象是(2)仪器b外侧的细玻璃导管的作用是
(3)仪器d中盛有苯、
 粉末,仪器a中生成的
粉末,仪器a中生成的 经过仪器e进入仪器d中。
经过仪器e进入仪器d中。①仪器e盛装的试剂名称是
②仪器d中的反应进行过程中,应保持温度在40~60℃之间,以减少副反应的发生。仪器d的加热方式最好采用
(4)仪器c的作用是
(5)该方法制备的氯苯中含有很多杂质。在工业生产中,先通过水洗除去
 、
、 及部分
及部分 ,然后通过碱洗除去其余
,然后通过碱洗除去其余 ,碱洗后通过分液得到含氯苯的有机混合物,混合物成分及各成分的沸点如下表所示:
,碱洗后通过分液得到含氯苯的有机混合物,混合物成分及各成分的沸点如下表所示:| 有机物 | 苯 | 氯苯 | 邻二氯苯 | 间二氯苯 | 对二氯苯 |
| 沸点/℃ | 80.0 | 132.2 | 180.4 | 172.0 | 173.4 |
②从该有机混合物中提取氯苯时,采用蒸馏方法,收集
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】置换反应的通式可表示为:单质甲+化合物A 单质乙+化合物B。请回答下列问题:
单质乙+化合物B。请回答下列问题:
(1)若甲为黄绿色气体,单质乙能使淀粉溶液变蓝色,则该反应的离子方程式为__ 。
(2)若甲为金属,其焰色为黄色,化合物B为一种常见的强碱,则该反应的化学方程式为__ 。
(3)若单质乙是黑色非金属固体单质,化合物B是优质的耐高温材料,则该反应的化学方程式为__ 。
(4)若化合物A可作光导纤维材料,乙为非金属半导体材料,则该反应的化学方程式为__ 。
 单质乙+化合物B。请回答下列问题:
单质乙+化合物B。请回答下列问题:(1)若甲为黄绿色气体,单质乙能使淀粉溶液变蓝色,则该反应的离子方程式为
(2)若甲为金属,其焰色为黄色,化合物B为一种常见的强碱,则该反应的化学方程式为
(3)若单质乙是黑色非金属固体单质,化合物B是优质的耐高温材料,则该反应的化学方程式为
(4)若化合物A可作光导纤维材料,乙为非金属半导体材料,则该反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】如图所示,A是固体金属单质,燃烧时火焰呈黄色且生成物为淡黄色固体B。请回答下列问题:
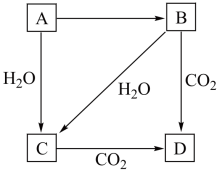
(1)写出A、B的化学式:A______ ,B______ 。
(2)写出下列转化的化学方程式:
①A→C______ 。
②B→D______ 。

(1)写出A、B的化学式:A
(2)写出下列转化的化学方程式:
①A→C
②B→D
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】纯碱是一种非常重要的化工原料,在玻璃、肥料、合成洗涤剂等工业中有着广泛的应用。
(1)工业上“侯氏制碱法”以NaCl、 、
、 及水等为原料制备纯碱,其反应原理为:
及水等为原料制备纯碱,其反应原理为: 。生产纯碱的工艺流程示意图如下:
。生产纯碱的工艺流程示意图如下:

请回答下列问题:
①析出的 晶体中可能含有少量氯离子杂质,检验该晶体中是否含有氯离子杂质的操作方法是:
晶体中可能含有少量氯离子杂质,检验该晶体中是否含有氯离子杂质的操作方法是:___________ 。
②该工艺流程中可回收再利用的物质是___________ 。
(2)实验室需要240mL2.00mol/L的 溶液:
溶液:
①所用仪器除天平、烧杯、药匙、玻璃棒、胶头滴管外还有___________ (填仪器名称);
②下列操作会造成所配溶液的浓度偏高的是___________ (填序号)
a.定容时俯视刻度线
b.容量瓶内壁附有水珠而未干燥处理
c.发现凹液面超过刻度线,立即将多余溶液吸出
d.溶液转移至容量瓶中后没有洗涤烧杯
(3)常温下在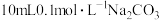 溶液中逐滴加入
溶液中逐滴加入 溶液20mL,溶液中含碳元素的各种微粒的质量分数(纵轴)随溶液pH变化的部分情况如下图所示。
溶液20mL,溶液中含碳元素的各种微粒的质量分数(纵轴)随溶液pH变化的部分情况如下图所示。

根据图示回答下列问题:
①在同一溶液中, 、
、 、
、
___________ (填“能”或“不能”)大量共存。
②将 和
和 混合并配成溶液,向溶液中滴加
混合并配成溶液,向溶液中滴加 稀盐酸。下列图像能正确表示加入盐酸的体积和生成
稀盐酸。下列图像能正确表示加入盐酸的体积和生成 的物质的量的关系的是
的物质的量的关系的是___________ (填字母)。

(4)若称取16.8g纯净的 固体,加热一段时间后,剩余固体的质量为13.7g。如果把剩余的固体全部加入到
固体,加热一段时间后,剩余固体的质量为13.7g。如果把剩余的固体全部加入到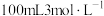 的盐酸中充分反应。求溶液中剩余的盐酸的物质的量浓度
的盐酸中充分反应。求溶液中剩余的盐酸的物质的量浓度___________ (设溶液的体积变化及盐酸的挥发忽略不计)(写出计算过程)。
(1)工业上“侯氏制碱法”以NaCl、
 、
、 及水等为原料制备纯碱,其反应原理为:
及水等为原料制备纯碱,其反应原理为: 。生产纯碱的工艺流程示意图如下:
。生产纯碱的工艺流程示意图如下:
请回答下列问题:
①析出的
 晶体中可能含有少量氯离子杂质,检验该晶体中是否含有氯离子杂质的操作方法是:
晶体中可能含有少量氯离子杂质,检验该晶体中是否含有氯离子杂质的操作方法是:②该工艺流程中可回收再利用的物质是
(2)实验室需要240mL2.00mol/L的
 溶液:
溶液:①所用仪器除天平、烧杯、药匙、玻璃棒、胶头滴管外还有
②下列操作会造成所配溶液的浓度偏高的是
a.定容时俯视刻度线
b.容量瓶内壁附有水珠而未干燥处理
c.发现凹液面超过刻度线,立即将多余溶液吸出
d.溶液转移至容量瓶中后没有洗涤烧杯
(3)常温下在
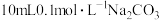 溶液中逐滴加入
溶液中逐滴加入 溶液20mL,溶液中含碳元素的各种微粒的质量分数(纵轴)随溶液pH变化的部分情况如下图所示。
溶液20mL,溶液中含碳元素的各种微粒的质量分数(纵轴)随溶液pH变化的部分情况如下图所示。
根据图示回答下列问题:
①在同一溶液中,
 、
、 、
、
②将
 和
和 混合并配成溶液,向溶液中滴加
混合并配成溶液,向溶液中滴加 稀盐酸。下列图像能正确表示加入盐酸的体积和生成
稀盐酸。下列图像能正确表示加入盐酸的体积和生成 的物质的量的关系的是
的物质的量的关系的是
(4)若称取16.8g纯净的
 固体,加热一段时间后,剩余固体的质量为13.7g。如果把剩余的固体全部加入到
固体,加热一段时间后,剩余固体的质量为13.7g。如果把剩余的固体全部加入到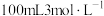 的盐酸中充分反应。求溶液中剩余的盐酸的物质的量浓度
的盐酸中充分反应。求溶液中剩余的盐酸的物质的量浓度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】Ⅰ、实验时用10 浓硫酸配制100mL1
浓硫酸配制100mL1
 溶液。
溶液。
(1)在配制过程示意图中,错误的有___________ (填序号)。

(2)下列操作导致所配制的稀硫酸的物质的量浓度偏低的是___________ (填字母)。
A.用量筒量取浓硫酸时俯视凹液面
B.将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶定容
C.容量瓶用蒸馏水洗后未干燥
D.定容时仰视液面
E.未洗涤烧杯和玻璃棒
F.转移到容量瓶的过程中,有少量的溶液溅出
G.用量筒量取浓硫酸倒入小烧杯后,用蒸馏水洗涤量筒并将洗涤液转移至小烧杯中
H.用不干燥的量筒量取浓硫酸
Ⅱ.焦亚硫酸钠含量的测定
工业焦亚硫酸钠(Na2S2O5)优质品要求质量分数 %。通过下列实验检测焦亚硫酸钠样品是否达到优质品标准。实验检测原理为:
%。通过下列实验检测焦亚硫酸钠样品是否达到优质品标准。实验检测原理为:
 (未配平)
(未配平)

准确称取 样品,快速置于预先加入
样品,快速置于预先加入 碘标准液及
碘标准液及 水的
水的 碘量瓶中,加入
碘量瓶中,加入 乙酸溶液,立即盖上瓶塞,水封,缓缓摇动溶解后,置于暗处放置
乙酸溶液,立即盖上瓶塞,水封,缓缓摇动溶解后,置于暗处放置 ;用
;用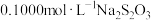 标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点,消耗Na2S2O3溶液
标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点,消耗Na2S2O3溶液 。
。
(3)滴定终点现象是___________ 。
(4)通过计算判断该样品是否为优质品。(写出计算过程)___________ 。
 浓硫酸配制100mL1
浓硫酸配制100mL1
 溶液。
溶液。(1)在配制过程示意图中,错误的有

(2)下列操作导致所配制的稀硫酸的物质的量浓度偏低的是
A.用量筒量取浓硫酸时俯视凹液面
B.将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶定容
C.容量瓶用蒸馏水洗后未干燥
D.定容时仰视液面
E.未洗涤烧杯和玻璃棒
F.转移到容量瓶的过程中,有少量的溶液溅出
G.用量筒量取浓硫酸倒入小烧杯后,用蒸馏水洗涤量筒并将洗涤液转移至小烧杯中
H.用不干燥的量筒量取浓硫酸
Ⅱ.焦亚硫酸钠含量的测定
工业焦亚硫酸钠(Na2S2O5)优质品要求质量分数
 %。通过下列实验检测焦亚硫酸钠样品是否达到优质品标准。实验检测原理为:
%。通过下列实验检测焦亚硫酸钠样品是否达到优质品标准。实验检测原理为: (未配平)
(未配平)
准确称取
 样品,快速置于预先加入
样品,快速置于预先加入 碘标准液及
碘标准液及 水的
水的 碘量瓶中,加入
碘量瓶中,加入 乙酸溶液,立即盖上瓶塞,水封,缓缓摇动溶解后,置于暗处放置
乙酸溶液,立即盖上瓶塞,水封,缓缓摇动溶解后,置于暗处放置 ;用
;用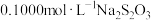 标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点,消耗Na2S2O3溶液
标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点,消耗Na2S2O3溶液 。
。(3)滴定终点现象是
(4)通过计算判断该样品是否为优质品。(写出计算过程)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】消毒剂在生活中应用非常广泛,K2FeO4、Cl2、ClO2、H2O2、NaClO是生活中不同领域的消毒剂,其中K2FeO4可用作水处理剂。下图是实验室制备K2FeO4的实验装置图,甲为制氯气的装置。
资料:K2FeO4为紫色固体,微溶于KOH,具有强氧化性。
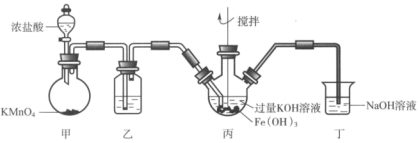
(1)在甲装置中,用KMnO4与浓盐酸反应制取氯气,反应的离子方程式为_______ ,乙中盛放的试剂是_______ ,作用是_______ 。
(2)装置丁中发生的离子反应方程式为_______ 。
(3)装置丙中发生的离子反应方程式为_______ ,当1molK2FeO4生成时,转移的电子数目为_______ 。
(4)实验需要室温下90mL2.0mol·L-1的KOH溶液
①配制KOH溶液除烧杯、量筒、玻璃棒、胶头滴管外,还需要的玻璃仪器有_______ 。
②下列有关配制过程中说法正确的是_______ (填序号)。
a.用托盘天平称量质量为11.2g的KOH
b.将称量的KOH放入容量瓶中,加90mL蒸馏水溶解
c.洗涤溶解KOH的烧杯,并将洗涤液转移至容量瓶中
d.容量瓶用蒸馏水洗净后必须干燥才能使用
e.定容时,仰视容量瓶刻度线会使配制的KOH溶液浓度偏低
f.摇匀后见液面低于刻度线,应及时加水至刻度线
资料:K2FeO4为紫色固体,微溶于KOH,具有强氧化性。

(1)在甲装置中,用KMnO4与浓盐酸反应制取氯气,反应的离子方程式为
(2)装置丁中发生的离子反应方程式为
(3)装置丙中发生的离子反应方程式为
(4)实验需要室温下90mL2.0mol·L-1的KOH溶液
①配制KOH溶液除烧杯、量筒、玻璃棒、胶头滴管外,还需要的玻璃仪器有
②下列有关配制过程中说法正确的是
a.用托盘天平称量质量为11.2g的KOH
b.将称量的KOH放入容量瓶中,加90mL蒸馏水溶解
c.洗涤溶解KOH的烧杯,并将洗涤液转移至容量瓶中
d.容量瓶用蒸馏水洗净后必须干燥才能使用
e.定容时,仰视容量瓶刻度线会使配制的KOH溶液浓度偏低
f.摇匀后见液面低于刻度线,应及时加水至刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某研究性学习小组组装了下图所示的装置制备ClO2气体(加热装置用“Δ”表示),反应原理为饱和草酸溶液与KClO3粉末在60℃时反应制得ClO2(温度过高或过低都会影响制气效率)
已知:①ClO2是一种黄绿色有刺激性气味的气体,熔点-59℃,沸点11.0℃
②草酸是酸性强于醋酸的二元弱酸,对应的钙盐(CaC2O4)不溶于醋酸,能溶于强酸,它还是一种还原性较强的物质。

(1)配平制备ClO2的化学方程式:
_____ KClO3+_____ H2C2O4 ——____ KHCO3+____ ClO2↑
(2)A装置中还缺少的一样仪器名称是___________ ,B装置的作用是________________ 。
(3)C装置吸收尾气后,溶液中含有NaOH、NaClO2、NaClO3等溶质,小组成员认为C中还可能含有Na2CO3,试分析可能的原因是_______________________ 。
(4)小组成员查资料得知“菠菜中富含可溶性草酸盐和碳酸盐”,他将菠菜研磨成汁、热水浸泡、过滤得到溶液,调节溶液呈碱性,加入足量的CaCl2溶液,产生白色沉淀,过滤、洗涤,沉淀备用,对生成的沉淀进行探究。
①提出合理假设
假设1:只存在CaCO3;
假设2:既存在CaCO3,也存在CaC2O4;
假设3:___________________________ 。
②基于假设2,设计实验方案,进行实验。请在答题卷上写出实验步骤以及预期现象和结论。限选 实验试剂:1 mol·L-1 H2SO4、0.1 mol·L-1 HCl、0.01 mol·L-1 KMnO4、澄清石灰水。
已知:①ClO2是一种黄绿色有刺激性气味的气体,熔点-59℃,沸点11.0℃
②草酸是酸性强于醋酸的二元弱酸,对应的钙盐(CaC2O4)不溶于醋酸,能溶于强酸,它还是一种还原性较强的物质。

(1)配平制备ClO2的化学方程式:
(2)A装置中还缺少的一样仪器名称是
(3)C装置吸收尾气后,溶液中含有NaOH、NaClO2、NaClO3等溶质,小组成员认为C中还可能含有Na2CO3,试分析可能的原因是
(4)小组成员查资料得知“菠菜中富含可溶性草酸盐和碳酸盐”,他将菠菜研磨成汁、热水浸泡、过滤得到溶液,调节溶液呈碱性,加入足量的CaCl2溶液,产生白色沉淀,过滤、洗涤,沉淀备用,对生成的沉淀进行探究。
①提出合理假设
假设1:只存在CaCO3;
假设2:既存在CaCO3,也存在CaC2O4;
假设3:
②基于假设2,设计实验方案,进行实验。请在答题卷上写出实验步骤以及预期现象和结论。
| 实验步骤 | 预期现象和结论 |
步骤1:取少量沉淀于试管中,加入 | |
步骤2: |
您最近一年使用:0次
【推荐2】已知三氯化铁的熔点为306℃,沸点为315℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解,并可作为过氧化氢分解的催化剂。某学习小组的同学对氯气与铁的反应及产物做了如图探究实验:

(1)装碱石灰的仪器名称是____ 。
(2)碱石灰的作用是____ 。
(3)本实验中,装置从左向右合理的连接顺序为:____
a→__________→__________→__________→__________→__________→__________→__________。
(4)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡)。充分反应后,进行如图实验:
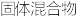








已知红色褪去的同时有气体生成,经检验为O2。
该小组内的同学们对红色褪去的原因提出了三种假设:
假设Ⅰ:H2O2还原Fe3+,使其转变为Fe2+;
假设Ⅱ:H2O2分解生成O2,O2氧化试剂X;
假设Ⅲ:____ 。
并对假设进行了以下实验探究:
实验①:取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;第二份滴加试剂X,溶液出现红色;第三份滴加稀盐酸和BaCl2溶液,产生白色沉淀。
实验②:另取同浓度的FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化。
回答下列问题:实验①说明假设____ 不正确;实验②的目的是____ ;由实验①②得出假设____ 是正确的。

(1)装碱石灰的仪器名称是
(2)碱石灰的作用是
(3)本实验中,装置从左向右合理的连接顺序为:
a→__________→__________→__________→__________→__________→__________→__________。
(4)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡)。充分反应后,进行如图实验:
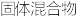








已知红色褪去的同时有气体生成,经检验为O2。
该小组内的同学们对红色褪去的原因提出了三种假设:
假设Ⅰ:H2O2还原Fe3+,使其转变为Fe2+;
假设Ⅱ:H2O2分解生成O2,O2氧化试剂X;
假设Ⅲ:
并对假设进行了以下实验探究:
实验①:取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;第二份滴加试剂X,溶液出现红色;第三份滴加稀盐酸和BaCl2溶液,产生白色沉淀。
实验②:另取同浓度的FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化。
回答下列问题:实验①说明假设
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某校化学实验小组为了证明铜与稀硝酸反应产生一氧化氮,用如图所示装置进行实验(加热装置和夹持装置均已略去,装置气密性良好,F是用于鼓入空气的双连打气球)。
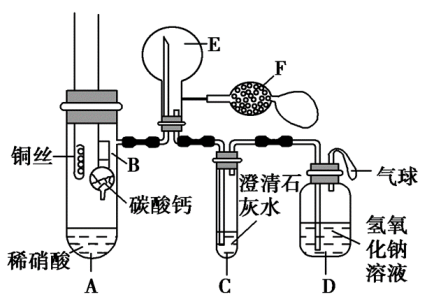
实验操作及现象:
试回答下列问题:
(1)操作I中产生气体的化学式为_______ 。操作I的目的是_______ 。
(2)操作III中A装置中产生无色气体;E中出现浅红色的原因_______ ,(用化学方程式表示)
(3)操作V中沉淀溶解的离子方程式为_______ 。
(4)当操作III使A中溶液增加2.64克时,理论上将A中产生的无色气体全部转化为硝酸,所需O2的物质的量为_______ ; 此过程转移电子数目为_______ 。
(5)尽管有操作I,但操作III中E装置内还是会出现浅红棕色原因是_______ 。(从实验装置设计分析)

实验操作及现象:
| 实验操作 | 现象 |
| I.将B装置下移,使碳酸钙与稀硝酸接触 | 产生气体 |
| II.当C装置中产生白色沉淀时,立刻将B装置上提 | |
| III.将A装置中铜丝放入稀硝酸中,给A装置微微加热 | A装置中产生无色气体,E装置中开始时出现浅红棕色气体 |
| IV.用F装置向E装置中鼓入空气 | E装置中气体颜色逐渐加深 |
| V.一段时间后 | C装置中白色沉淀溶解 |
(1)操作I中产生气体的化学式为
(2)操作III中A装置中产生无色气体;E中出现浅红色的原因
(3)操作V中沉淀溶解的离子方程式为
(4)当操作III使A中溶液增加2.64克时,理论上将A中产生的无色气体全部转化为硝酸,所需O2的物质的量为
(5)尽管有操作I,但操作III中E装置内还是会出现浅红棕色原因是
您最近一年使用:0次




