某同学称取 草酸亚铁晶体
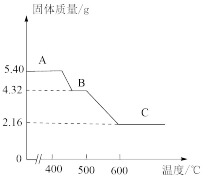
草酸亚铁晶体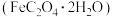 在氩气氛围中进行热重分析,得到固体的质量随温度变化的曲线如图所示。
在氩气氛围中进行热重分析,得到固体的质量随温度变化的曲线如图所示。
(1) 样品在氩气氛围中进行热重分析的原因是
样品在氩气氛围中进行热重分析的原因是______________________ 。
(2)分析数据,根据信息写出B对应产物的化学式:______________________ 。
(3) 时剩余固体只含一种铁的氧化物,且生成两种物质的量相等的气体。试写出B→C过程中发生反应的化学方程式:
时剩余固体只含一种铁的氧化物,且生成两种物质的量相等的气体。试写出B→C过程中发生反应的化学方程式:______________________ 。
 草酸亚铁晶体
草酸亚铁晶体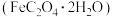 在氩气氛围中进行热重分析,得到固体的质量随温度变化的曲线如图所示。
在氩气氛围中进行热重分析,得到固体的质量随温度变化的曲线如图所示。
(1)
 样品在氩气氛围中进行热重分析的原因是
样品在氩气氛围中进行热重分析的原因是(2)分析数据,根据信息写出B对应产物的化学式:
(3)
 时剩余固体只含一种铁的氧化物,且生成两种物质的量相等的气体。试写出B→C过程中发生反应的化学方程式:
时剩余固体只含一种铁的氧化物,且生成两种物质的量相等的气体。试写出B→C过程中发生反应的化学方程式:
更新时间:2023-01-14 17:51:49
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】苯甲酸(无色针状晶体,熔点122.4℃)可广泛用于医药、染料载体、香料等,实验室用甲苯和高锰酸钾制备苯甲酸。反应方程式如图:
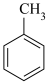 +2KMnO4
+2KMnO4
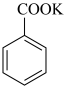 (苯甲酸钾)+KOH+2MnO2↓+H2O;
(苯甲酸钾)+KOH+2MnO2↓+H2O;
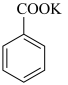 +HCl
+HCl
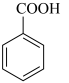 (苯甲酸)+KCl
(苯甲酸)+KCl
已知有关化合物的相关数据如表所示:
苯甲酸在100g水中的溶解度:0.18g(4℃),0.27g(18℃),2.2g(75℃)。
实验步骤:
i.合成:如图(固定及加热装置略去)所示,在三颈烧瓶中加入4.23mL甲苯和100mL蒸馏水,瓶口装上温度计、电动搅拌器、冷凝管,慢慢开启电动搅拌器,加热至沸腾。经冷凝管上口分批加入21.30g高锰酸钾(过量),继续煮沸至甲苯层消失,回流液中不再出现油珠为止,得到反应混合物。
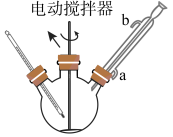
ii.对反应混合物进行分离:①趁热过滤→②洗涤滤渣→③合并滤液和洗涤液→④冷却→⑤盐酸酸化→⑥过滤。
iii.对粗产品苯甲酸进行提纯:①沸水溶解→②活性炭脱色→③趁热过滤→④___________→⑤过滤→⑥洗涤→⑦干燥。
请回答下列有关问题:
(1)根据上述实验药品的用量,三颈烧瓶的最适宜规格为___________(填标号)。
(2)冷凝管b处水流方向是___________ ( “进水”或“出水”)。
(3)高锰酸钾需要分批加入,请用化学反应速率观点说明理由___________ 。
(4)对粗产品苯甲酸进行提纯过程中, “③趁热过滤”的目的是___________ ; 可证明“⑥洗涤”步骤已洗涤干净的方法是___________ 。
(5)干燥后称量得苯甲酸2.44g,则苯甲酸的产率为___________ 。(保留两位有效数字)
 +2KMnO4
+2KMnO4
 (苯甲酸钾)+KOH+2MnO2↓+H2O;
(苯甲酸钾)+KOH+2MnO2↓+H2O; +HCl
+HCl
 (苯甲酸)+KCl
(苯甲酸)+KCl已知有关化合物的相关数据如表所示:
| 化合物 | 相对分子质量 | 密度(g•cm﹣3) | 溶解性 | 沸点(℃) |
| 甲苯 | 92 | 0.87 | 难溶于水 | 110.0 |
| 苯甲酸钾 | 160 | ﹣ | 易溶于水 | ﹣ |
| 苯甲酸 | 122 | 1.26 | 微溶于水 | 248.0 |
实验步骤:
i.合成:如图(固定及加热装置略去)所示,在三颈烧瓶中加入4.23mL甲苯和100mL蒸馏水,瓶口装上温度计、电动搅拌器、冷凝管,慢慢开启电动搅拌器,加热至沸腾。经冷凝管上口分批加入21.30g高锰酸钾(过量),继续煮沸至甲苯层消失,回流液中不再出现油珠为止,得到反应混合物。

ii.对反应混合物进行分离:①趁热过滤→②洗涤滤渣→③合并滤液和洗涤液→④冷却→⑤盐酸酸化→⑥过滤。
iii.对粗产品苯甲酸进行提纯:①沸水溶解→②活性炭脱色→③趁热过滤→④___________→⑤过滤→⑥洗涤→⑦干燥。
请回答下列有关问题:
(1)根据上述实验药品的用量,三颈烧瓶的最适宜规格为___________(填标号)。
| A.100mL | B.250mL | C.500mL | D.1000mL |
(3)高锰酸钾需要分批加入,请用化学反应速率观点说明理由
(4)对粗产品苯甲酸进行提纯过程中, “③趁热过滤”的目的是
(5)干燥后称量得苯甲酸2.44g,则苯甲酸的产率为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐2】白色固体A是由四种元素组成的化合物,为探究其组成和性质,进行了如下实验:
请回答:
(1)组成A的四种元素是___________ (填元素符号),A的化学式是___________ 。
(2)写出过量的气体B通入Ca(OH)2溶液的离子方程式:___________ 。
(3)固体A与稀硝酸反应的化学方程式是___________ 。

请回答:
(1)组成A的四种元素是
(2)写出过量的气体B通入Ca(OH)2溶液的离子方程式:
(3)固体A与稀硝酸反应的化学方程式是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】为充分利用资源,变废为宝,可从废旧CPU[含Au(金)、Ag、Cu和Pt(铂)]中回收Au,其化工流程如图:
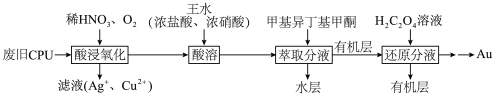
回答下列问题
(1)“酸浸氧化”中,为了提高反应速率,可以采取的措施是___________ (写出一种即可)。
(2)“酸浸氧化”中,通入氧气的目的是___________ 。
(3)“酸溶”时,Pt、Au分别转化为H2PtCl6和HAuCl4,同时有NO生成。Pt溶解的化学方程式是___________ 。
(4)“萃取分液”后的“水层”中可回收的金属是___________ 。
(5)从“还原分液”后的“有机层”中回收甲基异丁基甲酮,采用的方法是___________ 。
(6)理论上消耗1mol草酸(H2C2O4)可得到Au的质量为___________ g(结果保留一位小数)。
(7)提取“滤液”中的Ag+会涉及反应AgCl(s)+2NH3 [Ag(NH3)2]++Cl-,则该反应的平衡常数K的值为
[Ag(NH3)2]++Cl-,则该反应的平衡常数K的值为 ___________ 。已知:①[Ag(NH3)2]+ Ag++2NH3 K1=6×10-8;②Ksp(AgCl)=1.8×10-10。
Ag++2NH3 K1=6×10-8;②Ksp(AgCl)=1.8×10-10。

回答下列问题
(1)“酸浸氧化”中,为了提高反应速率,可以采取的措施是
(2)“酸浸氧化”中,通入氧气的目的是
(3)“酸溶”时,Pt、Au分别转化为H2PtCl6和HAuCl4,同时有NO生成。Pt溶解的化学方程式是
(4)“萃取分液”后的“水层”中可回收的金属是
(5)从“还原分液”后的“有机层”中回收甲基异丁基甲酮,采用的方法是
(6)理论上消耗1mol草酸(H2C2O4)可得到Au的质量为
(7)提取“滤液”中的Ag+会涉及反应AgCl(s)+2NH3
 [Ag(NH3)2]++Cl-,则该反应的平衡常数K的值为
[Ag(NH3)2]++Cl-,则该反应的平衡常数K的值为  Ag++2NH3 K1=6×10-8;②Ksp(AgCl)=1.8×10-10。
Ag++2NH3 K1=6×10-8;②Ksp(AgCl)=1.8×10-10。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】隔绝空气加热至 时硫酸亚铁铵
时硫酸亚铁铵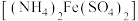 能完全分解,分解产物中含有铁氧化物、硫氧化物、氨气和水蒸气等。
能完全分解,分解产物中含有铁氧化物、硫氧化物、氨气和水蒸气等。
[实验探究]某化学小组选用如图所示部分装置进行分步实验(夹持装置略)。
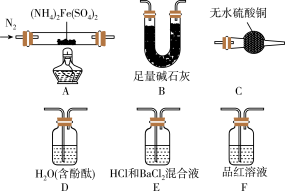
实验I:甲同学为探究分解产物中的硫氧化物是 还是
还是 ,连接装置
,连接装置 进行实验。
进行实验。
(1)实验过程中观察到:E中没有明显现象,F中溶液褪色,据此得出的结论是___________ 。
(2)B的作用是___________ 。
实验II:验证分解产物中含有水蒸气和氨气,并探究残留固体成分。
(3)所选用装置的正确连接顺序为___________ (填装置的字母序号)。
(4)证明有水蒸气生成的实验现象为___________ 。
(5)证明有氨气生成的实验现象为___________ 。
(6)实验证明 受热分解除上述产物外,还有
受热分解除上述产物外,还有 生成,写出A中反应的化学方程式
生成,写出A中反应的化学方程式___________ 。
(7)乙同学实验结束称量C装置,发现质量增加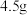 ,那么原本硫酸亚铁铵的物质的量为
,那么原本硫酸亚铁铵的物质的量为____ 。
 时硫酸亚铁铵
时硫酸亚铁铵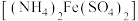 能完全分解,分解产物中含有铁氧化物、硫氧化物、氨气和水蒸气等。
能完全分解,分解产物中含有铁氧化物、硫氧化物、氨气和水蒸气等。[实验探究]某化学小组选用如图所示部分装置进行分步实验(夹持装置略)。

实验I:甲同学为探究分解产物中的硫氧化物是
 还是
还是 ,连接装置
,连接装置 进行实验。
进行实验。(1)实验过程中观察到:E中没有明显现象,F中溶液褪色,据此得出的结论是
(2)B的作用是
实验II:验证分解产物中含有水蒸气和氨气,并探究残留固体成分。
(3)所选用装置的正确连接顺序为
(4)证明有水蒸气生成的实验现象为
(5)证明有氨气生成的实验现象为
(6)实验证明
 受热分解除上述产物外,还有
受热分解除上述产物外,还有 生成,写出A中反应的化学方程式
生成,写出A中反应的化学方程式(7)乙同学实验结束称量C装置,发现质量增加
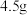 ,那么原本硫酸亚铁铵的物质的量为
,那么原本硫酸亚铁铵的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】硫酸铁铵[aFe2(SO4) 3·b(NH4) 2SO4·cH2O]广泛用于城镇生活饮用水、工业循环水的净化处理等。某化工厂以硫酸亚铁(含少量硝酸钙)和硫酸铵为原料,设计了如下工艺流程制取硫酸铁铵。

请回答下列问题:
(1)下列物质中最适合的氧化剂B是____________________ ;
a.NaClO b.H2O2c.KMnO4d.K2Cr2O7
反应的离子方程式____________________ 。
(2)上述流程中,用足量最适合的氧化剂B氧化之后和加热蒸发之前,需取少量检验Fe2+是否已全部被氧化,能否用酸性的KMnO4溶液?并说明理由____________________ 。(可用文字或方程式说明)
(3)检验硫酸铁铵中NH 的方法是
的方法是____________________ 。
(4)称取14.00 g所得样品,将其溶于水配制成100 mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到2.14 g沉淀;向另一份溶液中加入含0.05 mol Ba (NO3)2的溶液,恰好完全反应。则该硫酸铁铵的化学式为____________________ 。

请回答下列问题:
(1)下列物质中最适合的氧化剂B是
a.NaClO b.H2O2c.KMnO4d.K2Cr2O7
反应的离子方程式
(2)上述流程中,用足量最适合的氧化剂B氧化之后和加热蒸发之前,需取少量检验Fe2+是否已全部被氧化,能否用酸性的KMnO4溶液?并说明理由
(3)检验硫酸铁铵中NH
 的方法是
的方法是(4)称取14.00 g所得样品,将其溶于水配制成100 mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到2.14 g沉淀;向另一份溶液中加入含0.05 mol Ba (NO3)2的溶液,恰好完全反应。则该硫酸铁铵的化学式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
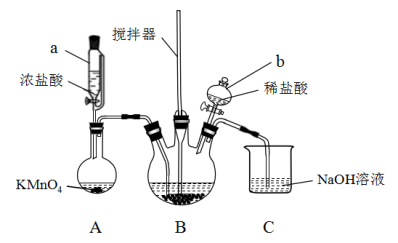
【推荐3】氯化铁在金属蚀刻、污水处理等方面有广泛应用。某兴趣小组以废铁屑为原料,用如图所示装置制备FeCl3·6H2O。
已知:FeCl3易溶于水、甲醇、乙醇,不溶于甘油。
实验步骤:
I.废铁屑的净化:取一只小烧杯,放入约5 g废铁屑,向其中注入15 mL 1 mol·L−1
Na2CO3溶液,浸泡数分钟后,分离出铁屑,洗净、晾干。
II.FeCl2溶液的制备:将处理后的废铁屑加入装置B的三颈烧瓶中,缓慢加入适当过量的稀盐酸,得到含FeCl2的混合液。
III.FeCl3溶液的制备:由装置A制备氯气,向FeCl2的混合液中缓慢通入足量的氯气。
IV.FeCl3·6H2O产品的分离提纯:将三颈烧瓶中的FeCl3混合液转移出来,经蒸发浓缩、冷却结晶、过滤、洗涤、重结晶、干燥,得到FeCl3·6H2O产品。
V.FeCl3·6H2O产品的纯度测定:用碘量法滴定并计算。
请回答:
(1)步骤I,从碳酸钠溶液中分离出铁屑的方法是___________ 。
(2)下列有关装置仪器的说法不正确 的是___________ 。
A.装置A、B之间应加装一个盛有饱和食盐水的洗气瓶
B.装置B中,搅拌器的作用是使反应混合物充分接触
C.装置C中,NaOH溶液的作用是吸收逸出的氯气,防止空气污染
D.仪器a和仪器b的功能相同,操作方法也相同
(3)下列说法正确的是___________ 。
A.步骤II,稀盐酸适当过量的目的是提高铁屑的利用率并抑制水解
B.步骤III,可用K4Fe(CN)6溶液检验“含有FeCl3的混合液”中是否存在Fe2+
C.步骤IV ,蒸发浓缩要适度,浓缩度太小产率偏低,浓缩度太大纯度偏低
D.步骤IV,在冷却结晶后的固液混合物中加入甘油可提高产率
(4)已知碘量法的滴定反应:I2 + 2Na2S2O3 = 2NaI + Na2S4O6
①测定FeCl3·6H2O产品纯度的步骤选项如下,请排序(操作不能重复使用):用电子天平称取5.000 g粗产品→配成250mL溶液→_____ →_____ →_____ →_____ →计算FeCl3·6H2O纯度。
a.加入稍过量的KI溶液,充分反应
b.用碱式滴定管取出25.00 mL待测液于锥形瓶中
c.用淀粉溶液作指示剂,用c mol·L−1 Na2S2O3标准溶液滴定
d.平行滴定三次,消耗标准溶液的体积平均值为V mL
e.用移液管取出25.00 mL待测液于锥形瓶中
②如果碱式滴定管的乳胶管中有气泡,会导致滴定溶液体积不准确,因此,必须排出乳胶管中的气泡。具体操作是:把乳胶管向上弯曲,___________ ,使溶液从尖嘴快速喷出,气泡即可随之排掉。(请在横线上补全操作)
③实验中测得FeCl3·6H2O的产品纯度偏低,若操作过程无误,请从物质性质和反应原理角度分析,可能的原因是___________ (写出一种即可)。

已知:FeCl3易溶于水、甲醇、乙醇,不溶于甘油。
实验步骤:
I.废铁屑的净化:取一只小烧杯,放入约5 g废铁屑,向其中注入15 mL 1 mol·L−1
Na2CO3溶液,浸泡数分钟后,分离出铁屑,洗净、晾干。
II.FeCl2溶液的制备:将处理后的废铁屑加入装置B的三颈烧瓶中,缓慢加入适当过量的稀盐酸,得到含FeCl2的混合液。
III.FeCl3溶液的制备:由装置A制备氯气,向FeCl2的混合液中缓慢通入足量的氯气。
IV.FeCl3·6H2O产品的分离提纯:将三颈烧瓶中的FeCl3混合液转移出来,经蒸发浓缩、冷却结晶、过滤、洗涤、重结晶、干燥,得到FeCl3·6H2O产品。
V.FeCl3·6H2O产品的纯度测定:用碘量法滴定并计算。
请回答:
(1)步骤I,从碳酸钠溶液中分离出铁屑的方法是
(2)下列有关装置仪器的说法
A.装置A、B之间应加装一个盛有饱和食盐水的洗气瓶
B.装置B中,搅拌器的作用是使反应混合物充分接触
C.装置C中,NaOH溶液的作用是吸收逸出的氯气,防止空气污染
D.仪器a和仪器b的功能相同,操作方法也相同
(3)下列说法正确的是
A.步骤II,稀盐酸适当过量的目的是提高铁屑的利用率并抑制水解
B.步骤III,可用K4Fe(CN)6溶液检验“含有FeCl3的混合液”中是否存在Fe2+
C.步骤IV ,蒸发浓缩要适度,浓缩度太小产率偏低,浓缩度太大纯度偏低
D.步骤IV,在冷却结晶后的固液混合物中加入甘油可提高产率
(4)已知碘量法的滴定反应:I2 + 2Na2S2O3 = 2NaI + Na2S4O6
①测定FeCl3·6H2O产品纯度的步骤选项如下,请排序(操作不能重复使用):用电子天平称取5.000 g粗产品→配成250mL溶液→
a.加入稍过量的KI溶液,充分反应
b.用碱式滴定管取出25.00 mL待测液于锥形瓶中
c.用淀粉溶液作指示剂,用c mol·L−1 Na2S2O3标准溶液滴定
d.平行滴定三次,消耗标准溶液的体积平均值为V mL
e.用移液管取出25.00 mL待测液于锥形瓶中
②如果碱式滴定管的乳胶管中有气泡,会导致滴定溶液体积不准确,因此,必须排出乳胶管中的气泡。具体操作是:把乳胶管向上弯曲,
③实验中测得FeCl3·6H2O的产品纯度偏低,若操作过程无误,请从物质性质和反应原理角度分析,可能的原因是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】化合物X由四种元素组成。某实验小组按如图流程进行相关实验(部分产物已略去):
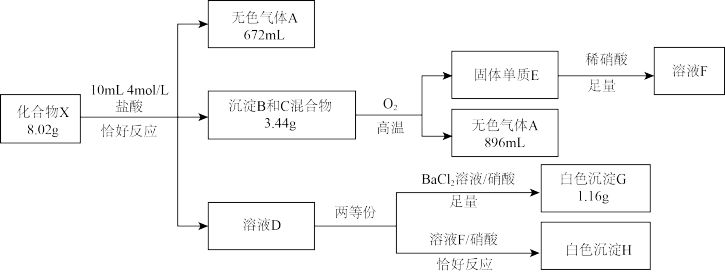
已知:无色气体A能使品红溶液褪色。沉淀B和C混合物中含两种元素,且B为黑色沉淀。溶液D中含有两种溶质,取溶液D进行焰色试验,火焰为黄色。气体体积已折算至标准状况。
请回答:
(1)组成X的四种元素为____ ;X的化学式为____ 。
(2)沉淀B和C混合物为____ (用化学式表示):写出B高温煅烧生成A和E的化学方程式____ 。
(3)气体A能与溶液F中的产物发生非氧化还原反应而生成白色沉淀,写出该反应的离子方程式____ 。
(4)有同学在溶液D中依次加入足量的硝酸钡溶液、硝酸银溶液、稀硝酸,经过滤、洗涤、干燥得到含G和H的固体混合物ag。设计实验,测定固体混合物中H的质量分数____ 。

已知:无色气体A能使品红溶液褪色。沉淀B和C混合物中含两种元素,且B为黑色沉淀。溶液D中含有两种溶质,取溶液D进行焰色试验,火焰为黄色。气体体积已折算至标准状况。
请回答:
(1)组成X的四种元素为
(2)沉淀B和C混合物为
(3)气体A能与溶液F中的产物发生非氧化还原反应而生成白色沉淀,写出该反应的离子方程式
(4)有同学在溶液D中依次加入足量的硝酸钡溶液、硝酸银溶液、稀硝酸,经过滤、洗涤、干燥得到含G和H的固体混合物ag。设计实验,测定固体混合物中H的质量分数
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】习近平总书记的“百炼钢做成了绕指柔”折射出我国钢铁工业从“跟跑”向“领跑”的蝶变。铁矿石中含铁量的测定是铁元素提炼的基础和前提。测定铁矿石中的铁含量可采用重铬酸钾法测定,其可分为三氯化钛—重铬酸钾滴定法和氯化亚锡、氯化汞—重铬酸钾滴定法,其流程如下图所示:
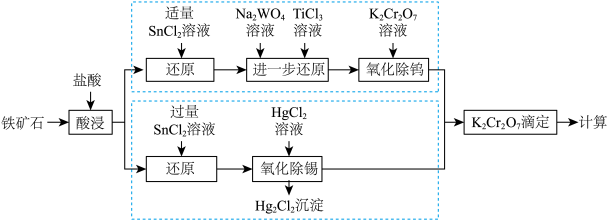
已知:i.氧化性顺序: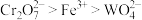 ;
;
ii.氯化汞为弱电解质,具备一定氧化性;
iii.Sn在溶液中的主要存在形式为 和
和 ;
;
iv.五价钨溶液为蓝色。
请回答下列问题:
(1)目前三氯化钛—重铬酸钾滴定法使用率更高,其主要原因为___________ 。
(2)提高“酸浸”速率可采取的措施是___________ 、___________ (任写两种)。
(3)“还原”与“氧化除锡”过程的离子反应方程式分别为___________ 、___________ 。
(4)“ 还原”溶液仍呈浅黄色,而“
还原”溶液仍呈浅黄色,而“ 还原”后溶液呈现蓝色,则蓝色溶液中铁元素的主要存在形式为
还原”后溶液呈现蓝色,则蓝色溶液中铁元素的主要存在形式为___________ , 的作用为
的作用为___________ 。
(5)现称取3.0g铁矿石进行溶矿处理,采用三氯化钛—重铬酸钾滴定法,将“氧化除钨”后溶液定容至100mL,每次取20.00mL进行滴定,平行滴定4次,数据如下:
①分析滴定数据,第4组实验数据偏高,分析过程发现滴定操作均规范正确,只是指示剂(二苯胺磺酸钠)滴加时多了几滴,请分析第4组数据异常原因___________ ;(二苯胺磺酸钠作氧化还原指示剂)
②计算该铁矿石中铁的质量分数为___________ (保留两位小数)。

已知:i.氧化性顺序:
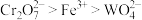 ;
;ii.氯化汞为弱电解质,具备一定氧化性;
iii.Sn在溶液中的主要存在形式为
 和
和 ;
;iv.五价钨溶液为蓝色。
请回答下列问题:
(1)目前三氯化钛—重铬酸钾滴定法使用率更高,其主要原因为
(2)提高“酸浸”速率可采取的措施是
(3)“还原”与“氧化除锡”过程的离子反应方程式分别为
(4)“
 还原”溶液仍呈浅黄色,而“
还原”溶液仍呈浅黄色,而“ 还原”后溶液呈现蓝色,则蓝色溶液中铁元素的主要存在形式为
还原”后溶液呈现蓝色,则蓝色溶液中铁元素的主要存在形式为 的作用为
的作用为(5)现称取3.0g铁矿石进行溶矿处理,采用三氯化钛—重铬酸钾滴定法,将“氧化除钨”后溶液定容至100mL,每次取20.00mL进行滴定,平行滴定4次,数据如下:
| 实验序号 | 1 | 2 | 3 | 4 |
消耗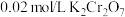 体积/mL 体积/mL | 34.95 | 35.05 | 35.00 | 36.30 |
②计算该铁矿石中铁的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】 (二氯化一氯五氨合钴)是一种易溶于热水、常温下难溶于水和乙醇的紫红色晶体。因在离子鉴定、电镀、医学方面的广泛应用受到人们的关注。
(二氯化一氯五氨合钴)是一种易溶于热水、常温下难溶于水和乙醇的紫红色晶体。因在离子鉴定、电镀、医学方面的广泛应用受到人们的关注。
某化学兴趣小组完成了部分该实验的实验报告:
一、实验步骤
Ⅰ.将适量氯化铵溶于浓氨水中,充分搅拌下,分批次加入 晶体,得到
晶体,得到 沉淀。
沉淀。
Ⅱ.边搅拌边慢慢滴入足量 溶液,得到
溶液,得到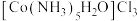 溶液。
溶液。
Ⅲ.慢慢注入适量浓盐酸,得到沉淀,水浴加热,冷却至室温,得到紫红色晶体,减压过滤。
Ⅳ.依次用不同试剂洗涤晶体,烘干,得到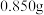 产品。
产品。
查阅资料显示: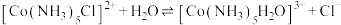
二、实验装置(部分)
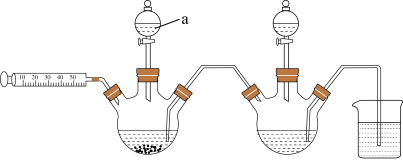
三、实验反思
(1)仪器a的名称是_______ 。
(2)本实验涉及钴配合物的配体有_______ (填化学式)。
(3)本实验应在通风橱中进行,原因是_______ 。
(4)步骤Ⅰ中分批次加入 晶体,原因是
晶体,原因是_______ 。
(5)步骤Ⅱ中加入双氧水的目的是_______ ;步骤Ⅲ中加入适量浓盐酸的目的是_______ 。
(6)步骤Ⅳ洗涤操作为:先用冷水洗涤,再用乙醇洗涤。其中,乙醇洗涤的目的是_______ 。
四、数据处理
(已知:产率 )
)
(7)该兴趣小组本次实验的产率是_______ 。(保留四位有效数字)
 (二氯化一氯五氨合钴)是一种易溶于热水、常温下难溶于水和乙醇的紫红色晶体。因在离子鉴定、电镀、医学方面的广泛应用受到人们的关注。
(二氯化一氯五氨合钴)是一种易溶于热水、常温下难溶于水和乙醇的紫红色晶体。因在离子鉴定、电镀、医学方面的广泛应用受到人们的关注。某化学兴趣小组完成了部分该实验的实验报告:
一、实验步骤
Ⅰ.将适量氯化铵溶于浓氨水中,充分搅拌下,分批次加入
 晶体,得到
晶体,得到 沉淀。
沉淀。Ⅱ.边搅拌边慢慢滴入足量
 溶液,得到
溶液,得到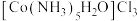 溶液。
溶液。Ⅲ.慢慢注入适量浓盐酸,得到沉淀,水浴加热,冷却至室温,得到紫红色晶体,减压过滤。
Ⅳ.依次用不同试剂洗涤晶体,烘干,得到
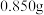 产品。
产品。查阅资料显示:
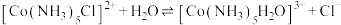
二、实验装置(部分)

三、实验反思
(1)仪器a的名称是
(2)本实验涉及钴配合物的配体有
(3)本实验应在通风橱中进行,原因是
(4)步骤Ⅰ中分批次加入
 晶体,原因是
晶体,原因是(5)步骤Ⅱ中加入双氧水的目的是
(6)步骤Ⅳ洗涤操作为:先用冷水洗涤,再用乙醇洗涤。其中,乙醇洗涤的目的是
四、数据处理
(已知:产率
 )
) (7)该兴趣小组本次实验的产率是
您最近一年使用:0次



