现有以下物质:①Fe2(SO4)3 ②Cu ③KIO3 ④Fe(OH)3胶体 ⑤FeSO4溶液 ⑥干冰 ⑦稀硝酸 ⑧乙醇 ⑨熔融碳酸钠。回答下列问题:
(1)以上物质中属于混合物的是_______ (填序号,下同);属于电解质的是_______ ;上述状态下能导电的是_______ 。
(2)①的电离方程式为_______ 。
(3)向④中逐滴滴加⑦,可观察到的现象是_______ 。
(4)⑤中混有少量①,除杂过程中选用的试剂为_______ 。
(5)向②中加入少量⑦,发生反应的离子方程式为_______ 。
(6)③可发生如下反应 (未配平);配平该反应并用双线桥法分析电子转移的情况:
(未配平);配平该反应并用双线桥法分析电子转移的情况:_______ ;每生成1.27 g I2,反应中转移电子的物质的量为_______ 。
(1)以上物质中属于混合物的是
(2)①的电离方程式为
(3)向④中逐滴滴加⑦,可观察到的现象是
(4)⑤中混有少量①,除杂过程中选用的试剂为
(5)向②中加入少量⑦,发生反应的离子方程式为
(6)③可发生如下反应
 (未配平);配平该反应并用双线桥法分析电子转移的情况:
(未配平);配平该反应并用双线桥法分析电子转移的情况:
更新时间:2023-01-15 18:32:58
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(1)除去Fe(OH)3胶体中混有的FeCl3的方法是_________________ 。
(2)在一定条件下,某固态化合物X受热分解的反应为:2X A↑+B↑+2C↑,测得反应后生成的混合气体的密度是同温同压下H2密度的12倍,则化合物X的摩尔质量为
A↑+B↑+2C↑,测得反应后生成的混合气体的密度是同温同压下H2密度的12倍,则化合物X的摩尔质量为_______ 。
(3)将标准状况下的a L HCl气体溶于1 L水中,得到的盐酸密度为b g/cm3,则该盐酸的物质的量浓度为________________ 。
(4)现有某温度下饱和NaCl溶液V mL,密度为ρg•cm-3,物质的量浓度为C mol•L-1则该温度下NaCl的溶解度为_________________ (用V、ρ、C表示)。
(5)有A、B、C、D 四种可溶性盐,它们的阳离子是Ba2+、Ag+、Na+、Cu2+ 中的某一种,阴离子是NO3-、SO42-、Cl-、CO32- 的某一种。
①若把四种盐分别溶解于盛有蒸馏水的四支试管中,C盐的溶液呈蓝色。
②若向①的四支试管中分别加盐酸,B溶液有沉淀产生,D溶液有无色无味气体逸出。
根据①②实验事实可推断它们的化学式为:
A、____________ C、______________ D、______________
(2)在一定条件下,某固态化合物X受热分解的反应为:2X
 A↑+B↑+2C↑,测得反应后生成的混合气体的密度是同温同压下H2密度的12倍,则化合物X的摩尔质量为
A↑+B↑+2C↑,测得反应后生成的混合气体的密度是同温同压下H2密度的12倍,则化合物X的摩尔质量为(3)将标准状况下的a L HCl气体溶于1 L水中,得到的盐酸密度为b g/cm3,则该盐酸的物质的量浓度为
(4)现有某温度下饱和NaCl溶液V mL,密度为ρg•cm-3,物质的量浓度为C mol•L-1则该温度下NaCl的溶解度为
(5)有A、B、C、D 四种可溶性盐,它们的阳离子是Ba2+、Ag+、Na+、Cu2+ 中的某一种,阴离子是NO3-、SO42-、Cl-、CO32- 的某一种。
①若把四种盐分别溶解于盛有蒸馏水的四支试管中,C盐的溶液呈蓝色。
②若向①的四支试管中分别加盐酸,B溶液有沉淀产生,D溶液有无色无味气体逸出。
根据①②实验事实可推断它们的化学式为:
A、
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】FeCl3是一种用途比较广泛的盐。
(1)印刷电路板是由高分子材料和铜箔复合而成。刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2.请写出反应的离子方程式______ 。
(2)FeCl3在天然水中可生成氢氧化铁胶体,其沉降水中悬浮物的速度高于铝盐(如硫酸铝等),是城市污水及工业废水处理的高效絮凝剂。实验室制取氢氧化铁胶体的方法是______ (填字母序号)。
A.将饱和的FeCl3溶液滴入沸水中,生成棕黄色液体即可。
B.在FeCl3溶液中加入足量的NaOH溶液
C.将饱和的FeCl3溶液滴入沸水,并继续煮沸至生成红褐色液体
D.将饱和的FeCl3溶液滴入沸水,并继续煮沸至生成红褐色沉淀
证明此胶体已经制成的最简单方法为______ 。
(3)FeCl3可使湿润的淀粉碘化钾试纸变蓝,化学方程式如下:2FeCl3+ 2KI = 2FeCl2+ I2+2KI,在上式上用双线桥法标出该反应电子转移的方向和数目_____ 。向反应后的溶液中加入CCl4溶液,振荡、静置后会发现下层液体的颜色为______ 色,再将混合液倒入______ (填仪器名称)中,将两层液体分离。
(1)印刷电路板是由高分子材料和铜箔复合而成。刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2.请写出反应的离子方程式
(2)FeCl3在天然水中可生成氢氧化铁胶体,其沉降水中悬浮物的速度高于铝盐(如硫酸铝等),是城市污水及工业废水处理的高效絮凝剂。实验室制取氢氧化铁胶体的方法是
A.将饱和的FeCl3溶液滴入沸水中,生成棕黄色液体即可。
B.在FeCl3溶液中加入足量的NaOH溶液
C.将饱和的FeCl3溶液滴入沸水,并继续煮沸至生成红褐色液体
D.将饱和的FeCl3溶液滴入沸水,并继续煮沸至生成红褐色沉淀
证明此胶体已经制成的最简单方法为
(3)FeCl3可使湿润的淀粉碘化钾试纸变蓝,化学方程式如下:2FeCl3+ 2KI = 2FeCl2+ I2+2KI,在上式上用双线桥法标出该反应电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】实验小组探究Fe(OH)3胶体的制备方法及其性质。

(1)制备Fe(OH)3胶体
①实验1,生成Fe(OH)3胶体和___________ (填化学式)。
②实验2与实验1对比,优点是___________ (写出1条即可)。
③综合上述实验:制备Fe(OH)3胶体提供OH-的物质可以是H2O或___________ ,控制反应条件即可制得。
(2)Fe(OH)3胶体的性质
资料:
Ⅰ、pH>10时,Fe(OH)3胶体溶解。
Ⅱ、固体FeCl3易升华(物质从固态不经过液态直接变成气态的过程)。
Ⅲ、Fe3+检验:若待测液中加入KSCN溶液,溶液变红色,则说明待测液中含有Fe3+。
实验4取5mL实验3得到的液体于蒸发皿中,继续加热,待蒸发皿中液体变为黏稠状,罩上漏斗,可观察到漏斗内出现棕褐色的烟,且有棕褐色固体附着在漏斗的内壁上。继续加热,蒸发皿中最终得到红棕色固体Fe2O3。
①根据资料,推测漏斗内棕褐色的烟中主要含有___________ (填化学式)。
②检验蒸发皿中红棕色固体中阳离子的方案:取少量红棕色固体溶于稀盐酸中,___________ 。
研究表明:Fe(OH)3胶体可净化水中的砷酸,砷酸浓度较低时以吸附为主,砷酸浓度较高时以反应为主。
③不同pH时,测得溶液中Fe(OH)3胶体对砷酸的吸附效率如图。pH为3~9时,Fe(OH)3胶体对砷酸的吸附效率高,pH较高时,吸附效率降低的原因是___________ 。

④去除水中高浓度砷酸的原理是Fe(OH)3胶体与砷酸反应生成砷酸铁(FeAsO4)沉淀,化学方程式是___________ 。

(1)制备Fe(OH)3胶体
| 实验 | 实验操作 | 丁达尔效应 |
| 1 | 向40mL沸腾的蒸馏水中滴入5滴饱和FeCl3溶液(浓度约为30%) | 迅速出现 |
| 2 | 向40mL蒸馏水中滴入5滴10%FeCl3溶液,然后滴入1滴10%NaOH溶液,边滴边搅拌 | 迅速出现 |
| 3 | 加热40mL饱和FeCl3溶液 | 一段时间后出现 |
②实验2与实验1对比,优点是
③综合上述实验:制备Fe(OH)3胶体提供OH-的物质可以是H2O或
(2)Fe(OH)3胶体的性质
资料:
Ⅰ、pH>10时,Fe(OH)3胶体溶解。
Ⅱ、固体FeCl3易升华(物质从固态不经过液态直接变成气态的过程)。
Ⅲ、Fe3+检验:若待测液中加入KSCN溶液,溶液变红色,则说明待测液中含有Fe3+。
实验4取5mL实验3得到的液体于蒸发皿中,继续加热,待蒸发皿中液体变为黏稠状,罩上漏斗,可观察到漏斗内出现棕褐色的烟,且有棕褐色固体附着在漏斗的内壁上。继续加热,蒸发皿中最终得到红棕色固体Fe2O3。
①根据资料,推测漏斗内棕褐色的烟中主要含有
②检验蒸发皿中红棕色固体中阳离子的方案:取少量红棕色固体溶于稀盐酸中,
研究表明:Fe(OH)3胶体可净化水中的砷酸,砷酸浓度较低时以吸附为主,砷酸浓度较高时以反应为主。
③不同pH时,测得溶液中Fe(OH)3胶体对砷酸的吸附效率如图。pH为3~9时,Fe(OH)3胶体对砷酸的吸附效率高,pH较高时,吸附效率降低的原因是

④去除水中高浓度砷酸的原理是Fe(OH)3胶体与砷酸反应生成砷酸铁(FeAsO4)沉淀,化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】正确认识物质分类,对学习化学知识有很大帮助。有下列物质:①铜 ②二氧化硫 ③氯化钠溶液 ④氯化氢 ⑤硫酸钡 ⑥氨气 ⑦酒精 ⑧硫酸溶液 ⑨氢氧化钠固体
请按要求回答下列问题:
(1)其中属于电解质的有___________ (填序号);
(2)属于非电解质的有___________ (填序号);
(3)能导电的有___________ (填序号);
(4)③和④___________ (填“能”或“不能”)发生离子反应,原因是___________
(5)请写出④和⑨反应的离子方程式:___________
请按要求回答下列问题:
(1)其中属于电解质的有
(2)属于非电解质的有
(3)能导电的有
(4)③和④
(5)请写出④和⑨反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】运用分类方法,可以发现物质及其变化的规律,预测物质的性质及可能发生的变化。科学的分类能够反映事物的本质特征,有利于人们分门别类地进行深入研究。利用所学过的知识回答下列问题:
有以下物质①石墨;②钠;③酒精;④氨气;⑤硫化氢;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氧化钠固体;⑩液态氯化氢。
(1)其中能导电的是_____ ;属于非电解质的是_____ 。
(2)等质量④和⑤中氢原子的数目之比为_____ ;若④和⑤中所含氢原子数相等,则④和⑤的质量之比为_____ 。
(3)写出⑥和⑩在水溶液中的离子方程式_____ 。
(4)室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2混合气体和1mol空气,此时活塞的位置如图所示。
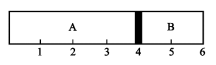
实验测得A室混合气体的质量为34g,若将A室H2、O2的混合气体点燃,恢复原温度后,(非气体体积忽略不计)最终活塞停留的位置在刻度_____ 处。
有以下物质①石墨;②钠;③酒精;④氨气;⑤硫化氢;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氧化钠固体;⑩液态氯化氢。
(1)其中能导电的是
(2)等质量④和⑤中氢原子的数目之比为
(3)写出⑥和⑩在水溶液中的离子方程式
(4)室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2混合气体和1mol空气,此时活塞的位置如图所示。

实验测得A室混合气体的质量为34g,若将A室H2、O2的混合气体点燃,恢复原温度后,(非气体体积忽略不计)最终活塞停留的位置在刻度
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】现有下列物质:①氢氧化钠固体 ②铜丝 ③氯化氢气体 ④稀硫酸 ⑤二氧化碳气体 ⑥氨水 ⑦碳酸氢钠固体 ⑧蔗糖晶体 ⑨碳酸钙固体 ⑩胆矾(CuSO4·5H2O)晶体
(1)上述物质相应状态下可导电的是_______ ;
(2)属于电解质的是_______ ;
(3)属于非电解质的是_______ ;
(4)⑦溶于水后的电离方程式是_______ ;
(5)①和⑦混合溶于水的离子方程式是_______ ;
(6)③溶于水形成的溶液与⑨反应的离子方程式是_________ 。
(1)上述物质相应状态下可导电的是
(2)属于电解质的是
(3)属于非电解质的是
(4)⑦溶于水后的电离方程式是
(5)①和⑦混合溶于水的离子方程式是
(6)③溶于水形成的溶液与⑨反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】近期央视播放了一套“大型文博探索节目”《国家宝藏》深受观众喜爱,其中由故宫博物院展出的《千里江山图卷》更是气象磅礴,吞吐山河,该卷长11.91米,颜色绚丽,由石绿,雌黄,赭石,砗磲,朱砂等颜料绘制而成,了解颜料的主要问题,回答以下问题:
(1)赭石,暗棕红色矿石,主要成分是氧化铁,遇盐酸可溶解, 工业炼铁常用含有氧化铁的赤铁矿为原料,在此过程中,炼铁的主要设备是________ ,炼铁的原料包括________ (填字母);
A.焦炭 B.铁矿石 C.烧碱 D.热空气
(2)用CO还原赤铁矿的主要原理是________ (用化学方程式表示)
(3)下列矿石主要成分为FeS2的是________ 。(填字母)
A.赤铁矿 B.磁铁矿 C.黄铁矿
(1)赭石,暗棕红色矿石,主要成分是氧化铁,遇盐酸可溶解, 工业炼铁常用含有氧化铁的赤铁矿为原料,在此过程中,炼铁的主要设备是
A.焦炭 B.铁矿石 C.烧碱 D.热空气
(2)用CO还原赤铁矿的主要原理是
(3)下列矿石主要成分为FeS2的是
A.赤铁矿 B.磁铁矿 C.黄铁矿
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】钠是一种非常活泼、具有广泛应用的金属。
(1)钠的原子结构示意图为___________ ,钠在反应中容易___________ 电子(填“得到”或“失去”)。
(2)汽车安全气囊的气体发生剂 可由金属钠生产。某汽车安全气囊内含
可由金属钠生产。某汽车安全气囊内含 、
、 和
和 等物质。
等物质。
ⅰ.当汽车发生较严重的碰撞时,引发 分解
分解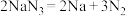 ,从而为气囊充气。产生的Na立即与
,从而为气囊充气。产生的Na立即与 发生置换反应生成
发生置换反应生成 ,化学方程式是
,化学方程式是___________ 。
ⅱ. 是冷却剂,吸收产气过程释放的热量。
是冷却剂,吸收产气过程释放的热量。 起冷却作用时发生反应的化学方程式为
起冷却作用时发生反应的化学方程式为___________ 。
ⅲ.一个安全气囊通常装有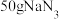 ,其完全分解所释放的
,其完全分解所释放的 为
为___________ mol。(保留两位小数)
(3)工业通过电解NaCl生产金属钠: ,过程如下:
,过程如下:
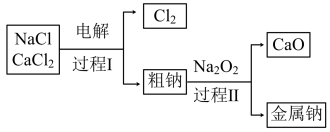
已知:电解时需要将NaCl加热至熔融状态。NaCl的熔点为801℃,为降低能耗,通常加入 从而把熔点降至约580℃。
从而把熔点降至约580℃。
①把NaCl固体加热至熔融状态,目的是___________ 。
②粗钠中含有少量杂质Ca,过程Ⅱ除去Ca的化学方程式是___________ 。
(1)钠的原子结构示意图为
(2)汽车安全气囊的气体发生剂
 可由金属钠生产。某汽车安全气囊内含
可由金属钠生产。某汽车安全气囊内含 、
、 和
和 等物质。
等物质。ⅰ.当汽车发生较严重的碰撞时,引发
 分解
分解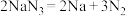 ,从而为气囊充气。产生的Na立即与
,从而为气囊充气。产生的Na立即与 发生置换反应生成
发生置换反应生成 ,化学方程式是
,化学方程式是ⅱ.
 是冷却剂,吸收产气过程释放的热量。
是冷却剂,吸收产气过程释放的热量。 起冷却作用时发生反应的化学方程式为
起冷却作用时发生反应的化学方程式为ⅲ.一个安全气囊通常装有
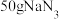 ,其完全分解所释放的
,其完全分解所释放的 为
为(3)工业通过电解NaCl生产金属钠:
 ,过程如下:
,过程如下:
已知:电解时需要将NaCl加热至熔融状态。NaCl的熔点为801℃,为降低能耗,通常加入
 从而把熔点降至约580℃。
从而把熔点降至约580℃。①把NaCl固体加热至熔融状态,目的是
②粗钠中含有少量杂质Ca,过程Ⅱ除去Ca的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】硫及其化合物在工业上有着广泛的应用。完成下列填空:
(1)写出工业上以硫磺为原料生产硫酸的第一步反应方程式______
(2)工业上用过硫酸钾(K2S2O8)测定钢铁中的锰含量,主要反应如下:____ Mn2++____ S2O82﹣+____ H2O→____ MnO4﹣+____ SO42﹣+______ H+。配平该反应方程式,氧化产物是______
(3)用电解硫酸氢钾的方法制取过硫酸钾:HSO4﹣在______ (填:“阳极”或“阴极”)反应生成S2O82﹣,另一极生成氢气,生成0.1mol的S2O82﹣同时可收集到______ g氢气
(4)已知硫酸的第二级电离并不完全:HSO4﹣ H++SO42﹣(Ki=1.2×10﹣2);在0.1mol/L的硫酸氢钾溶液中大约有30%的HSO4﹣电离,则该溶液中离子浓度由大到小排列第2位的离子是
H++SO42﹣(Ki=1.2×10﹣2);在0.1mol/L的硫酸氢钾溶液中大约有30%的HSO4﹣电离,则该溶液中离子浓度由大到小排列第2位的离子是____ ,第4位的离子是____ 。往该溶液中加入硫酸氢钾固体并保持温度不变,则溶液中
____ (填:“增大”、“减小”或“不变”)
(5)已知:HSO3﹣⇌H++SO32﹣K=1.02×10﹣7,NH4++H2O⇌NH3•H2O+H+ K=5.65×10﹣10。往亚硫酸氢铵中加入一定量的氢氧化钡溶液,可能发生的反应离子方程式是____ (选填编号)
a.HSO3﹣+Ba2++OH﹣=BaSO3↓+H2O
b.NH4++2HSO3﹣+2Ba2++3OH﹣=2BaSO3↓+2H2O+NH3•H2O
c.NH4++HSO3﹣+Ba2++2OH﹣=BaSO3↓+H2O+NH3•H2O
d.2NH4++4HSO3﹣+3Ba2++6OH﹣=3BaSO3↓+4H2O+2NH3•H2O+SO32﹣
(1)写出工业上以硫磺为原料生产硫酸的第一步反应方程式
(2)工业上用过硫酸钾(K2S2O8)测定钢铁中的锰含量,主要反应如下:
(3)用电解硫酸氢钾的方法制取过硫酸钾:HSO4﹣在
(4)已知硫酸的第二级电离并不完全:HSO4﹣
 H++SO42﹣(Ki=1.2×10﹣2);在0.1mol/L的硫酸氢钾溶液中大约有30%的HSO4﹣电离,则该溶液中离子浓度由大到小排列第2位的离子是
H++SO42﹣(Ki=1.2×10﹣2);在0.1mol/L的硫酸氢钾溶液中大约有30%的HSO4﹣电离,则该溶液中离子浓度由大到小排列第2位的离子是
(5)已知:HSO3﹣⇌H++SO32﹣K=1.02×10﹣7,NH4++H2O⇌NH3•H2O+H+ K=5.65×10﹣10。往亚硫酸氢铵中加入一定量的氢氧化钡溶液,可能发生的反应离子方程式是
a.HSO3﹣+Ba2++OH﹣=BaSO3↓+H2O
b.NH4++2HSO3﹣+2Ba2++3OH﹣=2BaSO3↓+2H2O+NH3•H2O
c.NH4++HSO3﹣+Ba2++2OH﹣=BaSO3↓+H2O+NH3•H2O
d.2NH4++4HSO3﹣+3Ba2++6OH﹣=3BaSO3↓+4H2O+2NH3•H2O+SO32﹣
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某兴趣小组利用铁在氧气中燃烧的产物磁性氧化铁做如下实验:
(1)磁性氧化铁与铝在一定条件下发生反应时,氧化剂与还原剂的物质的量之比为___________ 。将磁性氧化铁完全溶于较浓的盐酸中,得到棕黄色的浓溶液,其反应的离子方程式为___________ 取少量所得溶液加入双氧水,其反应的离子方程式为___________ 。
(2)取适量(1)中所得的棕黄色溶液于试管中,向其中加入稍过量的铁粉,发生主要反应的离子方程式为___________ ;静置后向上层清液中加入NaOH溶液,并放置一段时间,观察到的实验现象为___________ 。
(3)另取(1)中所得的棕黄色溶液于试管中,向其中通入足量的氯气,所发生反应的化学方程式为___________ 。写出高炉炼铁中一氧化碳还原氧化铁的化学方程式:___________ 。
(1)磁性氧化铁与铝在一定条件下发生反应时,氧化剂与还原剂的物质的量之比为
(2)取适量(1)中所得的棕黄色溶液于试管中,向其中加入稍过量的铁粉,发生主要反应的离子方程式为
(3)另取(1)中所得的棕黄色溶液于试管中,向其中通入足量的氯气,所发生反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】
(1)除去SiO2固体中混有的Al2O3, 其离子方程式为:_______ 。
(2)除去FeCl2溶液中的少量FeCl3, 其离子方程式为:_______ 。
(3)除去NaHCO3溶液中的少量Na2CO3, 其离子方程式为:_______ 。
(1)除去SiO2固体中混有的Al2O3, 其离子方程式为:
(2)除去FeCl2溶液中的少量FeCl3, 其离子方程式为:
(3)除去NaHCO3溶液中的少量Na2CO3, 其离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ、运用铁及其化合物的知识,完成下列各题。
(1)下列物质跟铁反应后的生成物,能跟KSCN溶液作用生成红色溶液的是________ 。
A.盐酸 B.氯气 C.CuSO4溶液 D.稀硫酸
(2)把过量的铁粉加入稀硝酸中,其结果是________ 。
A.不反应 B.生成硝酸铁 C.生成硝酸亚铁
(3)要除去FeCl2溶液中的少量FeCl3,可行的办法是________ 。
A.滴入KSCN溶液 B.通入氯气 C.加入铜粉 D.加入铁粉
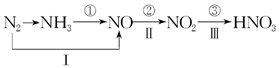
Ⅱ、工业上硝酸的制备和自然界中硝酸的生成既有相同的地方,又有区别。线路①、②、③是工业生产硝酸的主要途径,线路Ⅰ、Ⅱ、Ⅲ是雷电高能固氮过程中硝酸的生成途径。
(1)写出①步反应的化学方程式:____________________________________________________ 。
(2)下列环境问题与NO2的排放有关的是________ (填字母序号)。
A.赤潮 B.光化学烟雾 C.臭氧空洞 D.温室效应 E.酸雨
(3)若将12.8 g铜跟一定量的浓硝酸反应,铜消耗完时,共产生气体5.6 L(标准状况),则所消耗的硝酸的物质的量是________ 。
(1)下列物质跟铁反应后的生成物,能跟KSCN溶液作用生成红色溶液的是
A.盐酸 B.氯气 C.CuSO4溶液 D.稀硫酸
(2)把过量的铁粉加入稀硝酸中,其结果是
A.不反应 B.生成硝酸铁 C.生成硝酸亚铁
(3)要除去FeCl2溶液中的少量FeCl3,可行的办法是
A.滴入KSCN溶液 B.通入氯气 C.加入铜粉 D.加入铁粉
Ⅱ、工业上硝酸的制备和自然界中硝酸的生成既有相同的地方,又有区别。线路①、②、③是工业生产硝酸的主要途径,线路Ⅰ、Ⅱ、Ⅲ是雷电高能固氮过程中硝酸的生成途径。

(1)写出①步反应的化学方程式:
(2)下列环境问题与NO2的排放有关的是
A.赤潮 B.光化学烟雾 C.臭氧空洞 D.温室效应 E.酸雨
(3)若将12.8 g铜跟一定量的浓硝酸反应,铜消耗完时,共产生气体5.6 L(标准状况),则所消耗的硝酸的物质的量是
您最近一年使用:0次



