钠是一种非常活泼、具有广泛应用的金属。
(1)钠的原子结构示意图为___________ ,钠在反应中容易___________ 电子(填“得到”或“失去”)。
(2)汽车安全气囊的气体发生剂 可由金属钠生产。某汽车安全气囊内含
可由金属钠生产。某汽车安全气囊内含 、
、 和
和 等物质。
等物质。
ⅰ.当汽车发生较严重的碰撞时,引发 分解
分解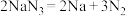 ,从而为气囊充气。产生的Na立即与
,从而为气囊充气。产生的Na立即与 发生置换反应生成
发生置换反应生成 ,化学方程式是
,化学方程式是___________ 。
ⅱ. 是冷却剂,吸收产气过程释放的热量。
是冷却剂,吸收产气过程释放的热量。 起冷却作用时发生反应的化学方程式为
起冷却作用时发生反应的化学方程式为___________ 。
ⅲ.一个安全气囊通常装有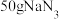 ,其完全分解所释放的
,其完全分解所释放的 为
为___________ mol。(保留两位小数)
(3)工业通过电解NaCl生产金属钠: ,过程如下:
,过程如下:
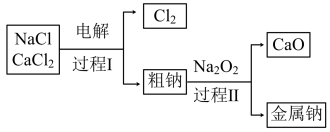
已知:电解时需要将NaCl加热至熔融状态。NaCl的熔点为801℃,为降低能耗,通常加入 从而把熔点降至约580℃。
从而把熔点降至约580℃。
①把NaCl固体加热至熔融状态,目的是___________ 。
②粗钠中含有少量杂质Ca,过程Ⅱ除去Ca的化学方程式是___________ 。
(1)钠的原子结构示意图为
(2)汽车安全气囊的气体发生剂
 可由金属钠生产。某汽车安全气囊内含
可由金属钠生产。某汽车安全气囊内含 、
、 和
和 等物质。
等物质。ⅰ.当汽车发生较严重的碰撞时,引发
 分解
分解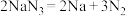 ,从而为气囊充气。产生的Na立即与
,从而为气囊充气。产生的Na立即与 发生置换反应生成
发生置换反应生成 ,化学方程式是
,化学方程式是ⅱ.
 是冷却剂,吸收产气过程释放的热量。
是冷却剂,吸收产气过程释放的热量。 起冷却作用时发生反应的化学方程式为
起冷却作用时发生反应的化学方程式为ⅲ.一个安全气囊通常装有
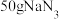 ,其完全分解所释放的
,其完全分解所释放的 为
为(3)工业通过电解NaCl生产金属钠:
 ,过程如下:
,过程如下:
已知:电解时需要将NaCl加热至熔融状态。NaCl的熔点为801℃,为降低能耗,通常加入
 从而把熔点降至约580℃。
从而把熔点降至约580℃。①把NaCl固体加热至熔融状态,目的是
②粗钠中含有少量杂质Ca,过程Ⅱ除去Ca的化学方程式是
更新时间:2024-01-19 09:41:56
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)下列粒子:①SO ②H2O③Na2O2④S2-⑤Fe⑥Al3+。在化学反应中可能被氧化也可能被还原的是
②H2O③Na2O2④S2-⑤Fe⑥Al3+。在化学反应中可能被氧化也可能被还原的是____ (填写序号);若少量的②与③充分反应,固体物质增重了0.6g,则生成的气体在标准状况下的体积为____ mL。
(2)在一定条件下,实验室分别用过氧化氢、高锰酸钾、氯酸钾、过氧化钠为原料制取氧气,当制得同温同压下相同体积的氧气时,四个反应中转移的电子的数之比为____ 。
(3)H2O2被称为绿色消毒剂,可用于消除采矿业废液中的KCN,发生反应为KCN+H2O2+H2O=A+NH3↑,则A的化学式为____ 。
(4)某反应体系中有六种粒子:H2O、S2-、S、H+、Mn2+、MnO ,其中S作氧化产物。写出并配平该反应的离子方程式,同时用双线桥标出电子转移的方向和数目
,其中S作氧化产物。写出并配平该反应的离子方程式,同时用双线桥标出电子转移的方向和数目___ 。
(1)下列粒子:①SO
 ②H2O③Na2O2④S2-⑤Fe⑥Al3+。在化学反应中可能被氧化也可能被还原的是
②H2O③Na2O2④S2-⑤Fe⑥Al3+。在化学反应中可能被氧化也可能被还原的是(2)在一定条件下,实验室分别用过氧化氢、高锰酸钾、氯酸钾、过氧化钠为原料制取氧气,当制得同温同压下相同体积的氧气时,四个反应中转移的电子的数之比为
(3)H2O2被称为绿色消毒剂,可用于消除采矿业废液中的KCN,发生反应为KCN+H2O2+H2O=A+NH3↑,则A的化学式为
(4)某反应体系中有六种粒子:H2O、S2-、S、H+、Mn2+、MnO
 ,其中S作氧化产物。写出并配平该反应的离子方程式,同时用双线桥标出电子转移的方向和数目
,其中S作氧化产物。写出并配平该反应的离子方程式,同时用双线桥标出电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氮的氢化物种类繁多,其中联氨(又称肼,N2H4,无色油状液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为__________________ ,其中氮的化合价为 _________ 。
(2) ①2O2(g)+N2(g)=N2O4(l) △H1
②N2(g)+2H2(g)=N2H4(l) △H2
③O2(g)+2H2(g)=2H2O(g) △H3
④2 N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) △H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=____________________ ,联氨和N2O4可作为火箭推进剂的主要原因为_________________________________________ 。
(3)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是固体逐渐变黑,并且有气泡产生,写出该反应的化学方程式__________________ 。
(4)联氨还可以用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2_____ kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是__________ 。
(1)联氨分子的电子式为
(2) ①2O2(g)+N2(g)=N2O4(l) △H1
②N2(g)+2H2(g)=N2H4(l) △H2
③O2(g)+2H2(g)=2H2O(g) △H3
④2 N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) △H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=
(3)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是固体逐渐变黑,并且有气泡产生,写出该反应的化学方程式
(4)联氨还可以用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有6.0gCO和CO2的混合气体,在标准状况下其体积为4.48L。请回答下列问题:
(1)该混合气体的平均摩尔质量为_________ 。
(2)将混合气体依次通过过量的溶液中,装置如图所示,最后收集在气球中(体积在标准状况下测定)。

①NaOH溶液中发生的离子反应方程式_________ 。
②气球的体积为_________  (忽略气球弹性的影响)。
(忽略气球弹性的影响)。
③若将混合气体通入足量的Na2O2中,转移的电子数为_________ (用NA表示)。
(1)该混合气体的平均摩尔质量为
(2)将混合气体依次通过过量的溶液中,装置如图所示,最后收集在气球中(体积在标准状况下测定)。

①NaOH溶液中发生的离子反应方程式
②气球的体积为
 (忽略气球弹性的影响)。
(忽略气球弹性的影响)。③若将混合气体通入足量的Na2O2中,转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(1)含氰废水中的CN-有剧毒。
①CN-中C元素显+2价,N元素显-3价,用原子结构解释N元素显负价的原因是___ ,共用电子对偏向N原子,N元素显负价。
②在微生物的作用下,CN-能够被氧气氧化成 ,同时生成NH3,该反应的离子方程式为
,同时生成NH3,该反应的离子方程式为______ 。
(2)含乙酸钠和对氯酚(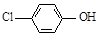 )的废水可以利用微生物电池除去,其原理如下图所示。
)的废水可以利用微生物电池除去,其原理如下图所示。
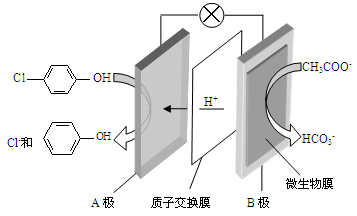
①B是电池的______ 极(填“正”或“负”);②A极的电极反应式为________ 。
(3)电渗析法处理厨房垃圾发酵液,同时得到乳酸的原理如下图所示(图中“HA”表示乳酸分子,A- 表示乳酸根离子)。

①阳极的电极反应式为________ 。
②简述浓缩室中得到浓乳酸的原理:_________ 。
③ 电解过程中,采取一定的措施可控制阳极室的pH约为6-8,此时进入浓缩室的OH-可忽略不计。400mL 10 g•L-1乳酸溶液通电一段时间后,浓度上升为145 g•L-1(溶液体积变化忽略不计),阴极上产生的H2在标准状况下的体积约为______ L。(乳酸的摩尔质量为90 g• mol-1)
(1)含氰废水中的CN-有剧毒。
①CN-中C元素显+2价,N元素显-3价,用原子结构解释N元素显负价的原因是
②在微生物的作用下,CN-能够被氧气氧化成
 ,同时生成NH3,该反应的离子方程式为
,同时生成NH3,该反应的离子方程式为(2)含乙酸钠和对氯酚(
 )的废水可以利用微生物电池除去,其原理如下图所示。
)的废水可以利用微生物电池除去,其原理如下图所示。
①B是电池的
(3)电渗析法处理厨房垃圾发酵液,同时得到乳酸的原理如下图所示(图中“HA”表示乳酸分子,A- 表示乳酸根离子)。

①阳极的电极反应式为
②简述浓缩室中得到浓乳酸的原理:
③ 电解过程中,采取一定的措施可控制阳极室的pH约为6-8,此时进入浓缩室的OH-可忽略不计。400mL 10 g•L-1乳酸溶液通电一段时间后,浓度上升为145 g•L-1(溶液体积变化忽略不计),阴极上产生的H2在标准状况下的体积约为
您最近一年使用:0次
【推荐2】查资料得:HNO2是一种弱酸且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是________ (填序号)。
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是________ (填序号)。
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI—淀粉溶液来区别
D.用AgNO3和HNO3两种试剂来区别
(3)某同学把酸性高锰酸钾溶液滴入NaNO2溶液中,观察到紫色褪去,同时生成NO3-和Mn2+,请写出反应的离子方程式:________ 。
(4)Fe与过量稀硫酸反应可制取FeSO4。若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是________ (填序号)。
A.Cl2 B.Fe C.H2O2 D.HNO3
(5)若FeSO4和O2的化学计量数比为2∶1,试配平下列方程式:
( ) FeSO4+( ) K2O2→( ) K2FeO4+( ) K2O+( ) K2SO4+( ) O2↑
(6)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成氢氧化铁胶体。高铁酸钾作为水处理剂发挥的作用是___________________ 。
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI—淀粉溶液来区别
D.用AgNO3和HNO3两种试剂来区别
(3)某同学把酸性高锰酸钾溶液滴入NaNO2溶液中,观察到紫色褪去,同时生成NO3-和Mn2+,请写出反应的离子方程式:
(4)Fe与过量稀硫酸反应可制取FeSO4。若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是
A.Cl2 B.Fe C.H2O2 D.HNO3
(5)若FeSO4和O2的化学计量数比为2∶1,试配平下列方程式:
(6)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成氢氧化铁胶体。高铁酸钾作为水处理剂发挥的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铁是一种重要的金属元素,其单质及其化合物在生产、生活中有着广泛的应用。回答下列问题:
(1)下列铁的化合物中,不能通过化合反应得到的是____ (填字母)。
A.Fe3O4 B.FeCl2 C.Fe(OH)2 D.FeCl3 E.Fe(OH)3
(2)FeS2高温灼烧,会产生大量的SO2,对环境产生污染。用铁盐溶液处理FeS2得到Fe2+和SO ,反应机理如图所示:
,反应机理如图所示:
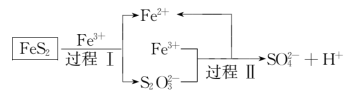
①过程Ⅰ中每有90gFeS2参与反应,理论上可还原___ molFe3+。
②总反应的离子方程式为___ 。
(3)已知FeCl3溶液与SO2的反应体系中存在下列两种化学变化:
Ⅰ.Fe3+与SO2发生络合反应生成Fe(SO2) (红棕色);
(红棕色);
Ⅱ.Fe3+与SO2发生氧化还原反应。
①写出反应Ⅱ的离子方程式:___ 。
②某学习小组为了探究FeCl3与SO2的反应情况,进行如下实验:
实验1:取5mL1mol•L-1FeCl3溶液于试管中,通入SO2至饱和,溶液很快由黄色变为红棕色。
实验2:用激光笔照射实验1中的红棕色溶液,溶液中无明显光路,说明红棕色物质不是___ (填分散系种类)。
实验3:将实验1中的溶液静置,1小时后,溶液逐渐变为浅绿色。
实验4:向实验3中的溶液加入2滴___ (填化学式)溶液,出现蓝色沉淀,说明有Fe2+。
若反应Ⅰ、Ⅱ的活化能分别为E1、E2,由上述实验可以得到的结论是:E1___ E2(填“>”“<”或“=”)。
实验5:另取5mL1mol•L-1FeCl3溶液于试管中,先滴加2滴浓盐酸,再通入SO2至饱和。几分钟后,溶液由黄色变为浅绿色,由此可知,促使氧化还原反应Ⅱ快速发生可采取的措施是___ 。
(1)下列铁的化合物中,不能通过化合反应得到的是
A.Fe3O4 B.FeCl2 C.Fe(OH)2 D.FeCl3 E.Fe(OH)3
(2)FeS2高温灼烧,会产生大量的SO2,对环境产生污染。用铁盐溶液处理FeS2得到Fe2+和SO
 ,反应机理如图所示:
,反应机理如图所示:
①过程Ⅰ中每有90gFeS2参与反应,理论上可还原
②总反应的离子方程式为
(3)已知FeCl3溶液与SO2的反应体系中存在下列两种化学变化:
Ⅰ.Fe3+与SO2发生络合反应生成Fe(SO2)
 (红棕色);
(红棕色);Ⅱ.Fe3+与SO2发生氧化还原反应。
①写出反应Ⅱ的离子方程式:
②某学习小组为了探究FeCl3与SO2的反应情况,进行如下实验:
实验1:取5mL1mol•L-1FeCl3溶液于试管中,通入SO2至饱和,溶液很快由黄色变为红棕色。
实验2:用激光笔照射实验1中的红棕色溶液,溶液中无明显光路,说明红棕色物质不是
实验3:将实验1中的溶液静置,1小时后,溶液逐渐变为浅绿色。
实验4:向实验3中的溶液加入2滴
若反应Ⅰ、Ⅱ的活化能分别为E1、E2,由上述实验可以得到的结论是:E1
实验5:另取5mL1mol•L-1FeCl3溶液于试管中,先滴加2滴浓盐酸,再通入SO2至饱和。几分钟后,溶液由黄色变为浅绿色,由此可知,促使氧化还原反应Ⅱ快速发生可采取的措施是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】根据你对金属钠性质的了解,回答下列问题:
(1)关于钠的叙述中,正确的是______(填字母)。
(2)由于金属钠很容易跟空气中的______ 、_____ 等物质反应,通常将它保存在______ 里。
(3)将一小块钠投入到下列溶液中,既能产生气体又会出现白色沉淀的是_____(填字母)。
(4)为粗略测定金属钠的相对原子质量,设计的装置如图所示,该装置(包括水)的总质量为ag,将质量为bg的钠放入足量水中,立即塞紧瓶塞。完全反应后再称量此装置的总质量为cg。

①无水氯化钙的作用是________ 。
②列出计算钠相对原子质量的数学表达式_______ (用含有a、b、c的算式表示)。
(1)关于钠的叙述中,正确的是______(填字母)。
| A.钠是银白色金属,硬度很大 |
| B.将钠放入坩埚,加热后钠剧烈燃烧,产生黄色火焰,生成过氧化钠 |
| C.钠长期放置于空气中,最终形成Na2CO3 |
| D.金属钠的熔点很高 |
(2)由于金属钠很容易跟空气中的
(3)将一小块钠投入到下列溶液中,既能产生气体又会出现白色沉淀的是_____(填字母)。
| A.稀硫酸 | B.硫酸铜溶液 | C.饱和NaOH溶液 | D.氯化镁溶液 |
(4)为粗略测定金属钠的相对原子质量,设计的装置如图所示,该装置(包括水)的总质量为ag,将质量为bg的钠放入足量水中,立即塞紧瓶塞。完全反应后再称量此装置的总质量为cg。

①无水氯化钙的作用是
②列出计算钠相对原子质量的数学表达式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】钠、氯及其化合物有如图转化关系,请按要求填空:
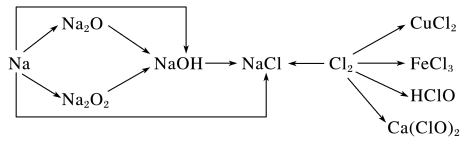
(1)金属钠的密度比水______ ,实验室中金属钠通常保存在______ 中。一小块金属钠投入水中的反应方程式是______ 。
(2)Na2O2是______ 色的固体,Na2O2的重要用途是______ ,有关反应的化学方程式为______ 。
(3)通常情况下,为了防止污染环境,在做完实验后,多余的氯气应用NaOH溶液吸收,其化学方程式为_____ 。
(4)新制的氯水滴入AgNO3溶液中,观察到______ 现象,原因是______ 。
(5)工业上用氯气和石灰乳反应制漂白粉,漂白粉的有效成分是____ ,漂白粉长时期露至在空气中会失效,用化学方程式表示其失效的原因:____ ,____ 。

(1)金属钠的密度比水
(2)Na2O2是
(3)通常情况下,为了防止污染环境,在做完实验后,多余的氯气应用NaOH溶液吸收,其化学方程式为
(4)新制的氯水滴入AgNO3溶液中,观察到
(5)工业上用氯气和石灰乳反应制漂白粉,漂白粉的有效成分是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】探究钠及其化合物的性质,请按要求填空:
(1)Na、Na2O、Na2O2、NaOH久置空气中最终都是变为_______ (填化学式);
(2)Na投入MgCl2溶液中发生反应的总化学方程式_______ 。(写一个方程式)
(3)向足量的蒸馏水中加入一定量Na2O2粉末,该反应的离子方程式为_______ 。
(1)Na、Na2O、Na2O2、NaOH久置空气中最终都是变为
(2)Na投入MgCl2溶液中发生反应的总化学方程式
(3)向足量的蒸馏水中加入一定量Na2O2粉末,该反应的离子方程式为
您最近一年使用:0次



