根据“机理图”书写方程式。
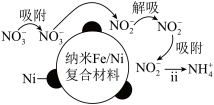
(1)酸性环境中脱硫过程示意图如图:

过程ⅰ反应的离子方程式为___________ 。
(2)酸性环境中,纳米 去除
去除 分两步,将步骤ⅱ补充完整:
分两步,将步骤ⅱ补充完整:___________ 。
ⅰ、 ;
;
ⅱ、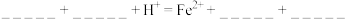 。
。
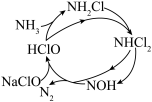
(3) 氧化可除去氨氮,反应机理如图所示(其中
氧化可除去氨氮,反应机理如图所示(其中 和略去):
和略去): 氧化
氧化 的总反应的化学方程式为
的总反应的化学方程式为___________ 。
(1)酸性环境中脱硫过程示意图如图:

过程ⅰ反应的离子方程式为
(2)酸性环境中,纳米
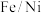 去除
去除 分两步,将步骤ⅱ补充完整:
分两步,将步骤ⅱ补充完整:
ⅰ、
 ;
;ⅱ、
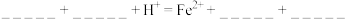 。
。(3)
 氧化可除去氨氮,反应机理如图所示(其中
氧化可除去氨氮,反应机理如图所示(其中 和略去):
和略去): 氧化
氧化 的总反应的化学方程式为
的总反应的化学方程式为
2023高三·全国·专题练习 查看更多[3]
更新时间:2023-02-04 17:18:20
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】某小组为了探究硫酸的性质,设计如下实验:
回答下列问题:
(1)实验①没有明显现象的原因是___________ ;改变一个条件,为使实验①中的反应持续发生,改变条件是___________ 。
(2)为了引发实验②中的反应,宜采取的措施是___________ ;实验后,观察产物水溶液的颜色,其操作方法是___________ 。
(3)实验④产生的气体是___________ (填化学式),比较实验③和④可知,从氧化还原角度分析,H+的作用是___________ ;写出该反应的离子方程式:___________ 。
(4)向实验④所得溶液中加入过量NaOH溶液得到沉淀M,用元素分析仪分析,M为铜的氧化物,提纯干燥后的M在惰性气体氛围下加热,12 g M完全分解为10 g CuO。M的化学式为___________ ;M能与稀硫酸酸化的KI溶液反应生成白色沉淀CuI(碘化亚铜),在滤液中加入淀粉溶液,溶液变蓝色。写出M和稀硫酸酸化的KI溶液反应的离子方程式:___________ 。
| 序号 | 操作 | 现象 |
| ① | 常温下,在铁片中加入过量的浓硫酸 | 没有明显现象 |
| ② | 常温下,在铜片上加入过量的浓硫酸 | 没有明显现象 |
| ③ | 在铜和过量30%H2O2的混合溶液中加入Na2SO4溶液 | 没有明显现象 |
| ④ | 在铜和过量30%H2O2的混合溶液中加入稀硫酸 | 溶液变蓝色,并产生气泡 |
(1)实验①没有明显现象的原因是
(2)为了引发实验②中的反应,宜采取的措施是
(3)实验④产生的气体是
(4)向实验④所得溶液中加入过量NaOH溶液得到沉淀M,用元素分析仪分析,M为铜的氧化物,提纯干燥后的M在惰性气体氛围下加热,12 g M完全分解为10 g CuO。M的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知反应:2KMnO4+16HCl(浓) = 2KCl+2MnCl2+5Cl2↑+8H2O
(1)请用双线桥法表示该反应___________ 。
(2)该反应的离子方程式是___________ 。
(3)浓盐酸在上述反应中显示出来的性质是___________(填序号)。
(4)该反应的氧化剂是___________ ,氧化产物是___________ ,氧化剂与还原剂的个数之比是___________ 。
(5)若生成 1 个 Cl2,则转移的电子数为___________ 。
(1)请用双线桥法表示该反应
(2)该反应的离子方程式是
(3)浓盐酸在上述反应中显示出来的性质是___________(填序号)。
| A.氧化性 | B.还原性 | C.酸性 | D.碱性 |
(5)若生成 1 个 Cl2,则转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)写出下列物质在水溶液中的电离方程式:
①KOH:_______________________________________________ ;
②KHSO4:____________________________________________ ;
③Fe2(SO4)3:__________________________________________ ;
(2)写出下列反应的离子方程式:
④Ba(OH)2溶液和H2SO4溶液反应________________________________________ ;
⑤Na2CO3溶液和HNO3溶液反应_________________________________________ ;
(3)配平下列方程式
⑥ NaClO3+ SO2+ H2SO4= ClO2+ NaHSO4_________________________________________ ;
⑦ Cl-+ MnO + H+= Mn2++ Cl2↑+ H2O
+ H+= Mn2++ Cl2↑+ H2O_________________________________________ 。
①KOH:
②KHSO4:
③Fe2(SO4)3:
(2)写出下列反应的离子方程式:
④Ba(OH)2溶液和H2SO4溶液反应
⑤Na2CO3溶液和HNO3溶液反应
(3)配平下列方程式
⑥ NaClO3+ SO2+ H2SO4= ClO2+ NaHSO4
⑦ Cl-+ MnO
 + H+= Mn2++ Cl2↑+ H2O
+ H+= Mn2++ Cl2↑+ H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】利用物质类别及核心元素的化合价推测物质的性质是研究化学的重要手段。硫元素的常见化合价与部分物质类别的对应关系如图。回答下列问题:
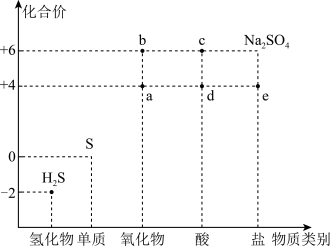
(1)将H2S与a混合,发生反应的氧化剂与还原剂的物质的量之比为_______ 。
(2)c的浓溶液能与H2S反应产生一种气体和淡黄色沉淀,写出此反应的化学方程式:_______ 。
(3)将a排入大气中会引起_______ 。
(4)硫元素还有一种常见的价态为-1价,如硫铁矿(主要成分为FeS2)中的硫元素。FeS2可以与Fe2(SO4)3溶液发生反应:7Fe2(SO4)3+FeS2+8H2O=15FeSO4+8H2SO4。该反应中的氧化剂是_______ (填化学式)。向反应后的溶液中通入空气能使Fe2(SO4)3溶液再生,写出再生反应的离子方程式:_______ 。
(5)常温下,c的浓溶液可用铁罐车或铝槽车运输,其原因是铁和铝在常温下遇到c的浓溶液会发生_______ 。
(6)若要验证木炭与c的浓溶液反应的产物中同时含有气体a和CO2,可选择以下试剂进行实验:
①NaOH溶液 ②品红溶液 ③溴水 ④Ca(OH)2溶液
选择合适试剂,并安排合理的顺序_______ (填序号)。

(1)将H2S与a混合,发生反应的氧化剂与还原剂的物质的量之比为
(2)c的浓溶液能与H2S反应产生一种气体和淡黄色沉淀,写出此反应的化学方程式:
(3)将a排入大气中会引起
(4)硫元素还有一种常见的价态为-1价,如硫铁矿(主要成分为FeS2)中的硫元素。FeS2可以与Fe2(SO4)3溶液发生反应:7Fe2(SO4)3+FeS2+8H2O=15FeSO4+8H2SO4。该反应中的氧化剂是
(5)常温下,c的浓溶液可用铁罐车或铝槽车运输,其原因是铁和铝在常温下遇到c的浓溶液会发生
(6)若要验证木炭与c的浓溶液反应的产物中同时含有气体a和CO2,可选择以下试剂进行实验:
①NaOH溶液 ②品红溶液 ③溴水 ④Ca(OH)2溶液
选择合适试剂,并安排合理的顺序
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2.已知该反应中H2O2只发生如下过程:H2O2→O2
(1)该反应中的还原剂是_______ 。
(2)写出该反应方程式并配平_______ 。
(3)如果反应转移了0.3 mol电子,则产生的气体在标准状况下的体积为_______ 。
(1)该反应中的还原剂是
(2)写出该反应方程式并配平
(3)如果反应转移了0.3 mol电子,则产生的气体在标准状况下的体积为
您最近一年使用:0次
【推荐3】国家实施“青山绿水”工程,加大力度研究脱硫及脱氮处理技术意义重大。回答下列问题:
(1)某工厂拟综合处理工业废气(主要含 、
、 、
、 、NO、CO),主要采用石灰乳、NaOH溶液等试剂。下列物质中,属于电解质的是
、NO、CO),主要采用石灰乳、NaOH溶液等试剂。下列物质中,属于电解质的是___________ (填序号)。
① ②
② ③CO ④石灰乳 ⑤NaOH
③CO ④石灰乳 ⑤NaOH
(2)写出少量 通入NaOH溶液的离子方程式:
通入NaOH溶液的离子方程式:___________ 。
(3)可用碱液吸收氮氧化物( )
)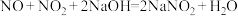 、
、
 。已知:NO与氢氧化钠溶液不反应。根据上述原理判断,将下列气体通入过量NaOH溶液中,反应结束后一定有剩余的是
。已知:NO与氢氧化钠溶液不反应。根据上述原理判断,将下列气体通入过量NaOH溶液中,反应结束后一定有剩余的是___________ (填字母)。
A.1mol NO和4mol B.1mol
B.1mol  和7mol NO C.6mol NO和4mol
和7mol NO C.6mol NO和4mol 
(4)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是硫酸。以下是二氧化硫形成酸雨的两种途径:
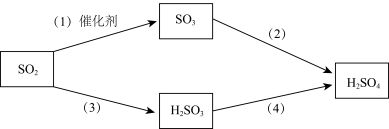
①请写出(1)中发生反应的化学方程式:___________ 。
②你认为减少酸雨产生的途径可采用的措施是___________ (填字母)。
A.少用煤作燃料 B.把工厂烟囱造高 C.燃料脱硫 D.在已酸化的土壤中加石灰 E.开发新能源
(5)利用 溶液可脱除二氧化硫,配平下列离子方程式:
溶液可脱除二氧化硫,配平下列离子方程式:_________

(6) 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,将烟气中
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,将烟气中 转化为无污染气体。当
转化为无污染气体。当 与NO的物质的量之比为1:1时,每转化1mol该氮氧化物混合气体,需要消耗标准状况下
与NO的物质的量之比为1:1时,每转化1mol该氮氧化物混合气体,需要消耗标准状况下 的体积为
的体积为___________ L。
(1)某工厂拟综合处理工业废气(主要含
 、
、 、
、 、NO、CO),主要采用石灰乳、NaOH溶液等试剂。下列物质中,属于电解质的是
、NO、CO),主要采用石灰乳、NaOH溶液等试剂。下列物质中,属于电解质的是①
 ②
② ③CO ④石灰乳 ⑤NaOH
③CO ④石灰乳 ⑤NaOH(2)写出少量
 通入NaOH溶液的离子方程式:
通入NaOH溶液的离子方程式:(3)可用碱液吸收氮氧化物(
 )
)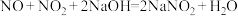 、
、
 。已知:NO与氢氧化钠溶液不反应。根据上述原理判断,将下列气体通入过量NaOH溶液中,反应结束后一定有剩余的是
。已知:NO与氢氧化钠溶液不反应。根据上述原理判断,将下列气体通入过量NaOH溶液中,反应结束后一定有剩余的是A.1mol NO和4mol
 B.1mol
B.1mol  和7mol NO C.6mol NO和4mol
和7mol NO C.6mol NO和4mol 
(4)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是硫酸。以下是二氧化硫形成酸雨的两种途径:

①请写出(1)中发生反应的化学方程式:
②你认为减少酸雨产生的途径可采用的措施是
A.少用煤作燃料 B.把工厂烟囱造高 C.燃料脱硫 D.在已酸化的土壤中加石灰 E.开发新能源
(5)利用
 溶液可脱除二氧化硫,配平下列离子方程式:
溶液可脱除二氧化硫,配平下列离子方程式:
(6)
 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,将烟气中
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,将烟气中 转化为无污染气体。当
转化为无污染气体。当 与NO的物质的量之比为1:1时,每转化1mol该氮氧化物混合气体,需要消耗标准状况下
与NO的物质的量之比为1:1时,每转化1mol该氮氧化物混合气体,需要消耗标准状况下 的体积为
的体积为
您最近一年使用:0次



